
【题目】氢氟酸能腐蚀玻璃。25℃下,向20mL0.2molL-1的氢氟酸中滴加0.2molL-1的NaOH溶液时,溶液的pH变化如图所示。
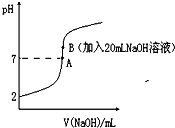
已知:电离度(α)和电离平衡常数(K)一样,可以用来衡量弱电解质在稀溶液中的电离能力。![]()
请回答下列问题:
(1)在氢氟酸的稀溶液中,通过改变以下条件能使氢氟酸的电离度[![]() (HF)]增大的是_______,可使氢氟酸的电离平衡常数[Ka(HF)] 增大的是_____________。
(HF)]增大的是_______,可使氢氟酸的电离平衡常数[Ka(HF)] 增大的是_____________。
a.升高温度 b.向溶液中滴入2滴浓盐酸 c.加入少量NaF固体 d.加水
(2)在此温度下,氢氟酸的电离平衡常数Ka(HF)为:_____,电离度α(HF)为______%。
(3)下列有关图中各点微粒浓度关系正确的是________。
a.在A处溶液中:c(F—)+c(HF)=0.2 molL-1
b.在B处溶液中:c(H+)+c(HF)= c(OH—)
c.在B处溶液中:c(Na+)>c(F—)>c(H+)>c(OH—)
d.在A和B处溶液中都符合:![]() = Ka(HF)
= Ka(HF)
(4)向此氢氟酸溶液中滴加10mlNaOH溶液后,请将HF分子与溶液中的离子浓度一起从大到小排序 ___________________________________________
【答案】 ad a 5.3×10-4 或5×10-4 5 b d C(F-)>C(Na+)> C(HF) >C(H+)>C(OH_)
【解析】(1)HF酸中存在HF H+ + F-,电离度![]() ,平衡常数Ka只与温度有关。a、HF的电离吸热,升高温度,平衡右移,电离度增大,Ka增大;b、向溶液中滴入2滴浓盐酸, H+浓度增大,平衡左移,电离度减小,Ka不变;c、加入少量NaF固体,F-浓度增大,平衡左移,电离度减小,Ka不变;d、加水稀释,促进电离,电离度增大,Ka不变。
,平衡常数Ka只与温度有关。a、HF的电离吸热,升高温度,平衡右移,电离度增大,Ka增大;b、向溶液中滴入2滴浓盐酸, H+浓度增大,平衡左移,电离度减小,Ka不变;c、加入少量NaF固体,F-浓度增大,平衡左移,电离度减小,Ka不变;d、加水稀释,促进电离,电离度增大,Ka不变。
故答案为:ad;a;
(2)由图象可知0.2molL-1的氢氟酸pH=2, c(H+)=0.01mol/L,则已电离c(HF)=0.01mol/L,α=![]() ,Ka=
,Ka=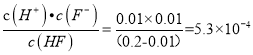
故答案为:5.3×10-4 或5×10-4; 5;
(3)a、该选项考查物料守恒,20mL0.2molL-1的氢氟酸中,物料守恒为:c(F-)+c(HF)=0.2molL-1,在A处溶液中,由于加入NaOH溶液,则溶液总体积大于20mL,则c(F-)+c(HF)<0.2molL-1,故a错误;b、在B处溶液中,HF和NaOH完全反应生成NaF,由质子守恒可知:c(H+)+c(HF)=c(OH-),故b正确;c、在B处溶液pH>7,则c(H+)<c(OH-),故c错误;d、由于温度不变,则电离常数不变,则在A和B处溶液中都符合: 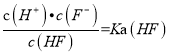 ,故d正确。
,故d正确。
故答案为:bd;
(4)向此氢氟酸溶液中滴加10mL NaOH溶液,反应后溶液为等物质的量HF和NaF的混合物,HF过量,溶液呈酸性,离子浓度大小关系应为c(F-)>c(Na+)>c(HF)>c(H+)>c(OH-),
故答案为:c(F-)>c(Na+)>c(HF)>c(H+)>c(OH-)。


科目:高中化学 来源: 题型:
【题目】为了能观察到丁达尔效应,一中鼹鼠科学社的同学在实验室制备Fe(OH)3胶体.
(1)胶体与其它分散系的本质区别是: .
(2)制备时,将逐滴滴加至中,待液体呈后,停止加热;反应方程式为 .
(3)有一种橘红色的硫化锑(Sb2S3)胶体,装入U型管,插入电极后通直流电,发现阳极附近橘红色加深,这叫现象,证明Sb2S3胶粒带电荷.
(4)如何设计实验验证制得的氢氧化铁是胶体: .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学用语是学习化学的重要工具。下列用来表示物质变化的化学用语中,不正确的是( )
A. 向沸水中滴加FeCl3溶液制备Fe(OH)3胶体:Fe3++3H2O![]() Fe(OH)3(胶体)+3H+
Fe(OH)3(胶体)+3H+
B. 明矾水解的离子方程式: Al3++ 3 H2O![]() Al(OH)3+3H+
Al(OH)3+3H+
C. 以石墨作电极电解氯化铝溶液:2Cl-+2H2O![]() 2OH-+H2↑+Cl2↑
2OH-+H2↑+Cl2↑
D. 硫化氢在水溶液中的电离方程式:H2S + H2O![]() HS- + H3O+
HS- + H3O+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在无色溶液中大量共存的一组离子是
A. Cu2+、SO42-、K+、Cl- B. Ag+、Cl-、OH-、Na+
C. NO3-、Cl-、Na+、Ca2+ D. NO3-、OH-、Mg2+、Na+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列试剂的保存或盛装方法中,错误的是
A. 钠保存在煤油中
B. 铁罐贮存浓硝酸
C. 新制的氯水保存在棕色玻璃瓶中
D. NaOH 溶液盛装在带玻璃塞的玻璃瓶中
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法或有关化学用语的表达正确的是( )
A.在基态多电子原子中,p轨道电子能量一定高于s轨道电子能量
B.基态Fe原子的外围电子排布图为: ![]()
C.因氧元素电负性比氮元素大,故氧原子第一电离能比氮原子第一电离能大
D.根据原子核外电子排布的特点,Cu在周期表中属于s区元素
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com