
【题目】将CH3COOH溶液逐滴加入到NaOH溶液中,至溶液为中性。此时溶液中( )
A. c(CH3COO-)=c(Na+) B. c(CH3COOH)< c(Na+)
C. c(CH3COO-)>c(Na+) D. c(CH3COO-)和c(Na+)的大小无法比较
科目:高中化学 来源: 题型:
【题目】利用废旧镀锌铁皮可制备磁性Fe3O4胶体粒子及副产物ZnO,制备流程如下图所示:
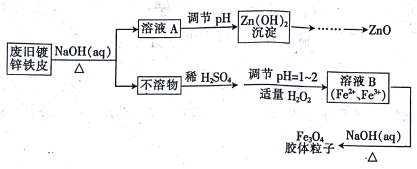
(1)从流程图可知,Zn、Fe中能与NaOH溶液反应的是________。
(2)Zn(OH)2沉淀加热可得ZnO,该反应______(填“是”或“不是”)氧化还原反应。
(3)向不溶物中加入稀H2SO4发生反应的离子方程式是_________。
(4)加入适量H2O2的目的是_________。
(5)如何证明已生成了Fe3O4胶体? _________。
(6)流程中所需的硫酸溶液由焦硫酸(H2SO4·SO3)溶于水配制而成,其中的SO3都转化为硫酸,若将445g焦硫酸溶于水配成4.00L 硫酸,该硫酸的物质的量浓度为__mol/L
(7)稀硫酸也可以用浓硫酸和水配制。已知4mol/L的硫酸溶液密度为ρ1 g/cm3,2mol/L的硫酸溶液密度为ρ2 g/cm3。100g物质的量浓度为4mol/L 的硫酸溶液与___mL水混合,使硫酸的物质的量浓度减小到2mol/L。(用含ρ1、ρ2的式子表示)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.CH3COOCH2CH3与CH3CH2COOCH3为同一种物质
B.C70与14C互为同素异形体
C.乙醇易溶于水,丙三醇(甘油)难溶于水
D.2,2﹣二甲基丙烷的一氯代物只有一种结构
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA表示阿伏加德罗常数,下列叙述中正确的是 ( )
A. 常温常压下,11.2 LCO2所含的原子数为1.5NA
B. 常温常压下,48 g O3含有的氧原子数为3NA
C. 标准状况下,224 L H2中所含原子数为NA
D. 标准状况下,1 L水所含分子数为![]() NA
NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有CO和CO2的混合气体,在标准状况下的体积为11.2L。请回答下列问题:
(1)该混合气体总的物质的量为_______。
(2)混合气体中碳原子的个数为___________。(用NA表示阿伏加德罗常数的值)
(3)为测定混合气体的组成,将该混合气体全部通过下图装置进行实验。经测定,A瓶中得到白色沉淀19.7g。
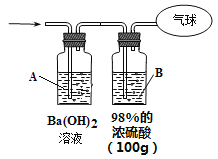
①从A瓶中获得沉淀质量的操作是_____________________称量。
②Ba(OH)2溶液浓度的测定。步骤如下:
a、过滤A溶液,得到滤液100mL(忽略溶液体积的微小变化)
b、将B瓶中的溶液配成1L溶液
c、将B瓶配制的溶液慢慢加入100mL滤液中直到不再产生沉淀。共消耗配制液50mL。
则步骤c中得到的沉淀的物质的量为______________。 原Ba(OH)2溶液的浓度为___________。
③气球中收集到的气体的质量为___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】【吉林大学附属中学2017届第八次模拟考试】麻黄素是中枢神经兴奋剂,其合成路线如图所示。NBS是一种选择性溴代试剂。

已知:![]()
(1)其中A为烃,相对分子质量为92,A的结构简式是________________;
E中官能团的名称为___________________。
(2)反应B→C的反应条件和试剂是_______________,⑤的反应类型是________。
(3)F的结构简式是____________________________。
(4)写出C→D的化学方程式______________________________________。
(5)化合物F的芳香族同分异构体有多种,M和N是其中的两类,它们的结构和性质如下:
①已知M遇FeCl3溶液发生显色反应,能和银氨溶液发生银镜反应,苯环上只有两个对位取代基,则M的结构简式可能为___________________________________。
②已知N分子中含有甲基,能发生水解反应,苯环上只有一个取代基,则N的结构有_____种。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示(B中冷却装置未画出),将氯气和空气(不参与反应)以体积比约1∶3混合通入含水8%的碳酸钠中制备Cl2O,并用水吸收Cl2O制备次氯酸溶液。
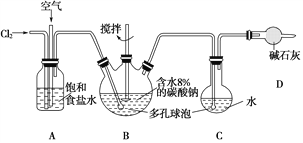
已知:Cl2O极易溶于水并与水反应生成HClO;Cl2O的沸点为3.8℃,42℃以上分解为Cl2和O2。
(1)①实验中控制氯气与空气的体积比的方法是___________________________________。
②使用多孔球泡的作用是_____________________________________。
(2)①装置B中产生Cl2O的化学方程式为____________________________________。
②若B无冷却装置,进入C中的Cl2O会大量减少。其原因是___________________________。
(3)装置C中采用棕色圆底烧瓶是因为________________________________。
(4)已知次氯酸可被H2O2、FeCl2等物质还原成Cl-。测定C中所得次氯酸溶液的物质的量浓度的实验方案:用_________量取20.00 mL次氯酸溶液于烧杯中,_____________________________。(可选用的试剂:H2O2溶液、FeCl2溶液、AgNO3溶液。除常用仪器外须使用的仪器有:电子天平,真空干燥箱)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com