
【题目】为验证卤素单质氧化性的相对强弱,某小组用下图所示装置进行实验(夹持仪器已略去,气密性已检验)。B、C中均加有10mL 1mol/L的NaBr溶液。

实验过程:
Ⅰ.打开弹簧夹,打开活塞a,滴加浓盐酸。
Ⅱ.当B和C中的溶液都变为黄色时,夹紧弹簧夹。
Ⅲ.当B中溶液由黄色变为红棕色时,关闭活塞a。
Ⅳ.打开活塞b,将少量液体放入D中,取下试管并振荡。
(1)验证氯气的氧化性强于碘的实验现象是________________________________________。
(2)B中溶液发生反应的化学方程式是____________________________________________。
(3)过程Ⅳ中出现的现象是________,由此可证明氧化性较强的是________(填“Br2”或“I2”)。
(4)设计过程Ⅲ的目的是__________________________________________________________。
【答案】淀粉KI试纸变蓝 Cl2+2NaBr→2NaCl+Br2 溶液分层,下层溶液呈紫红色 Br2 确认C的黄色溶液中无氯气,排除氯气对溴置换碘实验的干扰
【解析】
⑴黄绿色气体为氯气,由高锰酸钾和浓盐酸发生氧化还原反应生成,生成的氯气在A中,淀粉变蓝色,说明有单质碘生成,也说明氯气氧化性强于单质碘,故答案为淀粉KI试纸变蓝;
⑵氯气在B中和溴化钠反应:Cl2+2NaBr = 2NaCl+Br2,故答案为Cl2+2NaBr = 2NaCl+Br2;
⑶打开活塞b,将少量C中溶液滴入D中,关闭活塞b,取下D振荡、静至后溶液分层,CCl4层溶液变为紫红色,发生反应为:Br2+2NaI = 2NaBr+I2,氧化性强的为Br2,故答案为溶液分层,下层溶液呈紫红色;Br2;
⑷为验证溴的氧化性强于碘,实验时应避免氯气的干扰,当B中溶液由黄色变为棕红色时,说明有大量的溴生成,此时应关闭活塞a,否则氯气过量,影响实验结论,故答案为:确认C的黄色溶液中无氯气,排除氯气对溴置换碘实验的干扰。


科目:高中化学 来源: 题型:
【题目】(1)钙原子的结构示意图为_____。
(2)氧离子电子式为_____。
(3)0℃,1atm时,CO2的气体摩尔体积约为_____L/mol。
(4)1个普通水分子的质量大约是_____g。
(5)常温下,水的摩尔体积约为_____cm3/mol。
(6)已知n个12C原子的质量是a克,则m个32S原子的质量约是_____。
(7)电解饱和食盐水的方程式为_____;工业制漂白粉的方程式为_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用木质纤维可合成药物中间体H,还能合成高分子化合物G,合成路线如下:

已知:
①![]() ②
②![]()
(1)A的化学名称是___________________。
(2)B的结构简式是_____________,由C生成D的反应类型为_____________________。
(3)化合物E的官能团为__________________________。
(4)F分子中处于同一平面的原子最多有___________个。F生成G的化学反应方程式为_________________________________。
(5)芳香化合物I为H的同分异构体,苯环上一氯代物有两种结构,1molI发生水解反应消耗2mol NaOH,符合要求的同分异构体有______种,其中核磁共振氢谱显示有4种不同化学环境的氢,峰面积比为6:3:2:1的I结构简式为__________________________。
(6)写出用 为原料制备
为原料制备![]() 的合成路线(其他试剂任选)__________。
的合成路线(其他试剂任选)__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)顺铂(化学名称为顺二氯二氨合铂(II),化学式为PtCl2(NH3)2,相对分子质量为:300)是一种用于治疗癌症的药物,一片顺铂药片所含顺铂的质量为6×10-4g。那么一片顺铂药片中N原子的物质的量________;
(2)乙烯气体(C2H4)是石油化工产品之一,也是最重要的有机化工基础原料之一,在标准状况下其密度为_______g.L-1;(已知:标准状况下,Vm=22.4Lmol-1 )
(3)现有一种矿泉水样品,1.0升的该矿泉水含有4.8×10-2gMg2+。则________升矿泉水中含有1molMg2+;
(4)某“84消毒液”1000mL.其有效成分为NaClO(式量:74.5),质量分数为14.9%,密度为1.2g/L。其溶质的物质的量浓度为________;
(5)已知CO和CO2的混合气体7.2g。在标准状况下所占的体积为4.48L。则该混合气体中氧元素的质量为_______;
(6)如图所示两瓶体积相等的气体,在同温同压下,若瓶1两种气体______(填“物质的量”或者“质量”)相等,则两瓶中的气体原子总数和质量均相等。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高铁酸钠(Na2FeO4)(铁为+6价)是一种新型的净水剂,可以通过下述反应制取:
(1)配平下列化学方程式,并标明电子转移的方向与数目:
________Fe(OH)3+________NaOH+________NaClO→________Na2FeO4+________NaCl+________H2O,___________
(2)该反应中还原产物是________(填写化学式),________元素被氧化,氧化剂的电子式为________。
(3)当反应中有1mol Na2FeO4生成,转移的电子有________mol.
(4)如果配制250mL 0.1mol/L NaOH溶液,需要称取________g NaOH固体,所需的仪器有玻璃棒、胶头滴管、烧杯、________、________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮化铝(AlN)是一种新型非金属材料,室温下能缓慢水解。可由铝粉在氮气氛围中1700℃合成,产物为白色到灰蓝色粉末。某小组探究在实验室制备AlN并测定产品纯度,设计实验如下。请回答:
(一)制备AlN

(1)按气流由左向右的方向,上述装置的正确连接顺序为j→__________________→i(填仪器接口字母编号)。
(2)实验时,以空气为原料制备AlN。装置A中还原铁粉的作用为________________,装置B中试剂X为_____________________。
(二)测定产品纯度
取m g的产品,用以下装置测定产品中AlN的纯度(夹持装置已略去)。
已知:AlN + NaOH + H2O = NaAlO2 + NH3↑
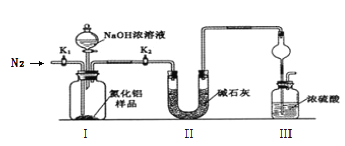
(3)完成以下实验步骤:组装好实验装置,首先_________________________________,加入实验药品。接下来的实验操作是关闭______________________________并打开______________,再打开分液漏斗活塞加入足量NaOH浓溶液后关闭,至不再产生气体。再______________,通入氮气一段时间,测定装置III反应前后的质量变化为n g。
(4)实验结束后,计算产品中AlN的纯度为___________﹪(用含m、n的代数式表示)。
(5)上述实验的设计仍然存在缺陷,你认为可能的缺陷及会导致的测定结果____________(用 “偏高”、“偏低”描述)如何______________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究表明,大气中氮氧化物和碳氢化合物受紫外线作用可产生二次污染物——光化学烟雾,其中某些反应过程如图所示。下列说法不正确的是

A. 整个过程中O3作催化剂
B. 反应III的方程式为O2+O===O3
C. 光化学烟雾中含甲醛、乙醛等刺激性物质
D. 反应I、反应Ⅱ均属于氧化还原反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钛(T)因具有硬度大、熔点高、耐酸腐蚀等优点而被应用于航空、电子等领域,由钛铁矿(主要成分是钛酸亚铁FeTiO3)提取金属钛并获得副产品FeSO4·7H2O的工艺流程如下:

(1)钛铁矿和浓硫酸反应的产物之一是 TiOSO4。常温下,该物质易溶于酸性溶液,在pH=5.0时开始转化为钛酸沉淀,则物质A是___________(填化学式,下同),B是___________;步骤Ⅳ生成TiO(OH)2(H2TiO3)的离子方程式是______________________。
(2)已知FeSO4·7H2O和TiOSO4的溶解度曲线如图所示,则步骤Ⅲ采用的操作是___________。

(3)工业上可通过下列反应由TiO2制备金属Ti:
TiO2+2C+2Cl2![]() TiCi4+2CO
TiCi4+2CO
TiCl4+2Mg![]() Ti+2MgCl2
Ti+2MgCl2
已知:常温下TiCl4是一种极易水解的无色液体,沸点为136.4℃。
①从下列供选用的装置中选择合适的装置制备TiCl4,按气流方向连接起来:A→___________→___________→___________→___________→C→___________。

②下列仪器中盛放的药品分别是B___________,G___________。
(4)一定条件下,将TiO2溶解并还原为Ti3+,再以KSCN溶液作指示剂,用NH4Fe(SO4)2标准溶液滴定Ti3+至全部生成Ti4+。称取TiO2样品0.60g,消耗0.20mol/L的NH4Fe(SO4)2溶液36.75mL,则样品中TiO2的质量分数是___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质互为同系物的是
A. 35Cl和37ClB. O2和O3C. C2H6和C5H12D. CH3CH2CH2CH3和CH3CH(CH3)2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com