
【题目】下列指定反应的离子方程式正确的是
A. 硫酸铝溶液中加入过量的氨水:A13++4NH3H2O=A1O2-+4NH4+
B. 稀硝酸中加入过量铁粉:Fe+4H++NO3-=Fe3++NO↑+2H2O
C. 浓盐酸与二氧化锰混合加热:MnO2+4H++2Cl-![]() Mn2++Cl2↑+2H2O
Mn2++Cl2↑+2H2O
D. 石灰水中加入过量小苏打溶液:HCO3-+Ca2++OH-=CaCO3↓+H2O
【答案】C
【解析】
A.向硫酸铝溶液中加入过量氨水,反应的离子方程式为:Al3++3NH3H2O═Al(OH)3↓+3NH4+,故A错误;
B.稀硝酸中加入过量铁粉,反应生成亚铁离子,正确的离子方程式为:3Fe+8H++2NO3-=3Fe2++2NO↑+4H2O,故B错误;
C.二氧化锰与浓盐酸混合加热,反应生成氯化锰、氯气和水,反应的离子方程式为:MnO2+4H++2Cl- ![]() Mn2++Cl2↑+2H2O,故C正确;
Mn2++Cl2↑+2H2O,故C正确;
D.碳酸氢钠过量,离子方程式按照氢氧化钙的组成书写,碳酸根离子有剩余,正确的离子方程式为:Ca2++2HCO3-+2OH-═CaCO3↓+2H2O+CO32-,故D错误;
答案选C。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】某研究性学习小组设计如下实验装置进行探究。
⑴装置A中反应的化学方程式为____________。
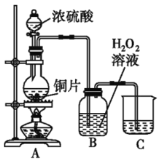
⑵实验结束后,欲验证反应生成的气体具有还原性,小组同学取装置B中溶液少量于一洁净的试管中,应向试管中加入的试剂是___。(填字母)。
a.品红溶液 b.稀盐酸 c.BaCl2溶液 d.稀硝酸
⑶实验结束,小组同学立即熄灭酒精灯,可能导致的后果是______________。
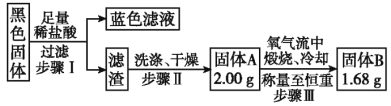
⑷实验结束,发现在铜片表面附着黑色固体。查阅资料得知此黑色固体可能含有CuO、CuS、Cu2S。常温下CuS和Cu2S都不溶于稀盐酸,在空气中煅烧都转化为CuO和SO2。该小组同学收集一定量黑色固体,按如下实验方案探究其成分:
①步骤Ⅱ中检验滤渣是否洗涤干净的实验方法是_______________。
②黑色固体的成分是_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关图像的说法正确的是

A. 图甲表示:向某明矾液中滴加过量的NaOH溶液,生成沉淀的物质的量与滴加NaOH溶液体积的关系
B. 图乙表示:向含等物质的量的NaOH和Na2CO3的混合溶液中滴加过量的稀盐酸,生成气体的体积与滴加HC1溶液体积的关系
C. 图丙表示:在稀硝酸溶液中加入过量的铁粉,溶液中Fe3+物质的量与加入铁粉物质的量的变化关系
D. 根据图丁,除去混在KNO3中少量的NaCl可用蒸发结晶的方法
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下反应:A2(气)+B2(气)![]() 2AB(气)达平衡状态的标志是( )
2AB(气)达平衡状态的标志是( )
A.单位时间内生成n摩A2,同时生成n摩AB
B.单位时间内生成n摩B2,同时生成2n摩AB
C.单位时间内生成n摩A2,同时生成n摩B2
D.容器内总物质的量不变(或总压不变)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA为阿伏加德罗常数的值。下列说法正确的是
A. 18g重水(D2O)所含的电子数目为10NA
B. Na2O2与足量的水反应生成1 molO2,转移电子数目为2NA
C. 100 mL1 molL-1 FeCl3溶液中含有 Fe3+数目为 0.1NA
D. 将2molSO2和1molO2充分反应,转移的电子数目为4NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铁、钴(Co)属于第四周期第VIII族元素,含铁、钴化合物具有诸多用途。回答下列问题:
(1)基态Co原子价层电子的电子排布图(轨道表达式)为________________。
(2)Co的配合物[Co(NH3)5Cl]SO4是一种重要的化合物。
①SO42-的空间立体构型为___________,其中S原子的杂化轨道类型是___________,写出一种与SO42-互为等电子体的分子的化学式:______________。
②[Co(NH3)5Cl]SO4中,N、O、S三种元素的第一电离能由大到小的顺序为_______________。
③[Co(NH3)5Cl]SO4中,存在___________(填字母)
a.离子键 b.金属键 c.配位键 d.非极性键 e.极性键
(3)铁氰化钾{K3 [Fe(CN)6]}溶液是检验Fe2+常用的试剂。
①1mol [Fe(CN)6]3-含![]() 键的数目为__________。
键的数目为__________。
②CN-能与多种离子形成配合物,碳原子提供孤电子对,而不是氮原子,其原因是____________。
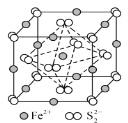
③FeS2晶体的晶胞如图所示。晶胞边长为a nm、FeS2相对分子质量为M,阿伏加德罗常数的值为NA,其晶体密度的计算表达式为______gcm-3;晶胞中Fe2+位于S22-所形成的正八面体的体心,该正八面体的边长为_________nm。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯元素在自然界有35Cl和37Cl两种同位素,氯元素的相对原子质量为35.5,则35Cl和37Cl的原子个数比为____;由Na、35Cl和37C构成的11.7g氯化钠中含35Cl的质量是___g;11.7g该晶体刚好能和某200mL的AgNO3溶液完全反应,则该AgNO3溶液的物质的量浓度是___mol/L。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知化学反应A2(g)+ B2(g) = 2AB(g)的能量变化如图所示,判断下列叙述中正确的是

A.每生成2分子AB吸收bkJ热量
B.断裂1molA—A和1molB—B键,放出akJ能量
C.该反应中反应物的总能量高于生成物的总能量
D.该反应热△H=+(a-b)kJ/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用如图所示装置进行下列实验:将①中溶液滴入②中,预测的现象与实际相符的是( )
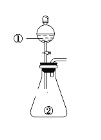
选项 | ①中物质 | ②中物质 | 预测②中的现象 |
A | 稀盐酸 | 碳酸钠与氢氧化钠的混合溶液 | 立即产生气泡 |
B | 浓硝酸 | 用砂纸打磨过的铝条 | 产生红棕色气体 |
C | 氯化铝溶液 | 浓氢氧化钠溶液 | 产生大量白色沉淀 |
D | 草酸溶液(H2C2O4具有还原性) | 高锰酸钾酸性溶液 | 溶液逐渐褪色 |
A.AB.BC.CD.D
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com