
A、 |
B、 |
C、 |
D、 |


科目:高中化学 来源: 题型:
| A、ClO2 |
| B、Cl2O3 |
| C、Cl2O |
| D、Cl2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、体系的压强不再改变 |
| B、混合气体密度不再改变 |
| C、反应速率3υA(正)=2υC(逆) |
| D、混合气体平均相对分子质量不再改变 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、该反应属于分解反应、氧化还原反应、放热反应 |
| B、该反应瞬间能产生大量高温气体,推动飞船飞行 |
| C、从能量变化上看,该反应是化学能转变为热能和动能 |
| D、反应中NH4ClO4只起到氧化剂的作用 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、要实现Fe2+→Fe3+的转化,必须加入还原剂 |
| B、在反应CaH2+2H2O═Ca(OH)2+2H2↑,水作氧化剂 |
| C、反应2H2S+SO2═3S+2H2O中氧化剂和还原剂的物质的量之比是2:1 |
| D、因Cl2的氧化性强于I2的氧化性,所以置换反应I2+2 NaClO3═2NaIO3+Cl2不能发生 |
查看答案和解析>>
科目:高中化学 来源: 题型:
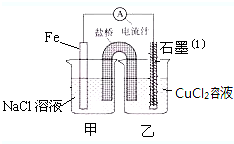 某实验小组的同学对电化学原理进行了一系列探究活动
某实验小组的同学对电化学原理进行了一系列探究活动查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com