
| Br2 |
| Cu/O2 |
| △ |

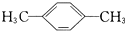 的系统命名为
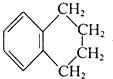
的系统命名为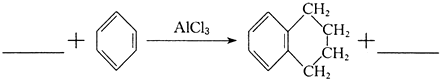
 ,对二甲苯被酸性高锰酸钾溶液氧化生成X为
,对二甲苯被酸性高锰酸钾溶液氧化生成X为 ,对苯二甲酸与乙二醇发生缩聚反应生成聚对苯二甲酸乙二醇酯.
,对苯二甲酸与乙二醇发生缩聚反应生成聚对苯二甲酸乙二醇酯.| 水 |
| △ |
| 水 |
| △ |
| △ |
| △ |
 ,对二甲苯被酸性高锰酸钾溶液氧化生成X为
,对二甲苯被酸性高锰酸钾溶液氧化生成X为 ,对苯二甲酸与乙二醇发生缩聚反应生成聚对苯二甲酸乙二醇酯,
,对苯二甲酸与乙二醇发生缩聚反应生成聚对苯二甲酸乙二醇酯, 的系统命名为1,3-二甲苯,步骤Ⅲ的反应方程式为
的系统命名为1,3-二甲苯,步骤Ⅲ的反应方程式为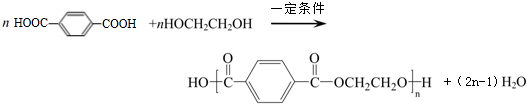 ,
, ;
; +ClCH2CH2CH2CH2Cl
+ClCH2CH2CH2CH2Cl| AlCl3 |
 +2HCl,
+2HCl,

科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、硫酸铝溶液中滴加过量浓氨水:Al3++4NH3?H2O=AlO2-+4NH4++2H2O |
| B、乙酸钠溶液显碱性原因:CH3COO-+H2O=CH3COOH+OH- |
| C、氢氧化钠溶液吸收少量SO2气体:SO2+2OH-=SO32-+H2O |
| D、漂白粉放置在空气中变质:ClO-+CO2+H2O=HClO+HCO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:
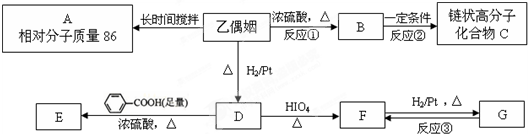
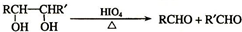
查看答案和解析>>
科目:高中化学 来源: 题型:
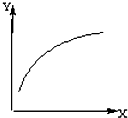 在密闭容器中加入A、B两种物质,在一定条件下反应:2A(s)+B(g)?2C(g) (△H<0).达到平衡后,改变一个条件(X),下列量(Y)的变化一定符合图中曲线的是( )
在密闭容器中加入A、B两种物质,在一定条件下反应:2A(s)+B(g)?2C(g) (△H<0).达到平衡后,改变一个条件(X),下列量(Y)的变化一定符合图中曲线的是( )| X | Y | |
| A | 再加入A | B的转化率 |
| B | 再加入B | C的体积分数 |
| C | 再加入C | B的体积分数 |
| D | 升高温度 | 混合气体密度 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、溶液Y中加入过量的NaOH溶液后过滤,滤液和沉淀中各含两种金属元素 |
| B、该矿石成分中能溶于盐酸的都是碱性氧化物,不溶的是酸性氧化物 |
| C、溶液Y中的阳离子主要是Mg2+、Al3+、Fe3+、H+ |
| D、沉淀X的成分是SiO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、硅酸钠是钠盐,也是硅酸盐 |
| B、碳酸钠使无色酚酞试液变红,属于碱 |
| C、CO2溶于水能导电,属电解质 |
| D、CO还原氧化铁获得铁,属于置换反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com