
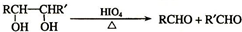
| HIO4 |
| △ |
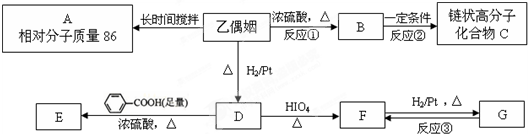
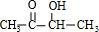 ,A的结构为
,A的结构为 ,乙偶姻在浓硫酸、加热条件下发生消去反应生成B,B为
,乙偶姻在浓硫酸、加热条件下发生消去反应生成B,B为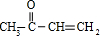 ,C是链状高分子化合物,B发生加聚反应生成C,C为
,C是链状高分子化合物,B发生加聚反应生成C,C为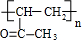 ,F与氢气发生加成反应生成G,G为CH3CH2OH,D与足量的苯甲酸发生酯化反应生成E,E为
,F与氢气发生加成反应生成G,G为CH3CH2OH,D与足量的苯甲酸发生酯化反应生成E,E为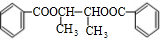 ,据此解答.
,据此解答.| HIO4 |
| △ |
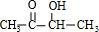 ,A的结构为
,A的结构为 ,乙偶姻在浓硫酸、加热条件下发生消去反应生成B,B为
,乙偶姻在浓硫酸、加热条件下发生消去反应生成B,B为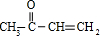 ,C是链状高分子化合物,B发生加聚反应生成C,C为
,C是链状高分子化合物,B发生加聚反应生成C,C为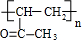 ,F与氢气发生加成反应生成G,G为CH3CH2OH,D与足量的苯甲酸发生酯化反应生成E,E为
,F与氢气发生加成反应生成G,G为CH3CH2OH,D与足量的苯甲酸发生酯化反应生成E,E为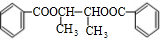 .
.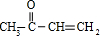 ,反应③是CH3CH2OH发生氧化反应生成CH3CHO,
,反应③是CH3CH2OH发生氧化反应生成CH3CHO, ,乙偶姻为
,乙偶姻为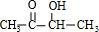 、C为
、C为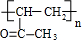 ;故答案为:
;故答案为: ;
;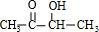 ;
;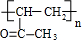 ;
;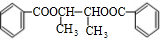 ,反应方程式为CH3CH(OH)CH(OH)CH3+2
,反应方程式为CH3CH(OH)CH(OH)CH3+2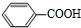
| 浓硫酸 |
| △ |
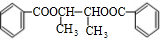 +2H2O,
+2H2O,
| 浓硫酸 |
| △ |
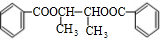 +2H2O;
+2H2O;


 小学课时特训系列答案
小学课时特训系列答案科目:高中化学 来源: 题型:
 含氯消毒剂和过氧化物等强氧化性消毒剂可防甲型H1N1流感.
含氯消毒剂和过氧化物等强氧化性消毒剂可防甲型H1N1流感.查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1mol乙烷分子中含有8NA个共价键 |
| B、0.05mol熔融的KHSO4中含有阳离子的数目为0.05 NA |
| C、标准状况下,22.4L甲醇的分子数为NA |
| D、1mol/L的氯化铵溶液含氮原子数为 NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
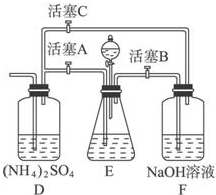 摩尔盐[(NH4)2SO4?FeSO4?6H2O]在空气中比一般亚铁盐稳定,是分析化学中常见的还原剂.某研究性学习小组设计了下面的实验装置来制备摩尔盐.
摩尔盐[(NH4)2SO4?FeSO4?6H2O]在空气中比一般亚铁盐稳定,是分析化学中常见的还原剂.某研究性学习小组设计了下面的实验装置来制备摩尔盐.查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
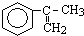 出发来合成A,其合成路线如下:
出发来合成A,其合成路线如下: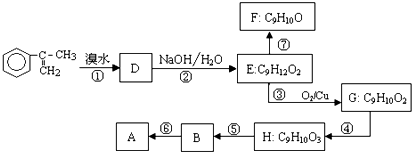
查看答案和解析>>
科目:高中化学 来源: 题型:
| Br2 |
| Cu/O2 |
| △ |

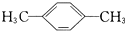 的系统命名为
的系统命名为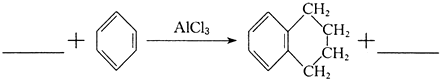
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
 某同学设计实验探究构成原电池的条件,装置如下:
某同学设计实验探究构成原电池的条件,装置如下:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com