
��CH4����ԭNOx�������������������Ⱦ��
���磺CH4(g)��4NO2(g)=4NO(g)��CO2(g)��2H2O(g)�� ��H1����574 kJ��mol��1
CH4(g)��4NO(g)=2N2(g)��CO2(g)��2H2O(g) ��H2����1 160 kJ��mol��1
���ڱ�״������CH4��ԭ4.48 L NO2����N2��������˵������ȷ����
(����)��
A���ù������յ�����Ϊ86.7 kJ
B���˹�������Ҫ��״����CH4����1.12 L
C��ת�Ƶĵ�����Ϊ0.8NA
D����֪2NO(g)��O2(g)=2NO2(g)����H����114 kJ��mol��1����CH4��ȼ������802 kJ��mol��1

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2014�꽭��ʡ��ͨ��ҵˮƽ���ԣ����ޣ���ѧ�Ծ��������棩 ���ͣ�ѡ����
����ǿ������Һ�д��������һ��������
A��K+��Cu2+��SO42-��NO3- B��Na+��Ba2+��Br����SO42-
C��NH4+��Fe3+��Cl����SCN�� D��K+��Fe2+��Cl����NO3-
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014�껯ѧ�߿�����ר��ʮ�� ������������ʼ����ۺ�Ӧ����ϰ���������棩 ���ͣ�ѡ����
����˵����ȷ���� (����)��
A��ʵ���ҿ��ü��ȷֽ�̼��Ƶķ�����ȡ������̼����
B����������������ˮ�����Ṥ����β������ֱ����ˮ����
C��������������ˮ��Ӧ�������գ������Ṥҵ��β��Ӧ����ˮ����
D�����ƽϸ�Ũ�ȵĵ�ˮʱ��Ӧ�Ƚ������ھƾ��У��ټ�ˮϡ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014�껯ѧ�߿�����ר��ʮһ Ԫ�صĵ��ʼ��仯�����������ת����ϰ���������棩 ���ͣ�ѡ����
X��Y��Z���ֲ�ͬ��������ͼ��ʾ��ת����ϵ����X�������� (����)��

A��Al2O3 B��SiO2 C��CO2 D��NH4Cl
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014�껯ѧ�߿�����ר��ʮ �������Һ����Ũ�ȵĹ�ϵ��ϰ���������棩 ���ͣ�ѡ����
���������У�����ȷ���� (����)��
A��c(NH4+)��ȵ�(NH4)2SO4��NH4Cl��Һ�У�����Ũ�ȴ�С��ϵ��c[(NH4)2SO4]<c(NH4Cl)
B����10 mL 0.10 mol��L��1��CH3COOH��Һ�м�������ʵ�����NaOH����Һ�У�c(Na��)��c(CH3COO��)>c(OH��)��c(H��)
C�����ֲ�ͬŨ�ȵ�HA��Һ�����ʵ���Ũ�ȷֱ�Ϊc1��c2��pH�ֱ�Ϊa��(a��1)������c1��10c2
D��NaHCO3��Һ�У�c(H��)��c(H2CO3)��c(CO32��)��c(OH��)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014�껯ѧ�߿�����ר���� ��˹����Ӧ�����Ȼ�ѧ����ʽ����д��ϰ���������棩 ���ͣ�ѡ����
��֪һ�������¶���1 mol���л�ѧ��������̬ԭ����Ҫ���յ��������£�H��H��436 kJ��Cl��Cl��243 kJ��H��Cl��431 kJ�����������Ȼ�ѧ����ʽ�������ȷ���� (����)��
A��2HCl(g)=H2(g)��Cl2(g)�ķ�Ӧ����H<0
B��H(g)��Cl(g)=HCl(g)����H����431 kJ��mol��1
C����ͬ�����£�H2(g)��Cl2(g)=2HCl(g)�ڹ��պ͵�ȼ�����µ���H���
D��H2(g)��Cl2(g)=2HCl(g)����H����183 kJ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014�껯ѧ�߿�����ר���� ��ѧ��Ӧ���ʺͻ�ѧƽ��������ж���ϰ���������棩 ���ͣ�ѡ����
һ���¶��£���2 L�ܱ������м�������Cu2O��ͨ��0.1 mol H2O(g)��������Ӧ��2H2O(g)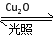 2H2(g)��O2(g)����H����484 kJ��mol��1����ͬʱ�����O2�����ʵ������±���
2H2(g)��O2(g)����H����484 kJ��mol��1����ͬʱ�����O2�����ʵ������±���
ʱ��/min | 20 | 40 | 60 | 80 |
n(O2)/mol | 0.001 0 | 0.001 6 | 0.002 0 | 0.002 0 |
����˵������ȷ���� (����)��
A��ǰ20 min�ڵ�ƽ����Ӧ����v(H2O)��5.0��10��5 mol��L��1��min��1
B���ﵽƽ��ʱ��������Ҫ�������������0.968 kJ
C������c(H2O)���������ˮ�ķֽ���
D����Ч����Cu2O�����Ĵ�С�й�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014�껯ѧ�߿�����ר���� ��ѧ���ü�����������ۺ�Ӧ����ϰ���������棩 ���ͣ�ѡ����
��NA���������ӵ�������ֵ������˵����ȷ����(����)��
A��1 mol��(��CH3)�к��еĵ�����Ϊ7NA
B��25 ��ʱ��pH��7��NH4Cl��NH3��H2O�Ļ����Һ�У�OH����Ϊ10��7NA
C��42 g��ϩ�к��еĹ��ۼ���ĿΪ9NA
D�����ݾ�Ϊ2.7 g������Ʒ�ֱ���100 mLŨ�Ⱦ�Ϊ2 mol��L��1���������
��������Һ��ַ�Ӧ��ת�Ƶĵ�������Ϊ0.3NA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014�껯ѧ�߿���ʱ���� 7-3��ѧƽ�ⳣ����ѧ��Ӧ���з�����ϰ���������棩 ���ͣ������
�״���ͨ����ú�������������ɵ�CO��H2��һ�������£��������·�Ӧ�Ƶ�:CO(g)��2H2(g) CH3OH(g)�������ͼʾ�ش��������⣺
CH3OH(g)�������ͼʾ�ش��������⣺

(1)�ӷ�Ӧ��ʼ��ƽ�⣬��H2Ũ�ȱ仯��ʾƽ����Ӧ����v(H2)= ��CO��ת����Ϊ ��
(2)�÷�Ӧ��ƽ�ⳣ������ʽΪ ���¶����ߣ�ƽ�ⳣ�� (���������С�����䡱)��
(3)����һ����ɱ���ܱ������г���1 mol CO��2 mol H2��1 mol CH3OH���ﵽƽ��ʱ��û��������ܶ���ͬ��ͬѹ����ʼ��1.6�������������ʺ�÷�Ӧ�� (����������桱)��Ӧ�����ƶ��������� ��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com