
【题目】我国科研人员提出了由CO2和CH4转化为高附加值产品CH3COOH的催化反应历程。该历程示意图如下。
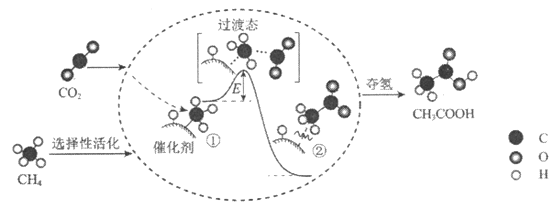
下列说法不正确的是
A. 该反应是化合反应
B. 催化剂参加了化学反应过程
C. CH4→CH3COOH过程中,有C—H键的断裂和形成
D. ①→②过程中,形成了C—C键,断裂的化学键的总键能<形成的化学键的总键能
科目:高中化学 来源: 题型:
【题目】现取m克铝镁合金与一定浓度的稀硝酸恰好完全溶解(假定硝酸的还原产物只有NO),向反应后的混合溶液中滴加bmol/LNaOH溶液,当滴加到VmL时,得到沉淀质量恰好为最大值n克,则下列有关该实验的说法中不正确的是 ( )
A. 沉淀中氢氧根的质量为(n-m)克
B. 恰好溶解后溶液中的NO3-离子的物质的量为![]() mol
mol
C. 生成标准状况下NO气体的体积为![]() L
L
D. 与合金反应反应的硝酸的物质的量为(![]() +
+![]() )mol
)mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氨基甲酸铵(H2NCOONH4)是一种易分解、易水解的白色固体,可用于化肥、灭火剂、洗涤剂等。某研究小组用下图所示的实验装置,利用氢氧化钠固体、浓氨水、干冰等作原料制备氨基甲酸铵。主要反应原理:2NH3(g) + CO2(g)=H2NCOONH4(s) ΔH<0。
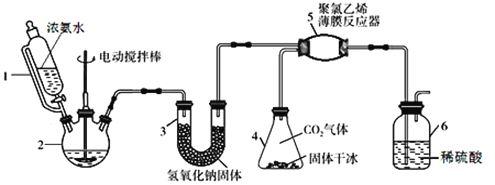
(1)实验室用98%的浓硫酸配制15%的稀硫酸,除量筒外还需使用下列仪器中的____。
a.烧杯 b.一定容积的容量瓶 c.玻璃棒 d.滴定管
(2)仪器1恒压分液漏斗,其优点是__________________________。
(3)仪器3中NaOH固体的作用是__________________________。
(4)仪器6的一个作用是控制原料气按反应计量系数充分反应,若反应初期观察到装置内稀硫酸溶液中产生气泡,应该______(填“加快”、“减慢”或“不改变”)产生氨气的流速。
(5)另有一种制备氨基甲酸铵的反应器(CCl4与液体石蜡均为惰性介质)如图。生成的氨基甲酸铵小晶体悬浮在四氯化碳中,当悬浮物较多时,停止制备。
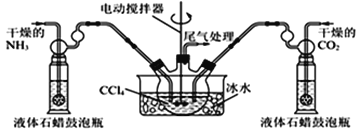
①发生器用冰水冷却的原因是________________________________________;
②从反应后混合物中过滤分离出产品。为了得到干燥产品,应采取的方法是_____(填序号)
a.常压加热烘干 b.高压加热烘干 c.真空40℃以下烘干
(6)已知氨基甲酸铵可完全水解,其中产物有碳酸氢铵。氨基甲酸铵水解反应的化学方程式为________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为除去某物质中所含的杂质,周佳敏同学做了以下四组实验,其中她所选用的试剂或操作方法正确的是( )
序号 | 物质 | 杂质 | 除杂试剂或操作方法 |
① | NaCl溶液 | Na2CO3 | 加入盐酸,蒸发 |
② | FeSO4溶液 | CuSO4 | 加入过量铁粉并过滤 |
③ | H2 | CO2 | 依次通过盛有NaOH溶液和浓硫酸的洗气瓶 |
④ | NaNO3 | CaCO3 | 加稀盐酸溶解、过滤、蒸发、结晶 |
A.①②③B.②③④C.①③④D.①②③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:转化率=某一反应物转化的量÷该反应物的初始量×100%。在一密闭容器中加入A、B、C三种气体,保持温度一定,在t1~t4时刻测得各物质的浓度如下表。据此判断下列结论不正确的是
测定时刻/s | t1 | t2 | t3 | t4 |
c(A)/(mol·L-1) | 6 | 3 | 2 | 2 |
c(B)/(mol·L-1) | 5 | 3.5 | 3 | 3 |
c(C)/(mol·L-1) | 1 | 2.5 | 3 | 3 |
A. 在t4时刻,该反应处于化学平衡状态
B. t3时,A的转化率比B的转化率高
C. t1至t2时刻,该反应的速率为3 mol·L-1 s-1
D. 该反应的化学方程式是:2A(g)+B(g)![]() C(g)
C(g)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】超音速飞机在平流层飞行时,尾气中的NO会破坏臭氧层。科学家正在研究利用催化技术将尾气中的NO和CO转变成CO2和N2,化学方程式如下:2NO+2CO ![]() 2CO2+N2,为了测定在某种催化剂作用下的反应速率,在某温度下用气体传感器测得不同时间的NO和CO浓度如表:
2CO2+N2,为了测定在某种催化剂作用下的反应速率,在某温度下用气体传感器测得不同时间的NO和CO浓度如表:
时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
c(NO)/ mol·L-1 | 1.00×10-3 | 4.50×10-4 | 2.50×10-4 | 1.50×10-4 | 1.00×10-4 | 1.00×10-4 |
c(CO)/ mol·L-1 | 3.60×10-3 | 3.05×10-3 | 2.85×10-3 | 2.75×10-3 | 2.70×10-3 | 2.70×10-3 |
请回答下列问题(均不考虑温度变化对催化剂催化效率的影响):
(1)在上述条件下反应能够自发进行,则反应的△H________0(填写“>”、“<”、“=”)。
(2)前2s内的平均反应速率v(N2)=_____________________。
(3)假设在密闭容器中发生上述反应,投入相等的反应物,反应刚开始时下列措施能提高NO反应速率的是_______。
A.选用更有效的催化剂 B.升高反应体系的温度
C.降低反应体系的温度 D.缩小容器的体积
(4)研究表明:在使用等质量催化剂时,催化剂比表面积会影响化学反应速率。为了分别验证温度、催化剂比表面积对化学反应速率的影响规律,某同学设计了三组实验,部分实验条件已经填在下面实验设计表中,请在下表中填入剩余的实验条件数据。
实验 编号 | T/℃ | NO初始浓度 mol·L-1 | CO初始浓度 mol·L-1 | 催化剂的比表面积 m2·g-1 | 达到平衡的时间 分钟 |
Ⅰ | 280 | l.20×10-3 | 5.80×10-3 | 82 | 200 |
Ⅱ | l.20×10-3 | 124 | 120 | ||
Ⅲ | 350 | 5.80×10-3 | 124 | 5 |
通过这3组实验,可以得出的温度、催化剂比表面积对化学反应速率的影响规律是___________________________________________________________.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】元素X、Y、Z、M、W在周期表中的位置如图:
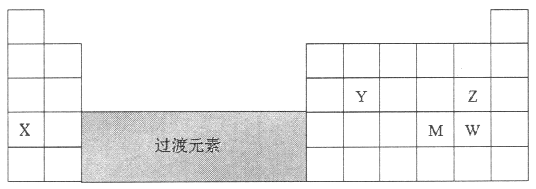
(1)X的元素符号是_________。
(2)YO2是玻璃的成分之一,是酸性氧化物。实验室盛装NaOH溶液的试剂瓶不能用玻璃塞的原因是:_________+_________OH-=_________+_________。
(3)元素Z和元素W中,非金属性比较弱的是_________(填元素符号)。在Z和W形成的原子个数比为1:1的化合物中,W的化合价是_________。
(4)元素M(Se)是人体必需的微量元素。Se能与H2反应生成H2Se,用原子结构解释原因_________。298K、1.01×105pa时,O2、S、Se、Te分别与H2化合生成1 mol气态氢化物时的热量的变化数据(Q)如下图所示。图中表示Se与H2化合的点是_________(填字母)。
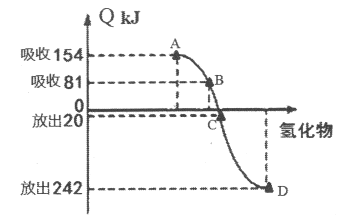
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】医药合成中可用下列流程合成一种治疗心脏病的特效药物(G)。

已知:①RCH=CH2![]() RCH2CH2CHO;
RCH2CH2CHO;
②
(1)B的核磁共振氢谱图中有_______组吸收峰,C的名称为_________。
(2)E中含氧官能团的名称为_______,写出D→E的化学方程式_______ 。
(3)E-F的反应类型为________ 。
(4)E的同分异构体中,结构中有醚键且苯环上只有一个取代基结构有_____种,写出其中甲基数目最多的同分异构体的结构简式_______ 。
(5)下列有关产物G的说法正确的是__________
A.G的分子式为C15H28O2 B.1molG水解能消耗2molNaOH
C.G中至少有8个C原子共平面 D.合成路线中生成G的反应为取代反应
(6)写出以1-丁醇为原料制备C的同分异构体正戊酸(CH3CH2CH2CH2COOH)。合成路线流程图示例如下:H2C=CH2![]() CH3CH2Br
CH3CH2Br![]() CH3CH2OH,无机试剂任选。___________
CH3CH2OH,无机试剂任选。___________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组变化中,前者小于后者的是( )
①CH4(g)+2O2(g)===CO2(g)+2H2O(l) ΔH1
CH4(g)+2O2(g)===CO2(g)+2H2O(g) ΔH2
②2H2(g)+O2(g)═2H2O(l) ΔH1
H2(g)+![]() O2(g)===H2O(l) ΔH2
O2(g)===H2O(l) ΔH2
③t ℃时,在一定条件下,将1 mol SO2和1 mol O2分别置于恒容和恒压的两个密闭容器中,达到平衡状态时分别反应放出的热量
④CaCO3(s)===CaO(s)+CO2(g) ΔH1
CaO(s)+H2O(l)===Ca(OH)2(s) ΔH2
A. ①②③ B. ②④ C. ②③④ D. ③④
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com