
【题目】某同学组装了如图所示的电化学装置,则下列说法正确的是( )
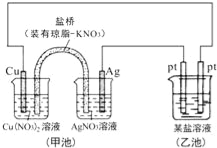
A.图中甲池为原电池装置,Cu电极发生还原反应
B.实验过程中,甲池左侧烧杯中NO3﹣的浓度不变
C.若甲池中Ag电极质量增加5.4g时,乙池某电极析出1.6g金属,则乙中的某盐溶液可能是AgNO3溶液
D.若用铜制U形物代替“盐桥”,工作一段时间后取出U形物称量,质量会减小
科目:高中化学 来源: 题型:
【题目】(12分)电炉加热时用纯O2氧化管内样品,根据产物的质量确定有机物的组成.下列装置是用燃烧法确定有机物分子式常用的装置.

(1)产生的O2按从左到右的流向,所选装置各导管的正确连接顺序是
(2)C装置中浓硫酸的作用是 .
(3)D装置中MnO2的作用是 .
(4)燃烧管中CuO的作用是 .
(5)若实验中所取样品只含C、H、O三种元素中的两种或三种,准确称取0.92g样品,经充分反应后,A管质量增加1.76g,B管质量增加1.08g,则该样品的实验式为 .
(6)用质谱仪测定其相对分子质量,得如图二所示的质谱图,则该有机物的相对分子质量为 .
(7)能否根据A的实验式确定A的分子式 (填“能”或“不能”),若能,则A的分子式是 (若不能,则此空不填).
(8)该物质的核磁共振氢谱如图三所示,则其结构简式为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有部分短周期元素的性质或原子结构如下表:
元素编号 | 元素性质或原子结构 |
T | 最外层电子占核外电子总数的3/8 |
X | 最外层电子数是次外层电子数的2倍 |
Y | 常温下单质为双原子分子,其氢化物水溶液呈碱性 |
Z | 元素最高正价是+7价 |
(1)元素X的一种同位素可测定文物年代,该同位素中子数为8,这种同位素的符号是 .
(2)Y的氢化物与Y的最高价氧化物的水化物反应生成的物质名称为:
(3)Z所在族元素的四种氢化物中,沸点最低的物质的化学式为:
(4)探寻物质的性质差异性是学习的重要方法之一.T、X、Y、Z四种元素的最高价氧化物的水化物中化学性质明显不同于其他三种酸的是 (填分子式),阐述理由是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】组成为C3H5O2C1的有机物甲,在NaOH溶液中加热后经酸化可得组成为C3H6O3的有机物乙,在一定条件下,每2分子有机物乙能发生酯化反应生成1分子酯丙,丙的结构式不可能的是
A.![]()
B.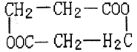
C.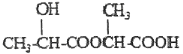
D.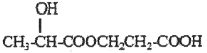
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下面列出了几组物质,请将物质的合适组号填写在空格上.
①金刚石与C60;②O2与O3;③16O、17O和18O;
④CH4和CH3CH2CH3;⑤乙烯和乙烷;⑥葡糖糖和果糖
⑦![]() 和
和![]() ;⑧
;⑧![]() 和
和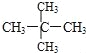 ;
;
(1)互为同位素的是 ;
(2)互为同素异形体的是 ;
(3)互为同系物的是 ;
(4)互为同分异构体的是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室中用二氧化锰和浓盐酸反应制备氯气.进行此实验,所用仪器如图:
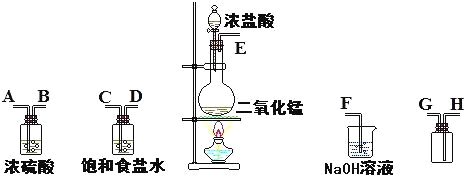
(1)连接上述仪器的正确顺序(填各接口处的字母):接 ;接 ;接 ;接 .
(2)在制备氯气的发生装置中,用到的玻璃仪器除酒精灯外,还有 .
(3)写出用如图装置制备氯气的离子方程式 :
(4)A、B两组同学分别用两种方法制取氯气:A组用含146g HCl的浓盐酸与足量的二氧化锰反应;B组用87g二氧化锰与足量的浓盐酸反应,则所得氯气的物质的量的关系为A B(填“>”、“<”或“=”)
(5)实验中饱和食盐水的作用是 :
(6)写出氯气尾气吸收的化学方程式: .
(7)如何验证氯气已经收集满?
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业废水中含有流失的生产用料、中间产物和产品,以及生产过程中产生的污染物。随着工业的迅速发展,废水的排放量迅速增加,严重威胁人类的健康和安全,工业废水的处理比城市污水的处理更为重要。下图是含铬工业废水和含氰废水的处理流程:
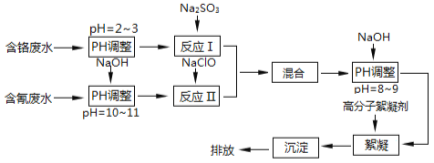
请回答下列问题:
(1)电镀废水中的铬主要以CrO42—形式存在,其中Cr元素的化合价为 。
(2)酸性条件下,CrO42—极易被还原剂还原为毒性较小的Cr3+。图中“反应Ⅰ”的离子方程式为 。
(3)pH>10时,“反应Ⅱ”中的NaClO可快速地将氰离子(CN—)氧化为无毒的两种物质,这两种物质是 、 (写化学式);若pH<8.5,则生成剧毒的CNCl气体(沸点13.1℃),写出该反应的离子方程式 。
(4)经过“反应Ⅰ”和“反应Ⅱ”将两种废水混合的目的是 。
(5)含氰废水及含铬废水可以通过电化学的方法进行无害化处理。
①可采用惰性电极对含氰废水进行电解,氰离子在碱性条件下被氧化为无毒的物质,该电解工艺中,阳极电极反应式是 。
②电解法处理酸性含铬废水(若铬元素以Cr2O72—形式存在)时,以铁板和石墨作电极,处理过程中存在反应Cr2O72—+6Fe2++14H+=2Cr3++6Fe3++7H2O。则阳极的电极反应式为 ,当有1 mol Cr2O72—被还原时,电路中转移的电子为 mol。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】骨架型镍催化剂因其具有多孔结构对氢气有极强吸附性,故常用作加氢反应的催化剂。一种镍铜硫化矿(主要成分为Ni2S和Cu2S)为原料制备骨架型镍的工艺流程如下:
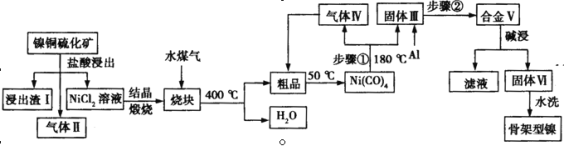
⑴镍铜硫化矿酸浸所得的浸出渣Ⅰ的主要成分是Cu2S,气体Ⅱ中主要含有两种成分,则该步反应的化学方程式为 ;
⑵写出步骤①的化学方程式 。合金Ⅴ在碱浸前要粉碎,粉碎的目的是 ;
⑶碱浸时选择浓NaOH溶液,反应的离子方程式是: ;
⑷碱浸后残铝量对骨架型镍的催化活性有重大影响。分析如图,残铝量在 范围内催化剂活性最高,属于优质产品;
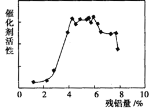
⑸使用新制骨架型镍进行烯烃加氢反应,有时不加入氢气也可以完成反应,原因是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com