
足量的两份铝粉分别与等体积的盐酸和NaOH 溶液反应,同温同压下产生的气体体积比为1:1,则盐酸和NaOH溶液的物质的量浓度之比为
A.2:3 B.3:1 C.1:2 D.1:1
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
用6.02×1023表示阿伏加德罗常数的值,下列说法中正确的是 ( )
A.常温常压下,1.6 g臭氧中含有6.02×1022个氧原子
B.标准状况下,2.24 L水中含有6.02×1022个水分子
C.2.24 L氨气分子中含6.02×1023个电子
D.2.4 g金属镁变为镁离子时失去6.02×1022个电子
查看答案和解析>>
科目:高中化学 来源: 题型:
绿色化学的核心是反应过程的绿色化,即要求原料物质中的所有原子完全被利用且全部转入期望的产品中,下列过程不符合这一思想的的是
A.甲烷与氯气反应制氯仿:CH4+3Cl2 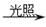 CHCl3+3HCl
CHCl3+3HCl
B.烯烃与水煤气发生的羰基合成反应:
RCH=CH2+CO+H2  RCH2CH2CHO
RCH2CH2CHO
C.甲烷、CO合成乙酸乙酯:2CH4+2CO  CH3COOCH2CH3
CH3COOCH2CH3
D.乙烯合成聚乙烯


查看答案和解析>>
科目:高中化学 来源: 题型:
(1)热电厂发电时的能量转化途径通常是“化学能→热能→机械能→电能”, 而燃料电池
的能量转化途径为“ ▲ 能→ ▲ 能”, 因此燃料电池的能量转化效率高。
(2)某同学在做电解水实验后,观察到绕成螺旋状的两铂丝电极上附有大量气泡,于是他将两极接到电表上,发现“电表显示电压超过2V,且电压逐渐下降”。
对这个现象的合理解释是 ▲ 。
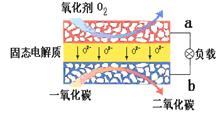 (3)右图为固态氧化物燃料电池(SOFC)的原理示意图。试写出电极反应式:正极 ▲ ,负极 ▲ ;在导线中电子流动方向为a ▲ b(用“→”或“←”表示)。该电池可选用的固态电解质为 ▲ (填字母)
(3)右图为固态氧化物燃料电池(SOFC)的原理示意图。试写出电极反应式:正极 ▲ ,负极 ▲ ;在导线中电子流动方向为a ▲ b(用“→”或“←”表示)。该电池可选用的固态电解质为 ▲ (填字母)
A.ZrO(氧化锆) B.NaOH C.Na2SO4
此电池的工作温度一般应为 ▲ (填字母)。A.常温 B.约100℃ C.约1000℃
(4)在电池反应中,每消耗0.5mol氧气,理论上能生成标准状况下CO2气体 ▲ L。
查看答案和解析>>
科目:高中化学 来源: 题型:
在无色强酸性溶液中,下列各组离子一定能大量共存的是
A.Na+、K+、Cl-、SO42- B.Cu2+、K+、SO42-、NO3-
C.K+ 、NH4+、SO42-、CO32- D.Ba2+、Na+、Cl-、SO42-
查看答案和解析>>
科目:高中化学 来源: 题型:
向一定量的Cu、Fe2O3的混合物中加入100 mL 1 mol·L-1的盐酸,恰好使混合物完全溶解,所得溶液中不含Fe3+,若用过量的CO在高温下还原相同质量的原混合物,固体减少的质量为
A.3.2 g B.2.4 g C.1.6 g D.0.8 g
查看答案和解析>>
科目:高中化学 来源: 题型:
将4 g NaOH溶于水配成50 mL溶液,取出5 mL,这5 mL溶液的物质的量浓度是 ( )
A.2 mol/L B.1 mol/L
C.0.1 mol/L D.0.05 mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
镁是生产铝合金必需的添加材料。镁合金被公认为“21世纪绿色环保新型材料”,可广泛运用于航空航天、汽车等10多个领域。现把镁条投入到盛有盐酸的敞口容器中,产生H2的速率如图所示。在下列因素中对产生H2速率没有影响的是
A.溶液的温度 B.镁条的表面积
C.Cl-的浓度 D. H+的浓度
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com