
【题目】下列各组材料中,不能组成原电池的是( )
A | B | C | D | |
两极材料 | 锌片、石墨 | 锌片、铜片 | 铜片、石墨 | 铁片、铜片 |
插入溶液 | 硫酸溶液 | 无水乙醇 | 硝酸银溶液 | 稀盐酸 |
A.AB.BC.CD.D
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】图是一些常见单质、化合物之间的转化关系图,有些反应中的部分物质被略去.常温常压下,A为无色有毒气体,B为红棕色粉末,C、E为金属单质,G、J的焰色均为黄色.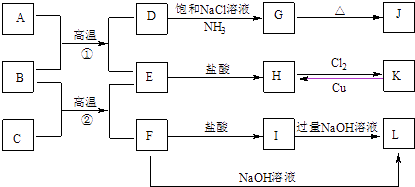
请回答下列问题:
(1)G的化学式为 , D的电子式为 .
(2)F→L反应的化学方程式为 .
(3)K→H是制作印刷电路板的重要反应,该反应的离子方程式为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】通常状况下,CO是一种无色、无味、有毒的气体,难溶于水,与酸、碱、盐溶液均不反应。已知乙二酸晶体加热分解的方程式为:H2C2O4·2H2O![]() 3H2O+CO2↑+CO↑,不考虑其他因素干扰,如何利用下列装置验证反应产物中含有CO2和CO(装置不能重复使用)。酒精喷灯可作高温热源。请回答下列问题:
3H2O+CO2↑+CO↑,不考虑其他因素干扰,如何利用下列装置验证反应产物中含有CO2和CO(装置不能重复使用)。酒精喷灯可作高温热源。请回答下列问题:
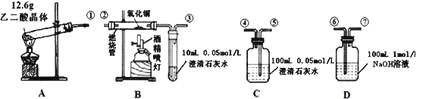
(1)检验装置A气密性的方法是
(2)按气流方向连接各仪器,用数字表示接口的连接顺序:
①→
(3)证明CO存在的实验现象是
(4)本实验尾气处理的方法是
(5)根据题给的数据,假设各反应均充分发生且产生的气体全部排出,并与吸收液充分反应(提示:B、C中澄清石灰水均先变浑浊,后又变澄清),D中溶质及对应的物质的量是: 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中正确的是( )
A.32 g O2占有的体积约为22.4 L
B.22.4 L N2含阿伏加德罗常数个氮分子
C.在标准状况下,22.4 L水的质量约为18 g
D.22 g二氧化碳与标准状况下11.2 L HCl约含有相同的分子数
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应中属于氧化还原反应,但水既不做氧化剂,又不做还原剂的是( )
A.Cl2+H2O=HCl+HClO
B.2K+2H2O=2KOH+H2↑
C.2F2+2H2O=4HF+O2
D.Na2O+H2O=2NaOH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,氢氧化钙固体在水溶液中达到溶解平衡:Ca(OH)2 (s) ![]() Ca2++2OH-,向其中加入以下物质,恢复到室温,Ca(OH)2固体减少的是( )
Ca2++2OH-,向其中加入以下物质,恢复到室温,Ca(OH)2固体减少的是( )
A. CH3COONa B. AlCl3 C. NaOH D. CaCl2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.A、B、C、D是中学化学常见的混合物分离或提纯的基本装置。
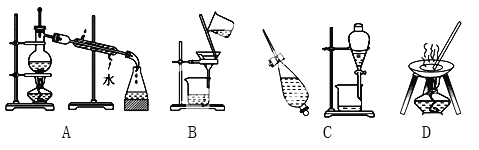
请根据混合物分离或提纯的原理,回答在下列实验中需要使用哪一种装置,将A、B、C、D填入适当的空格中。
(1)从碘水中提取碘_____________________________;
(2)实验室制取蒸馏水_____________________________;
(3)去粗盐中的泥沙_____________________________;
(4)与海水晒盐原理相符的是___________________________。
Ⅱ.现有下列八种物质:①HCl气体②Cu ③CO ④CO2 ⑤金刚石 ⑥KMnO4固体 ⑦Ba(OH)2溶液 ⑧熔融KAl(SO4)2
(1)属于单质的是_________;属于酸性氧化物的是_________;所给状态能导电的电解质是_________;(填所给物质的序号)
(2)写出Ba(OH)2在水中的电离方程式:____________________________________________;
(3)用双线桥表示该反应中电子转移的方向和数目_______
2KMnO4+16HCl=5Cl2↑+2MnCl2+2KCl+8H2O
若有0.8mol还原剂被氧化,则转移电子的物质的量是_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CaC2晶体的晶胞结构与NaCl晶体的相似(如图所示),但CaC2晶体中含有的中哑铃形C ![]() 的存在,使晶胞沿一个方向拉长.下列关于CaC2晶体的说法中正确的是( )
的存在,使晶胞沿一个方向拉长.下列关于CaC2晶体的说法中正确的是( ) 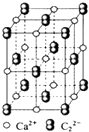
A.1个Ca2+周围距离最近且等距离的C22﹣数目为6
B.该晶体中的阴离子与F2是等电子体
C.6.4克CaC2晶体中含阴离子0.1mol
D.与每个Ca2+距离相等且最近的Ca2+共有12个
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】锰氧化物(CuMn2O4)能在常温下催化氧化空气中的一氧化碳和甲醛(HCHO).
(1)锰元素位于第四周期第ⅦB族.基态Mn2+的核外电子排布式为 . NO3﹣的空间构型为 .
(2)HCHO中含有的σ键和π键数目之比为 .
(3)火山喷出的岩浆中含有多种硫化物,冷却时ZnS比HgS先析出,原因是
(4)Cu3N形成的晶体结构如图所示.则与同一个N3﹣相连的Cu+有个,Cu+的半径为a pm,N3﹣的半径为b pm,则Cu3N的密度为gcm﹣3 . (只列式,不用计算出结果)(阿伏加德罗常数用NA表示,1pm=10﹣10 cm) 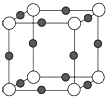
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com