
【题目】下列反应中属于氧化还原反应,但水既不做氧化剂,又不做还原剂的是( )
A.Cl2+H2O=HCl+HClO
B.2K+2H2O=2KOH+H2↑
C.2F2+2H2O=4HF+O2
D.Na2O+H2O=2NaOH
 考前必练系列答案
考前必练系列答案科目:高中化学 来源: 题型:
【题目】如图所示是学生课外活动小组设计的制取氨气并进行氨气溶于水的喷泉实验等试验的装置示意图
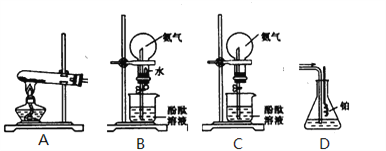
请回答下列问题:
(1)学生甲用图A所示装置制备氨气,写出该法制取氨气的化学方程式_________________________;制出的氨气应使用________法来收集,要得到干燥的氨气可选用___________作干燥剂。
(2)学生乙用图B所示装置进行喷泉实验,上部烧瓶已充满干燥氨气,引发水上喷的操作是________。
(3)学生丙将装置B误装为装置C,但经同学讨论后,认为也可引发喷泉。请说明用该装置引发喷泉的方法____________________。
(4)学生丁用装置D吸收一段时间氨气后,再通入空气,同时将经加热的铂丝插入装置D的锥形瓶内,看到了具有催化作用的铂丝(催化剂)保持红热,同时瓶内生成了红棕色的气体。写出在此过程中可能发生反应的化学方程式________________________,____________________________.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图为实验室某浓盐酸试剂瓶标签上的有关数据,试根据标签上的有关数据回答下列问题:
盐酸
分子式:HCl
相对分子质量:36.5
密度:1.19 g·cm-3
HCl的质量分数:36.5%
(1)该浓盐酸中HCl的物质的量浓度为_________mol·L -1 。
(2)取用任意体积的该盐酸溶液时,下列物理量中不随所取体积的多少而变化的是________。
A.溶液中HCl的物质的量 B.溶液的浓度
C.溶液中Cl- 的数目 D.溶液的密度
(3)某学生取上述浓盐酸100mL,
①若加水稀释到500 mL,所得盐酸的物质的量浓度为________mol·L -1 。
②若需使该溶液的质量分数变为原来的![]() ,应该加______mL蒸馏水。
,应该加______mL蒸馏水。
③若需使该溶液的物质的量浓度变为原来的![]() ,需加蒸馏水的体积______119mL(该空填“>”“<”或“=”)。
,需加蒸馏水的体积______119mL(该空填“>”“<”或“=”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组材料中,不能组成原电池的是( )
A | B | C | D | |
两极材料 | 锌片、石墨 | 锌片、铜片 | 铜片、石墨 | 铁片、铜片 |
插入溶液 | 硫酸溶液 | 无水乙醇 | 硝酸银溶液 | 稀盐酸 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知蛋白质含有C、H、O、N等元素。下列关于自然界中氮循环的说法错误的是
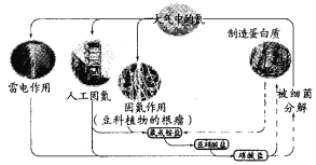
A. 含氮无机物和含氮有机物可相互转化
B. 碳、氢、氧三种元素也可能参与了氮循环
C. 铵盐转化为硝酸盐,发生了还原反应
D. 目前人工固氮的反应为N2+3H2![]() 2NH3
2NH3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】选择萃取剂将碘水中的碘萃取出来,这种萃取剂应具备的性质是( )
A. 不溶于水,且必须易与碘发生化学反应
B. 不溶于水,且必须比水密度大
C. 不溶于水,且必须比水密度小
D. 不溶于水,且比水更容易使碘溶解
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氢化铝锂(LiAlH4)是有机合成中的重要还原剂。某课题组设计实验制备氢化铝锂并测定其纯度。已知: 氢化铝锂、氢化锂遇水都剧烈反应并产生同一种气体。
I.制备氢化锂
选择图I中的装置制备氢化锂(有些装置可重复使用):
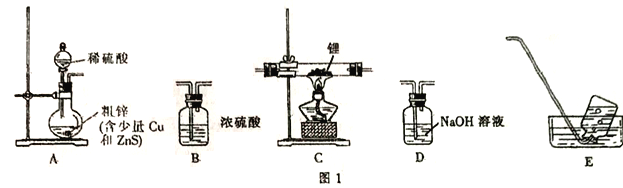
(1)装置的连接顺序(从左至右)为A→______________。
(2)检在好装蹬装置的气密性,点燃酒精灯前需进行的实验操作是_______________。
(3)写出制备氢化铝锂的化学方程式:__________________。
II. 制备氢化铝锂
1947年,Schlesinger,Bond和Finholt首次制得氢化铝锂,其方法是使氢化锂与无水三氯化铝按一定比例在乙醚中混合,搅样,充分反应后,经一系列操作得到LiAlH4晶体。
(4)写出氢化锂与无水三氯化铝反应的化学方程式:____________________。
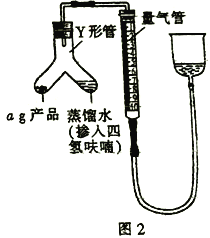
III.测定氢化铝锂产品(不含氢化锂)的纯度
(5)按图2装配仪器、检查装置气密性并装好药品(Y形管中的蒸馏水足量,为了避免氢化铝锂遇水发生爆炸,蒸馏水中需掺入四氢呋喃作稀释剂),启动反应的操作是________。读数之前上下移动量气管右侧的容器,使量气管左、右有两侧的液面在同一水平面上,其目的是_________。
(6)在标准状况下,反应前量气管读数为V1mL,反应完毕并冷却之后,量气管读数为V2mL。该样品的纯度为_____________(用含a、V1、V2的代数式表示)。如果起始读数时俯视刻度线,测得的结果将________(填“偏高”“偏低”或“无影响”)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com