
【题目】25 ℃时,在pH都等于9的NaOH和CH3COONa两种溶液中,设由水电离产生的OH- 离子 Amol·L-1与Bmol·L-1,则A和B关系为( )
A. A>B B. A=10-4 B C. B=10-4 A D. A=B
 53天天练系列答案
53天天练系列答案科目:高中化学 来源: 题型:
【题目】硫及其化合物对人类的生产和生活有着重要的作用。一种由含硫化合物参与的制氢示意图如下:

(1)①反应2的化学方程式为___________;该反应能量转化的主要方式为_________。
②反应4的热化学方程式为2H2SO4(l)![]() 2SO2(g)+O2(g)+2H2O(g) △H=+550kJ/mol
2SO2(g)+O2(g)+2H2O(g) △H=+550kJ/mol
已知:a. H2SO4(l)![]() SO3(g)+H2O(g) △H=X
SO3(g)+H2O(g) △H=X
b.2SO3(g)![]() 2SO2(g)+O2(g) △H=+196kJ/mol
2SO2(g)+O2(g) △H=+196kJ/mol
则X=____________。
(2)SO2是一种大气污染物,已知: 2SO2(g)+O2(g)![]() 2SO3(g) △H<0。
2SO3(g) △H<0。
①下列有关该反应速率的叙述正确的是_____________(填字母)。
a.升高温度可以增大活化分子百分数,加快反应速率
b.增大压强能增大活化分子百分数,加快反应速率
c.使用催化剂可以使反应物分子平均能量升高,加快反应速率
d.在质量一定的情况下,催化剂颗粒的表面积大小,对反应速率有显著影响
②该反应的化学平衡常数表达式为K=____________。
③下列有关图像一定正确的是__________(填字母)。

(3)现有甲、乙两个体积相等的恒容容器,甲容器中充入1molSO2和1molO2,乙容器中充入1molSO3和0.5molO2,发生反应:2SO2(g)+O2(g)![]() 2SO3(g) △H<0,甲、乙容器起始反应温度相同,两容器均为绝热容器,平衡时,甲容器中SO2的转化率为a,乙容器中SO3的分解率为b,则:
2SO3(g) △H<0,甲、乙容器起始反应温度相同,两容器均为绝热容器,平衡时,甲容器中SO2的转化率为a,乙容器中SO3的分解率为b,则:
①a+b__________1(填“<”、“>”或“=”)。
②下列叙述能说明甲容器中反应达平衡状态的是_______________(填字母)。
A.v正(O2)=2v逆(SO3) B.混合气体的密度不变
C.c(SO2)=c(SO3) D.混合气体的总物质的量不变
E.容器内温度不变 F.SO2和O2的质量比不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各离子组可在同一溶液中大量共存,且形成无色溶液的是( )
A. Fe2+、H+、NO3-、Cl- B. H+、Na+、Cl-、CO32-
C. Na+、Mg2+、OH-、SO42- D. K+、Na+、OH-、NO3-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知有机物C的分子式为C9H9OCl,分子中有一个苯环,苯环上只有一个侧链且不含甲基,一定条件下C能发生银镜反应。C与其他物质之间的转化如图所示(部分无机产物已略去):

(1)F中官能团的名称是_____________________;C→F的反应类型是____________。
(2)C的结构简式是______________________,I的结构简式是__________________。
(3)D与银氨溶液反应的化学方程式为_________________________________。
(4)有的同学认为B中可能没有氯原子,理由是_______________________。
(5)D的一种同系物W(分子式为C8H8O2)有多种同分异构体,则符合以下条件的W的同分异构体有________种,写出其中核磁共振氢谱有4个峰且能发生银镜反应的结构简式___________________。
①属于芳香族化合物
②遇FeCl3溶液不变紫色
③能与NaOH溶液发生反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】镁——H2O2酸性电池采用海水作电解质(加入一定量酸),下列说法正确的是( )
A.电池总反应为Mg+H2O2+2H+=Mg2++ 2H2O
B.负极反应为H2O2+2e-+ 2H+= 2H2O
C.电池工作时,正极周围海水的pH减小
D.电池工作时,溶液中的H+向负极移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知S2O8n-离子和H2O2一样含过氧键,因此也有强氧化性,S2O8n-离子在一定条件下可把Mn2+氧化成MnO4-离子,若反应后S2O8n-离子生成SO42-离子;又知反应中氧化剂与还原剂的离子数之比为5:2则S2O8n-中的n值和S元素的化合价是( )
A. 2, +7 B. 2, +6 C. 4 ,+7 D. 4 , +4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】中学化学中有很多物质可以实现下图中物质之间的转化.其中反应条件和部分反应的产物已略去.液体B和C可能是单一溶质的溶液,也可能是纯净物. 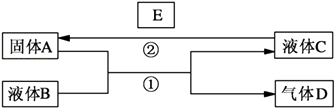
(1)若A是一种红色金属,气体D能使品红溶液褪色,加热时又恢复原色.写出反应①的化学方程式 .
(2)若A是金属单质,D是一种无色气体,遇到空气变为红棕色,液体C呈蓝色.写出反应①的离子方程式;
写出反应②的任意一个离子方程式 .
(3)若A是一种金属单质,D是最轻的气体,B能否是NaOH溶液(填“能”或“否”).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】[2017新课标Ⅲ]氟他胺G是一种可用于治疗肿瘤的药物。实验室由芳香烃A制备G的合成路线如下:
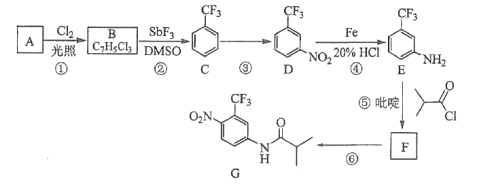
回答下列问题:
(1)A的结构简式为____________。C的化学名称是______________。
(2)③的反应试剂和反应条件分别是____________________,该反应的类型是__________。
(3)⑤的反应方程式为_______________。吡啶是一种有机碱,其作用是____________。
(4)G的分子式为______________。
(5)H是G的同分异构体,其苯环上的取代基与G的相同但位置不同,则H可能的结构有______种。
(6)4-甲氧基乙酰苯胺(![]() )是重要的精细化工中间体,写出由苯甲醚(
)是重要的精细化工中间体,写出由苯甲醚(![]() )制备4-甲氧基乙酰苯胺的合成路线___________(其他试剂任选)。
)制备4-甲氧基乙酰苯胺的合成路线___________(其他试剂任选)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下,在固定容积的密闭容器中,能表示反应X(g)+2Y(g)![]() 2Z(g)一定达到化学平衡状态的是
2Z(g)一定达到化学平衡状态的是
①X、Y、Z的物质的量之比为1∶2∶2
②X、Y、Z的浓度不再发生变化
③容器中气体的压强不再发生变化
④单位时间内生成n mol Z,同时生成n mol X
A. ①② B. ①④ C. ②③ D. ③④
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com