
某实验小组依据甲醇燃烧的反应原理,设计如图所示的电池装置。
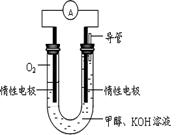 (1)该电池中OH-向_______极移动(填“正”或“负”)
(1)该电池中OH-向_______极移动(填“正”或“负”)
(2)该电池负极的电极反应为_______________________________。
(3)用该电池电解(惰性电极)500 mL某CuSO4溶液,电解一段时间后,
为使电解质溶液恢复到原状态,需要向溶液中加入9.8 g Cu(OH)2
固体。则原CuSO4溶液的物质的量浓度为_______________,
电解过程中收集到标准状况下的气体体积为_____________。
科目:高中化学 来源: 题型:
 A、B、C、D、E、F是中学化学中常见的六种短周期元素,有关位置及信息如下:A的最高价氧化物对应的水化物与其氢化物反应生成离子化合物;C单质一般保存在煤油中;F的最高价氧化物对应的水化物既能与酸反应又能与碱反应,G单质是日常生活中用量最大的金属,易被腐蚀或损坏。请回答下列问题:
A、B、C、D、E、F是中学化学中常见的六种短周期元素,有关位置及信息如下:A的最高价氧化物对应的水化物与其氢化物反应生成离子化合物;C单质一般保存在煤油中;F的最高价氧化物对应的水化物既能与酸反应又能与碱反应,G单质是日常生活中用量最大的金属,易被腐蚀或损坏。请回答下列问题:
(1)A元素的氢化物水溶液能使酚酞变红的原因用电离方程式解释为 。
(2)同温同压下,将a L A氢化物的气体和b L D的氢化物气体通入水中,若所得溶液的pH=7,
则a b(填“>"或“<”或“=”)
(3)常温下,相同浓度F、G简单离子的溶液中滴加NaOH溶液,F、G两元素先后沉淀,F (OH)n完全沉淀的pH是4.7,G (OH)n完全沉淀的pH是2.8,则ksp较大的是: (填化学式)
(4)A与B可组成质量比为7:16的三原子分子,该分子释放在空气中其化学作用可能引发的后果有: 。
①酸雨 ②温室效应 ③光化学烟雾 ④臭氧层破坏
(5)A和C组成的一种离子化合物,能与水反应生成两种碱,该反应的化学方程式是 。
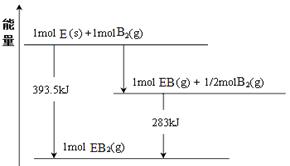
(6)已知一定量的E单质能在B2 (g)中燃烧,其可能的产物及能量关系如下左图所示:请写出一定条件下EB2(g) 与E(s)反应生成EB(g)的热化学方程式 。

(7)若在D与G组成的某种化合物的溶液甲中,加入铜片,溶液会慢慢变为蓝色,依据产生该现象的反应原理,所设计的原电池如上右图所示,其反应中正极反应式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列涉及离子方程式书写的评价合理的是 ( )
| 选项 | 化学反应及离子方程式 | 评价 |
| A | 次氯酸钙溶液中通入足量SO2:Ca2++ClO-+SO2+H2O===CaSO4↓+Cl-+2H+ | 正确 |
| B | 实验室用浓盐酸与MnO2反应制Cl2:MnO2+4H++2Cl- | 错误,H+、Cl-的化学计量数应相等 |
| C | 硝酸铁溶液中加过量氨水:Fe3++3NH3·H2O===Fe(OH)3(胶体)+3NH | 错误,Fe(OH)3应该是沉淀 |
| D | 铝溶于碳酸中:2Al+3H2CO3===2Al3++3H2↑+3CO | 正确 |
查看答案和解析>>
科目:高中化学 来源: 题型:
反应A(g)+2B(g)=C(g)的反应过程中能量变化如右下图所示。曲线a表示不使用催化剂时反应的能量变化,曲线b表示使用催化剂后的能量变化。下列相关说法正确的是
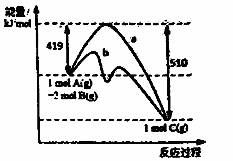
A.该反应是吸热反应
B.催化剂改变了该反应的焓变
C.催化剂降低了该反应的活化能
D.该反应的焓变△H=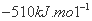
查看答案和解析>>
科目:高中化学 来源: 题型:
高铁电池是一种新型可充电电池,电解质溶液为KOH,放电时的总反应式为:( )
3Zn+2K2FeO4+8H2O 3Zn(OH)2+2Fe(OH)3+4KOH,下列叙述正确的是
3Zn(OH)2+2Fe(OH)3+4KOH,下列叙述正确的是
A.放电时负极反应为:3Zn —6e—+6OH— == 3Zn(OH)2
B.放电时OH—向正极移动
C.充电时每转移3 mol电子,阳极有1 mol Fe(OH)3 被还原
D.充电时阳极反应式为:3Zn(OH)2+6e— == 3Zn+6OH—
查看答案和解析>>
科目:高中化学 来源: 题型:
已知:A、B、C、D、E为周期表1~36号中的元素,它们的原子序数逐渐增大。A的基态原子有3个不同的能级,各能级中电子数相等;C的基态原子2p能级上的未成对电子数与A原子相同;C2—离子D2+离子具有相同的、稳定的电子层结构;E的基态原子的外围电子排布式为3d84s2。
请回答下列问题:
⑴A、B、C、D四种元素中,电负性最大的是 (填元素符号)。
⑵B的氢化物的沸点远高于A的氢化物的主要原因是 。
⑶由A、B、C形成的离子CAB-与AC2互为等电子体,则CAB-中A原子的杂化方式为 。
 ⑷E2+离子能与AC分子形成[E(AC)4]2+,其原因是AC分子中含有 。
⑷E2+离子能与AC分子形成[E(AC)4]2+,其原因是AC分子中含有 。
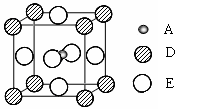
⑸最近发现,只含A、D、E三种元素的一种晶体(晶胞如右图所示)具有超导性。A原子的配位数为 ;该晶体的化学式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
一定条件下,可逆反应X(g)+3Y(g) 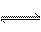 2Z(g),若X、Y、Z起始浓度分别为c1、c2、c3(均不为0),当达平衡时X、Y、Z的浓度分别为0.1mol /L,0.3mol/ L,0.08 mol/L,则下列判断不合理的是
2Z(g),若X、Y、Z起始浓度分别为c1、c2、c3(均不为0),当达平衡时X、Y、Z的浓度分别为0.1mol /L,0.3mol/ L,0.08 mol/L,则下列判断不合理的是
A.c1:c2=1:3 B.平衡时,Y和Z的生成速率之比为3:2
C.X、Y的转化率不相等 D.c1的取值范围为0< c1 <0.14 mo /L
查看答案和解析>>
科目:高中化学 来源: 题型:
现代工业将煤炭气化,既可以提高燃料的利用率、减少CO、SO2等的排放,又可以扩大水煤气的广泛用途。
⑴已知:2C(s)+O2(g)=2CO(g);ΔH1 , 2H2(g)+O2(g)=2H2O(g);ΔH2 。
则反应C(s)+H2O(g)  CO(g)+H2(g);ΔH= 。(用含ΔH1、ΔH2
CO(g)+H2(g);ΔH= 。(用含ΔH1、ΔH2
的代数式表示)
(2)制甲醇所需要的氢气,可用下列反应制取:
H2O(g)+CO(g)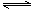 H2(g)+CO2(g)△H < 0 某温度下,该反应的平衡常数K=1。
H2(g)+CO2(g)△H < 0 某温度下,该反应的平衡常数K=1。
①该温度下,若起始时c(CO)= 1 mol/L, c(H2O)= 2 mol/L,反应进行一段时间后,测得H2的浓度为0.5 mol/L,则此时该反应v(正) v(逆) (填>、=、<)。
②若降低温度,该反应的K值将 。(填"增大"、"减小"或"不变" )
③据研究CO(g)+2H2(g) CH3OH(g),制备甲醇的反应过程中起催化作用的为Cu2O,反应体系中含少量CO2有利于维持催化剂Cu2O的量不变,原因是: _______________________________________ (用化学方程式表示)。
CH3OH(g),制备甲醇的反应过程中起催化作用的为Cu2O,反应体系中含少量CO2有利于维持催化剂Cu2O的量不变,原因是: _______________________________________ (用化学方程式表示)。
(3)CO和H2在一定条件下合成甲醇的反应为:CO(g)+2H2(g)  CH3OH(g);ΔH3。现在容积均为1L的a、b、c、d、e五个密闭容器中分别充入1mol CO和2mol H2的混合气体,控温,进行实验,测得相关数据如下图1和图2。
CH3OH(g);ΔH3。现在容积均为1L的a、b、c、d、e五个密闭容器中分别充入1mol CO和2mol H2的混合气体,控温,进行实验,测得相关数据如下图1和图2。
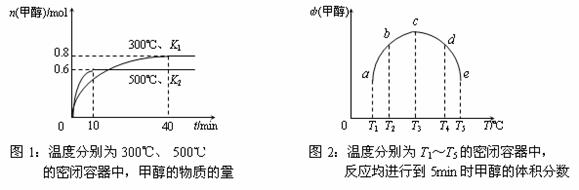
①该反应的ΔH3 0(选填“<”、“>”或“=”,下同),K1 K2。
②将容器c中的平衡状态转变到容器d中的平衡状态,可采取的措施有 。
(4)某燃料电池以CO为燃料,以空气为氧化剂,以熔融态K2CO3为电解质。写出该燃料电池负极的电极反应式: 。
查看答案和解析>>
科目:高中化学 来源: 题型:
将4.6 g Cu和Mg完全溶于浓硝酸溶液中,反应中硝酸的还原产物为4480mL NO2气和336 mL N2O4气体(标准状况下),反应后的溶液中,加入过量NaOH溶液,生成沉淀的质量为 ( )
A. 9.02 g B. 8.51 g C. 8.26 g D. 7.04 g
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com