
【题目】柔性屏手机开始崭露头脚。某柔性屏手机的柔性电池以碳纳米管作电极材料,以吸收ZnSO4溶液的有机高聚物为固态电解质,其电池总反应为:MnO2+![]() Zn+(1+
Zn+(1+![]() )H2O+
)H2O+![]() ZnSO4
ZnSO4 ![]() MnOOH+
MnOOH+![]() ZnSO4·3Zn(OH)2·xH2O,其电池结构如图1所示,图2是有机高聚物的结构片段。下列说法中,正确的是
ZnSO4·3Zn(OH)2·xH2O,其电池结构如图1所示,图2是有机高聚物的结构片段。下列说法中,正确的是

A.充电时,含有锌膜的碳纳米管纤维一端连接电源正极
B.放电时,电极的正极反应为:MnO2+e-+H+=MnOOH
C.充电时,Zn2+移向Zn膜
D.氢键是一种特殊的化学键,键能大于共价键,能使高聚物更稳定
 开心练习课课练与单元检测系列答案
开心练习课课练与单元检测系列答案科目:高中化学 来源: 题型:
【题目】一种形状像布袋结构的烯烃分子,其形状和结构如图所示,有关说法不正确的是( )

A. 该烯烃的分子式为C5H4
B. 该分子所有碳原子在同一平面
C. 1 mol该有机物最多可与2 mol Br2发生加成反应
D. 与其互为同分异构体且只含三键的链烃不止—种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙醇是制取饮料、香精、染料、涂料、洗涤剂等产品的原料。

完成下列填空:
(1)实验室用乙醇制取乙烯时,浓硫酸的用量远远超过作为催化剂的正常用量,原因是______。
(2)验证乙烯加成反应性质时,需对乙烯气体中的干扰物质进行处理,可选用的试剂是_____(填写化学式);能确定乙烯通入溴水中发生了加成反应的事实是______。(选填编号)
a.溴水褪色 b.有油状物质生成
c.反应后水溶液酸性增强 d.反应后水溶液接近中性
(3)实验室用乙醇和乙酸制备乙酸乙酯时,甲、乙两套装置如图1都可以选用。关于这两套装置的说法正确的是______。(选填编号)

a.甲装置乙酸转化率高 b.乙装置乙酸转化率高
c.甲装置有冷凝回流措施 d.乙装置有冷凝回流措施
(4)用乙装置实验时,提纯乙中乙酸乙酯的流程如图3以上流程中试剂A的化学式是______;操作Ⅱ的名称是______;操作Ⅲ一般适用于分离______混合物。
(5)如图2是用乙醇制备溴乙烷的装置,实验中有两种加料方案:
①先加溴化钠→再加乙醇→最后加1:1浓硫酸;
②先加溴化钠→再加1:1浓硫酸→最后加乙醇。
按方案①和②实验时,产物都有明显颜色,若在试管中加入______,产物可变为无色。与方案①相比较,方案②的明显缺点是______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列“实验结论”与“实验操作及现象”不相符的一组是( )
选项 | 实验操作及现象 | 实验结论 |
A | 把一小块钠放入水中,立刻熔成小球 | 该反应是放热反应 |
B | 向某溶液中加入AgNO3溶液,产生白色沉淀 | 该溶液中一定含有Cl- |
C | 向NaHCO3溶液中滴入酚酞溶液,溶液颜色变红 | NaHCO3溶液显碱性 |
D | 向某溶液中加入NaOH溶液,生成的白色絮状沉淀迅速变成灰绿色,最后变成红褐色 | 该溶液中一定含有Fe2+ |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某密闭容器中充入等物质的量的气体A和B,一定温度下发生反应:A(g)+xB(g)![]() 2C(g),达到平衡后,只改变反应的一个条件,测得容器中物质的浓度、反应速率随时间的变化关系如图所示。下列说法中正确的是
2C(g),达到平衡后,只改变反应的一个条件,测得容器中物质的浓度、反应速率随时间的变化关系如图所示。下列说法中正确的是
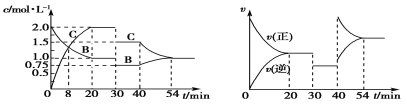
A.反应方程式中的x=1
B.该反应为放热反应
C.30 min时改变的条件是加入催化剂
D.前30 min内 A的反应速率为0.05 mol/(L·min)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用反应6NO2+8NH3=7N2+12H2O构成电池的方法,既能实现有效除氮氧化物的排放,减轻环境污染,又能充分利用化学能,装置如图所示,回答问题:
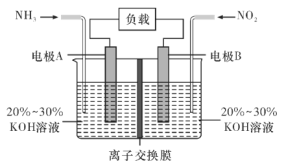
(1)电流从____(选填“左”或“右”,下同)侧电极经过负载后流向______侧电极。
(2)为使电池持续放电,离子交换膜需选用______离子交换膜(选填“阴”或“阳”)。
(3)A电极上的电极反应式为___________________________。
(4)当有4.48 L NO2(标准状况)被处理时,转移电子为________摩尔。
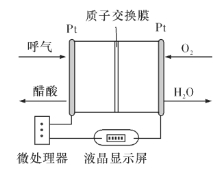
(5)负载可以测定电流大小,从而确定气体含量,酒驾测定工作原理与其相似。仔细阅读图:写出酒驾测定中电池总反应方程式:______________________________,负极反应方程式:____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】立方烷衍生物I的合成路线如图:
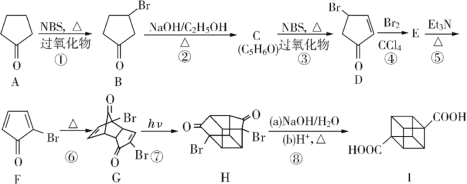
请回答下列问题:
(1)C的结构简式为____________,E的结构简式为__________。
(2)③的反应类型为____________,⑤的反应类型为__________。
(3)已知A由下述三步反应,其中第3步反应试剂和条件为O2/Cu,△。
![]()
请写出反应1的试剂和条件:___________,反应2的化学方程式为_______________________。
(4)在该合成路线中的化合物(A~I),其中互为同分异构体的是_____________(填字母代号)
(5)化合物I的核磁共振氢谱共有____组峰,峰面积之比为____________。
(6)第⑥步反应的名称为D-A反应,理解其中成键与断键关系,请写出由乙炔为原料合成1,4-环己二烯流程。(无机试剂、溶剂任选)_______________
(7)写出以![]() 和
和![]() 为原料,制备医药中间体
为原料,制备医药中间体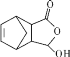 的合成路线(无机试剂、溶剂任选)___________
的合成路线(无机试剂、溶剂任选)___________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,向1 L pH=10的 NaOH溶液中持续通入CO2。通入CO2的体积(V)与溶液中水电离产生的OH-离子浓度(c)的关系如图所示。
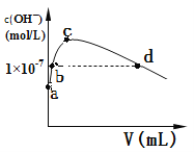
(1)c点溶液中离子浓度由大至小的关系是:________________________________________________。
(2)a点溶液中由水电离产生的c(H+)=______________;b点溶液中c(H+)________1×10-7mol/L(填写“等于”、“大于”或“小于”)。
(3)能使0.1mol/L乙酸溶液的电离程度以及pH都增大的是___。(选填序号)
a.加水稀释 b.加入少量乙酸钠固体 c.通氯化氢 d.加入少量苛性钠固体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图表示反应 N2(g)+3H2(g)![]() 2NH3(g)+Q的正反应速率随时间的变化情况,试根据如图曲线判断下列说法可能正确的是( )
2NH3(g)+Q的正反应速率随时间的变化情况,试根据如图曲线判断下列说法可能正确的是( )
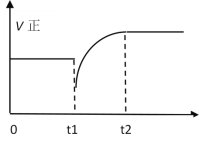
A.t1时只减小了压强
B.t1时只降低了温度
C.t1时只减小了NH3的浓度,平衡向正反应方向移动
D.t1时减小N2浓度,同时增加了NH3的浓度
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com