
【题目】(化学——选修5:有机化学基础)
合成抗癌新药盐酸埃克替尼的关键中间体G的一种合成路线如下图:

已知:①A分子中只有一种化学环境的氢;
②TsCl为![]()
(1)A的结构简式为__________________。
(2)E的分子式为_____________;G中的含氧官能团的名称有___________。
(3)由E生成F的反应类型是________________。
(4)W是D的同分异构体.W是三取代芳香族化合物,既能发生银镜反应和水解反应,又能与FeC13溶液发生显色反应;1mol W最多可与4mol NaOH反应,W的同分异构体有______种;若W的核磁共振氢谱只有4组峰.则W的结构简式为:_____________。
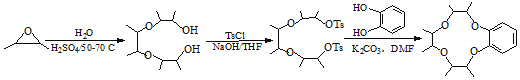
(5)参照上述合成路线,以(![]() )和邻苯二酚为原料(其它试剂任选),设计制备的
)和邻苯二酚为原料(其它试剂任选),设计制备的 合成路线。_____________________________________
合成路线。_____________________________________
【答案】![]() C13H16O6 醚键和羧基 取代反应 6
C13H16O6 醚键和羧基 取代反应 6 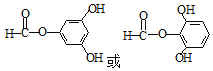
【解析】
A分子不饱和度=(2×2+24)/2=1,A分子中只有一种化学环境的氢,则A结构简式为![]() ,B反应取代反应生成C,E发生取代反应生成F,根据F结构简式知,E结构简式为
,B反应取代反应生成C,E发生取代反应生成F,根据F结构简式知,E结构简式为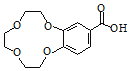 ,C发生取代反应生成E,F发生还原反应生成G;依据题中信息,先用
,C发生取代反应生成E,F发生还原反应生成G;依据题中信息,先用![]() 合成
合成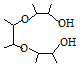 ,
, 发生取代反应生成
发生取代反应生成 ,
, 发生取代反应生成
发生取代反应生成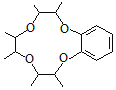 ,据此答题。
,据此答题。
A分子不饱和度=(2×2+24)/2=1,A分子中只有一种化学环境的氢,则A结构简式为![]() ,B反应取代反应生成C,E发生取代反应生成F,根据F结构简式知,E结构简式为
,B反应取代反应生成C,E发生取代反应生成F,根据F结构简式知,E结构简式为 ,C发生取代反应生成E,F发生还原反应生成G。
,C发生取代反应生成E,F发生还原反应生成G。
(1)通过以上分析知,A的结构简式为![]() ,故答案为:
,故答案为:![]() 。
。
(2)E的结构简式为 ,则其分子式为C13H16O6:G中的含氧官能团的名称有醚键和羧基;
,则其分子式为C13H16O6:G中的含氧官能团的名称有醚键和羧基;
故答案为:C13H16O6,醚键和羧基。
(3)由E生成F的反应类型是取代反应,
故答案为:取代反应。
(4)W是D的同分异构体,W是三取代芳香族化合物,说明W含有苯环;既能发生银镜反应和水解反应,又能与FeCl3溶液发生显色反应,说明W含有酯基、醛基和酚羟基;1molW最多可与4molNaOH反应,则E为含有酚羟基、HCOO—,如果两个—OH处于邻位,有2种同分异构体,如果两个—OH处于间位,有3种同分异构体,如果两个—OH处于对位,有1种同分异构体,所以W的同分异构体有6种;若W的核磁共振氢谱只有4组峰.则W的结构简式为: ,
,
故答案为:6; 。
。
(5)根据题中信息,先用![]() 合成
合成 ,
, 再发生取代反应生成
再发生取代反应生成 ,最后用
,最后用 合成
合成 。具体合成路线为:
。具体合成路线为: ,
,
故答案为: 。
。


 应用题作业本系列答案
应用题作业本系列答案科目:高中化学 来源: 题型:
【题目】三氧化二镍(Ni2O3)可用于制造高能电池元件。电解法制备过程如下:用NaOH 溶液将NiCl2溶液的pH调至7.5(该pH下溶液中的Ni2+不沉淀),加入适量硫酸钠固体后进行电解。电解过程中产生的Cl2(不考虑Cl2的逸出)在弱碱性条件下生成ClO﹣,ClO﹣再把二价镍(可简单写成Ni2+)氧化为Ni3+,再将Ni3+经一系列反应后转化为Ni2O3,电解装置如图所示。下列说法不正确的是( )

A. 加入适量硫酸钠的作用是增加离子浓度,增强溶液的导电能力
B. 电解过程中阴、阳两极附近溶液的pH均升高
C. 当有1mol Ni2+氧化为Ni3+时,外电路中通过的电子数目为1NA,通过阳离子交换膜的Na+数目为1NA
D. 反应前后b池中Cl- 浓度几乎不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】云南是南方丝绸之路的重要节点,有着丰富的铜镍矿石资源。回答下列相关问题:
(1)镍在元素周期表中的位置是____,其基态原子的电子排布式为_____,该原子核外有___个未成对电子。
(2)Ni(NH3)4SO4中N的杂化轨道类型是_____;1 mol Ni(NH3)42+中含有的![]() 键数目为____个;SO42-的立体构型是______。
键数目为____个;SO42-的立体构型是______。

(3)氨是_____分子(填“极性”或“非极性”),经测定NH4F为分子晶体,类比NH3·H2O表示出NH4F分子中的氢键_____。
(4)铜镍合金的立方晶胞结构如图所示,其中原子A的坐标参数为(0,1,0);
①原子B的坐标参数为____;
②若该晶体密度为dg/cm3,则铜镍原子间最短距离为____pm
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A. 含有金属元素的化合物一定是离子化合物
B. 具有共价键的化合物就是共价化合物
C. 由非金属元素形成的化合物一定不是离子化合物
D. 含有离子键的化合物必是离子化合物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.酯的水解反应和酯化反应都属于取代反应
B.乙烯能使溴水褪色,发生氧化反应
C.乙醇不能被酸性高锰酸钾溶液氧化
D.葡萄糖不能发生银镜反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某废旧锂电池材料含有钴酸锂(LiCoO2)、导电剂石墨和铝粉等。回收废旧锂电池中钴的工艺流程如下:

已知:Ksp(CoC2O4)=2.5×10-9,Ksp(CoCO3)=1.5×10-13
回答下列问题:
(1)“浸出液”的主要成分是LiHC2O4、Al(HC2O4)3,“浸出渣”的主要成分是CoC2O4。“浸出”中生成CoC2O4的化学方程式为 _______ ,若H2C2O4用量过大,CoC2O4的产率反而会降低,原因是____。
(2)“转化”中加入Na2CO3溶液发生反应的离子方程式为___________,该反应进行的程度较大,试用平衡常数K解释原因 _____ 。
(3)“电解”时装置如图所示。阳极的电极反应式为______,电解后a室中的电解液可返回 ________工序继续使用。

(4)某废旧锂电池粉末中LiCoO2的质量分数为w,将mkg该废料进行回收利用,电解得到钴nkg,钴的回收率为____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求完成下列问题:
(1)乙酸乙酯的键线式 _________________;间二甲苯的结构简式 ____________________;![]() 的分子式 ______________________;
的分子式 ______________________;
(2)戊烷(C5H12)的某种同分异构体只有一种一氯代物,该烃的结构简式: __________;
(3)分子式为C4H9Cl的物质,有4种同分异构体,请写出这4种同分异构体的结构简式:___________, __________, __________, _________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铅蓄电池的两极分别为Pb、PbO2,电解液为硫酸,工作时的反应为Pb+PbO2+2H2SO4=2PbSO4+2H2O,下面结论正确的是
A. Pb为正极,被氧化B. 溶液的pH不断减小
C. SO42-只向PbO2处移动D. 电解液密度不断减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于0.2mol/LBa(NO3)2溶液,正确的说法是( )
A.该溶液中含有的Ba2+离子的物质的量是0.2mol
B.该溶液中含有的NO3-离子的物质的量是0.4mol
C.若此溶液是0.5升,则其中Ba2+离子的物质的量浓度为0.1mol/L
D.若此溶液是0.5升,则其中所含NO3-离子的物质的量为0.2mol
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com