
【题目】人体内的微量元素对人体的健康起着重要作用。下列各元素中,全部属于微量元素的是
A. I、K、O、S B. N、H、O、P、C
C. B、Mo、Fe、Zn、Cu D. Fe、Ca、Cu、Mg、C
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】设NA表示阿伏加德罗常数的值。下列说法正确的是( )
A.一定条件下,0.2 mol SO2与足量O2充分反应,生成SO3分子数为0.2NA
B.0.1 mol —NH2(氨基)中含有的电子数为0.7NA
C.3.4 g H2O2中含有的共用电子对数为0.1NA
D.常温常压下,16 g O2和O3混合气体含有的氧原子数为NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:Ksp(AgCl) = 1.8 × 10-10 ,Ksp(AgI) = 1.5 × 10-16 ,Ksp(Ag2CrO4) =2.0 × 10-12,则在相同温度下,下列难溶盐的饱和溶液中,Ag+浓度大小顺序正确的是
A.AgCl>AgI>Ag2CrO4 B.AgCl>Ag2CrO4>AgI
C.Ag2CrO4>AgCl>AgI D.Ag2CrO4>AgI>AgCl
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示为8000C时A、B、C三种气体在密闭容器中反应时浓度的变化只从图上分析不能得出的结论是( )

A.A是反应物
B.前2 min A的分解速率为0.1molL-1min-1
C.达平衡后,若升高温度,平衡向正反应方向移动
D.达平衡后,若增大压强,平衡向逆反应方向移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)实验室用Na2CO310H2O晶体配制0.05mol/L的Na2CO3溶液970mL,应选用的容量瓶的规格 ,称取Na2CO310H2O的质量是 g。
(2)2molO3和3molO2的质量之比为 ,分子数之比为 ,同温同压下的密度之比为 ,含氧原子数之比为 。
(3)现有下列九种物质①AgCl ②铜 ③液态醋酸 ④CO2 ⑤H2SO4 ⑥Ba(OH)2固体 ⑦酒精 ⑧稀硝酸 ⑨熔融FeCl3
①上述状态下可导电的是(填序号,下同) ,属于电解质的是 ,属于非电解质的是 。
②上述九种物质中有两种物质之间可发生离子反应H++OH-=H2O,该离子反应对应的化学方程式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】近年来燃煤脱硫技术受到各界科研人员的重视,某脱硫技术涉及如下反应:
Ⅰ. CaSO4(s)+CO(g)![]() CaO(s)+SO2(g)+CO2(g) ΔH1=+218.4 kJ· mol-1
CaO(s)+SO2(g)+CO2(g) ΔH1=+218.4 kJ· mol-1
Ⅱ. CaO(s)+3CO(g)+SO2(g)![]() CaS(s)+3CO2(g) ΔH2=-394.0 kJ· mol-1
CaS(s)+3CO2(g) ΔH2=-394.0 kJ· mol-1
(1) 若用K1、K2分别表示反应Ⅰ、Ⅱ的化学平衡常数,则反应![]() CaSO4(s)+2CO(g)
CaSO4(s)+2CO(g)![]()
![]() CaS(s)+2CO2(g)的平衡常数K= (用含K1、K2的式子表示)。
CaS(s)+2CO2(g)的平衡常数K= (用含K1、K2的式子表示)。
(2) 某科研小组研究在其他条件不变的情况下,改变起始一氧化碳物质的量对反应Ⅱ的影响,实验结果如右图所示(图中T表示温度)。
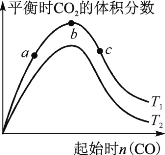
比较在a、b、c三点所处的平衡状态中,反应物SO2的转化率最高的是 。
②图像中T2 (填“高于”、“低于”、“等于”或“无法确定”)T1,判断的理由是 。
(3)反应3X+Y![]() 2Z在2 min达到平衡后的t1~t6内反应速率与反应时间图像如图,在每一时刻均改变一个影响反应速率的因素,则( )
2Z在2 min达到平衡后的t1~t6内反应速率与反应时间图像如图,在每一时刻均改变一个影响反应速率的因素,则( )

A.在t1时增大了压强 B.在t3时加入了催化剂
C.在t4时降低了温度 D.t2~t3时A的转化率最高
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知反应:H2(g)+![]() O2(g)===H2O(g) ΔH1 ; N2(g)+O2(g)===2NO(g) ΔH2 ;N2(g)+3H2(g)===2NH3(g) ΔH3 ,则反应2NH3(g)+
O2(g)===H2O(g) ΔH1 ; N2(g)+O2(g)===2NO(g) ΔH2 ;N2(g)+3H2(g)===2NH3(g) ΔH3 ,则反应2NH3(g)+![]() O2(g)===2NO(g)+3H2O(g)的ΔH为( )
O2(g)===2NO(g)+3H2O(g)的ΔH为( )
A.3ΔH1+2ΔH2-ΔH3 B.ΔH1+ΔH2-ΔH3
C.3ΔH1+ΔH2+ΔH3 D.3ΔH1+ΔH2-ΔH3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】通常人们把拆开1 mol某化学键所吸收的能量或形成1 mol某化学键所释放的能量看作该化学键的键能,键能的大小可用于估算化学反应的反应热(ΔH),已知
化学健 | H-H | Cl-Cl | H-Cl |
键能 | 436 kJ/mol | 243 kJ/mol | 431 kJ/mol |
则下列热化学方程式不正确的是( )
A.![]() H2(g)+
H2(g)+![]() Cl2(g)===HCl(g) ΔH=-91.5 kJ·mol-1
Cl2(g)===HCl(g) ΔH=-91.5 kJ·mol-1
B.H2(g)+Cl2(g)===2HCl(g) ΔH=-183 kJ·mol-1
C.2HCl(g)===H2(g)+Cl2(g) ΔH=+183 kJ·mol-1
D.![]() H2(g)+
H2(g)+![]() Cl2(g)===HCl(g) ΔH=91.5 kJ·mol-1
Cl2(g)===HCl(g) ΔH=91.5 kJ·mol-1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com