
����Ŀ���ӣ�Cd����һ����;�㷺�Ľ�����Ҳ�Ƕ����彡����в�����к�Ԫ��֮һ��
��1��1.00gCdS������ȫȼ������CdO�����SO2����ų�2.75kJ���������÷�Ӧ���Ȼ�ѧ����ʽΪ____��
��2�������£�Ksp(CdCO3) = 4.0��10��12��Ksp[Cd(OH)2] = 3.2 ��10��14�����ܽ�ȣ�mol��L��1���ϴ����____ [�CdCO3����Cd(OH)2��]������112mg��L��1 Cd2+�ķ�ˮ�Ӽ��pH��9.0���ﵽƽ��ʱ����Һ��c(Cd2+)=____��
��3��һ���������������Ʊ���������ȥ�����ӷ�ˮ��Cd2+��ԭ�����£�

�پ۱������ĵ���Ľṹ��ʽΪ____��
��ʹ����������������ij���ӷ�ˮ����ȥ������pH�Ĺ�ϵ��ͼ-1��ʾ����ǿ���������£�pHԽС����Ч��Խ���ԭ����____��

��4��һ���õ綯��ѧ��������Ⱦ��������װ����ͼ-2��ʾ��
��ʵ��ǰ������������NaOH��Һ��ϡ���ἰ����ˮϴ�ӣ���Ŀ����____��
��ʵ������������Ϸ����ĵ缫��ӦΪ____��
�ۻ���̿��������____��
���𰸡� 2CdS(s) + 3O2(g) = 2CdO(s) +2SO2(g) ��H =��792kJ��mol��1 Cd(OH)2 3.2��10��4 mol��L��1 CH2=CHCONH2 H+�룭NH2����NH���ϵĵ�ԭ�ӽ�ϣ������������������Ļ��� ��ȥ���۱������ۺ����� Fe ��2e��= Fe2+ ���������������Ǩ�����ü���Χ��Cd2+��������
����������1��1.00gCdS������ȫȼ������CdO�����SO2����ų�2.75kJ��������288g��2mol CdS������ȫȼ������CdO�����SO2����ų�2.75��288kJ=792kJ���������÷�Ӧ���Ȼ�ѧ����ʽΪ2CdS(s) + 3O2(g) = 2CdO(s) +2SO2(g) ��H =��792kJ��mol��1����2����ΪCdCO3��Cd(OH)2 ����ͬһ��������,ǰ��ΪAB��,����ΪAB2��.���Բ���ֱ�ӱȽ�Ksp����Ҫ��������Һ�е��ܽ��s(mol / L)�� CdCO3 ���ܽ��s =![]() = 2.0��10-6 (mol/L) �� Cd(OH)2 ���ܽ��s =
= 2.0��10-6 (mol/L) �� Cd(OH)2 ���ܽ��s = ![]() = 2 ��10-5 (mol/L)�������ܽ�ȣ�mol��L��1���ϴ����Cd(OH)2�������£�pH=9.0��c(OH-)=10-5mol/L��Ksp[Cd(OH)2] = c(Cd2+)c2(OH-)= c(Cd2+)����10-5mol/L��2= 3.2 ��10��14��c(Cd2+)= 3.2��10��4 mol��L��1����3���پ۱������ĵ���Ϊ����������ṹ��ʽΪCH2=CHCONH2����H+�룭NH2����NH���ϵĵ�ԭ�ӽ�ϣ������������������Ļ��ԣ�����ǿ���������£�pHԽС����Ч��Խ���4����ʵ��ǰ������������NaOH��Һ��ϡ���ἰ����ˮϴ�ӣ��Գ�ȥ���۱������ۺ����⣻��ʵ�������������Ϊԭ��صĸ�������������ʧ���Ӳ����������ӣ��ʷ����ĵ缫��ӦΪFe ��2e��= Fe2+���ۻ���̿�����������������������Ǩ�����ü���Χ��Cd2+�������ӡ�
= 2 ��10-5 (mol/L)�������ܽ�ȣ�mol��L��1���ϴ����Cd(OH)2�������£�pH=9.0��c(OH-)=10-5mol/L��Ksp[Cd(OH)2] = c(Cd2+)c2(OH-)= c(Cd2+)����10-5mol/L��2= 3.2 ��10��14��c(Cd2+)= 3.2��10��4 mol��L��1����3���پ۱������ĵ���Ϊ����������ṹ��ʽΪCH2=CHCONH2����H+�룭NH2����NH���ϵĵ�ԭ�ӽ�ϣ������������������Ļ��ԣ�����ǿ���������£�pHԽС����Ч��Խ���4����ʵ��ǰ������������NaOH��Һ��ϡ���ἰ����ˮϴ�ӣ��Գ�ȥ���۱������ۺ����⣻��ʵ�������������Ϊԭ��صĸ�������������ʧ���Ӳ����������ӣ��ʷ����ĵ缫��ӦΪFe ��2e��= Fe2+���ۻ���̿�����������������������Ǩ�����ü���Χ��Cd2+�������ӡ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ij�о���ѧϰС��Ϊ̽��п�����ᷴӦ��ȡͬ������ͬ�����пƬ��ͬŨ��������������ƽ��ʵ�飺
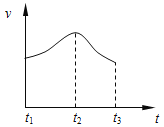
ʵ��٣��Ѵ�пƬͶ�뵽ʢ��ϡ������Թ��У������������������ʱ仯��ͼ��ʾ��
ʵ��ڣ��Ѵ�пƬͶ�뵽��FeCl3��ͬŨ�ȹ�ҵϡ�����У����ַų������������١�
ʵ��ۣ��������е��뼸��CuCl2��Һ�������������ʼӿ졣
�Իش��������⣺
(1)�Է���ʵ�����t1��t2���ʱ仯����Ҫԭ����________��t2��t3���ʱ仯����Ҫԭ����_____________��
(2)ʵ��ڷų������������ٵ�ԭ����_____________��(�����ӷ���ʽ��ʾ)
(3)ʵ��۷�Ӧ���ʼӿ����Ҫԭ����___________��
II��һ���¶��£���2L���ܱ������У�X��Y��Z������������ʵ�����ʱ��仯��������ͼ��ʾ��
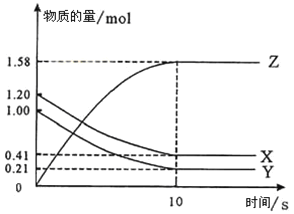
(1)д���÷�Ӧ�Ļ�ѧ����ʽ_______________��
(2)��Ӧ��ʼ��10s����X��ʾ�ķ�Ӧ������__________��
(3)������������˵��������Ӧ�ﵽƽ��״̬����______��
a. ��X��Y�ķ�Ӧ����֮��Ϊ1:1
b. ���������X�������������ֲ���
c. X��Y��Z��Ũ��֮��Ϊ1:1:2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������У����������ᷴӦ������������������Һ��Ӧ���ǣ� ��
A.MgOB.Al(OH)3C.NH4ClD.FeCl3
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ����������������ȷֽ�Ļ�ѧ����ʽΪ��5NH4NO3![]() 2HNO3��4N2��9H2O���ڷ�Ӧ�б������뱻��ԭ�ĵ�ԭ����֮��Ϊ( )
2HNO3��4N2��9H2O���ڷ�Ӧ�б������뱻��ԭ�ĵ�ԭ����֮��Ϊ( )
A. 5��3 B. 5��4 C. 1��1 D. 3��5
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������dz��������ᣬ��ˮ�dz��������
��1��25��ʱ����0.1000mol��L��1����ζ�25.00mL0.1000mol��L��1��ˮ�ĵζ�������ͼ��ʾ��
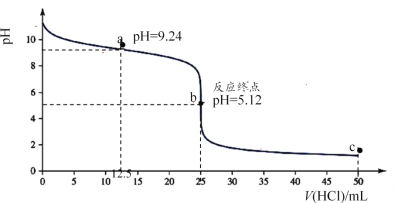
�ٵζ�ʱ����ѡ��____������ȡ���̪������ָʾ���� ��ƿ��ˮ�ĵ���̶ȣ�a��____b�㣨�������������������
�ڵζ�����Ӧ�յ�ǰ����Һ�з�����Ӧ�����ӷ���ʽΪ____��
�۵ζ���a�㴦����ƿ��NH4+ ��Cl����NH3��H2O��Ũ����С������˳��Ϊ____��
�ܵζ���c�㴦����ƿ��NH4+ ��Cl����H+��Ũ����С������˳��Ϊ____��
��2��25��ʱ����HCl��NaOH���ڴ����pH�����һ��c(CH3COOH)+c(CH3COO��)=0.1 mol��L��1��Һ����Һ��H+��OH����CH3COO����CH3COOHŨ�ȵĶ���ֵ��lgc����pH��ϵ��ͼ��ʾ��
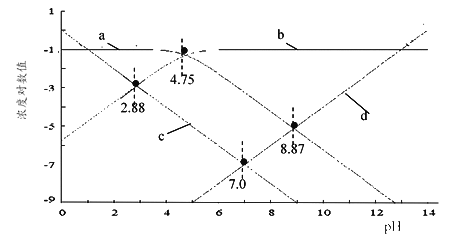
��ͼ�б�ʾH+������____����Сд��ĸ����0.1 mol��L��1CH3COONa��Һ��pHԼΪ____������2λС������
�ڷ�ӦCH3COOH![]() CH3COO��+ H+�ĵ��볣���Ķ���ֵlgK=____������ֵ����
CH3COO��+ H+�ĵ��볣���Ķ���ֵlgK=____������ֵ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��̼����ϩ���㷺������ص���ʡ�����ϳɵ��м���ȡ�һ����CH2=CH2��CO2��O2Ϊԭ�ϣ�������ͭ���⻯����µ��Ʊ�̼����ϩ���ķ�Ӧ���£�

��1��Fe2+��̬��������Ų�ʽΪ____��
��2��д��һ����CO2��Ϊ�ȵ�����������ӣ�____��
��3��̼����ϩ����̼ԭ���ӻ��������Ϊ____��1mol̼����ϩ�������к�![]() ����ĿΪ____��
����ĿΪ____��
��4��FeO�����ṹ��ͼ-1��ʾ����������ÿ��Fe2+���ڵ�Fe2+��____����һ����Sn��Cu��Fe��S��ɵĻ�����ľ����ṹ��ͼ-2��ʾ���û�����Ļ�ѧʽΪ____��

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ԭ��Ӧ�����ֻ�����Ӧ���͵Ĺ�ϵ����ͼ��ʾ�������л�ѧ��Ӧ������Ӱ���ֵ���
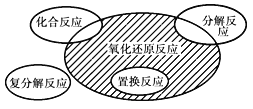
A. Cl2��2KBr=Br2��2KCl
B. 2NaHCO3![]() Na2CO3��H2O��CO2��
Na2CO3��H2O��CO2��
C. 3Mg+N2![]() Mg3N2
Mg3N2
D. 2Na2O2��2CO2=2Na2CO3��O2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������߱�ʾ±��Ԫ��ij��������˵�����ı仯���ƣ���ȷ����

A. A B. B C. C D. D
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ŨHNO3���������ʷ�Ӧ���ȱ��ֳ��������ֱ��ֳ����Ե��ǣ�������
A. CuO B. FeO C. C D. CaCO3
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com