
����Ŀ��ij��ѧʵ���Ҳ����ķ�Һ�к��� Fe3+��Cu2+��Ag+���ֽ������ӣ���ͬѧ���������ͼ��ʾ�ķ����Է�Һ���д������Ի��ս����������������ݴ˷���������˵����ȷ����( )

A. ���� A �к��� 2 �ֽ�������
B. ���� KSCN ��Һ��������Һ B �������Ľ�������
C. ��Һ A ��ֻ�������������ս����õ����� C
D. �����٢ڢ��ж���Ҫ�õ���������©��
���𰸡�B
��������
Fe3+��Cu2+��Ag+���ֽ������Ӻ���������Ӧ�����������Ӻ͵���ͭ��ͨ�����˵õ�����A����ҺA����Ϊ������������AΪ����ͭ�Ļ��������ҺA�������������������Ӿ��л�ԭ�����ױ��������������ʼ�����������ܰ���������������������������ҺB�к��������������ӺͼӦ�������������������ʳ���CΪ����������������ˮͨ����������Fe3+��Cu2+�������ŷ����Դ˽�������
A.��Һ�к���Fe3+��Cu2+��Ag+���ֽ���������������������ۺ��������ӱ���ԭΪ����������ͭ���ӱ���ԭ�ɽ���ͭ�������ӱ���ԭ�������������ڵڢٵõ��ij����к��н���ͭ����������������A����
B.��ҺB�к��еĽ���������ΪFe3+����ΪFe3+��SCN-������������Ӧ��Fe3++3SCN-=Fe(SCN)3����Һ��Ѫ��ɫ��������Һ�е���KSCN��Һ������˵������Һ�к���Fe3+��������ҺB�к��еĽ��������ӳ��õ��Լ���KSCN��Һ������Bѡ������ȷ����
C.��ҺA����������������������������������������������ȶ����ױ���������������������C����
D.�����ڼ������������Ϊ�������ӵ���������������Ҫ©������D������
����Bѡ������ȷ����


 ��ٽ������½������������ϵ�д�
��ٽ������½������������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������ȷ����( )
A.�ڷDZ�״���£�1mol�κ�����������������22.4L
B.ͬ��ͬѹ���������壬ֻҪ���ǵķ�������ͬ����ռ���������ͬ
C.�ڱ�״���£����Ϊ22.4L�����ʶ���1mol
D.1mol�κ���������һ����22.4L
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵������ȷ��һ����(����)
A. H2��D2��T2��Ϊͬλ��
B. 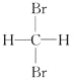 ��
��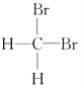 ��Ϊͬ���칹��
��Ϊͬ���칹��
C. ��������춡�黥Ϊͬϵ��
D. (CH3)2CHC2H5��CH3CH2CH(CH3)2����ͬ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ѽ�����ѧƽ���ij���淴ӦX(g)+2Y(g)![]() 2Z(g)���������ı�ʹ��ѧƽ��������Ӧ�����ƶ�ʱ������������ȷ����
2Z(g)���������ı�ʹ��ѧƽ��������Ӧ�����ƶ�ʱ������������ȷ����
�����������������һ�����ӣ�������������һ�����ӣ� ����Ӧ���ת����һ������
����Ӧ���Ũ��һ�����ͣ�������Ӧ����һ�������淴Ӧ���ʣ���һ��ʹ�ô���
A���٢ڢ� B���ۢܢ� C���ڢ� D���ܢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ֳ��£�N2H4����ɫҺ�壩��һ��Ӧ�ù㷺�Ļ���ԭ�ϣ����������ȼ�ϣ��ش��������⣺
��1���������ӵĵ���ʽΪ___________�� ���е��Ļ��ϼ�Ϊ___________��
��2��ʵ�����п��ô���������Һ�백��Ӧ�Ʊ���������Ӧ�Ļ�ѧ����ʽΪ____________.
��3����2O2��g��+N2��g���TN2O4��l�� ��H1
��N2��g��+2H2��g���TN2H4��l�� ��H2
��O2��g��+2H2��g���T2H2O��g�� ��H3
��2N2H4��l��+N2O4��l���T3N2��g��+4H2O��g�� ��H4=��1048.9kJmol��1
������Ӧ��ЧӦ֮��Ĺ�ϵʽΪ��H4=______________�� ������N2O4����Ϊ����ƽ�������Ҫԭ��Ϊ______________________��
��4������Ϊ��Ԫ�����ˮ�еĵ��뷽ʽ�백���ƣ�������һ�����뷴Ӧ��ƽ�ⳣ��ֵΪ_____ ����֪��N2H4+H+N2H5+��K=8.7��107��Kw=1.0��10��14���������������γɵ���ʽ�εĻ�ѧʽΪ_______________��
��5��������һ�ֳ��õĻ�ԭ������װ������AgBr���Թ��м���������Һ���۲쵽��������_______________�� ���������ڴ�����ѹ��¯ˮ�е�������ֹ��¯����ʴ��������1kg�������ɳ�ȥˮ���ܽ��O2__________kg����ʹ��Na2SO3����ˮ���ܽ��O2��ȣ��������ŵ���________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ܱ������г���һ����NO2��������Ӧ2NO2(g) ![]() N2O4(g)����H����57 kJ�� mol��1�����¶�ΪT1��T2ʱ��ƽ����ϵ��NO2�����������ѹǿ�仯��������ͼ��ʾ������˵����ȷ����
N2O4(g)����H����57 kJ�� mol��1�����¶�ΪT1��T2ʱ��ƽ����ϵ��NO2�����������ѹǿ�仯��������ͼ��ʾ������˵����ȷ����
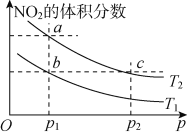
A. a��c����ķ�Ӧ���ʣ�a>c
B. a��b����NO2��ת���ʣ�a<b
C. a��c�����������ɫ��a�cdz
D. ��a�㵽b�㣬�����ü��ȵķ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������������Ҫ�Ĺ���Ԫ�ء�
��1����λ��Ԫ�����ڱ��õ�_____________�壬���̬ԭ����δ�ɶԵ��ӵĸ���Ϊ______��
��2��[Fe(H2NCONH2)]6(NO3)3�������������������غ���������һ����Ҫ�������û�������Fe3+�ĺ�������Ų�ʽΪ____________________�������ǽ���Ԫ�صĵ縺���ɴ�С��˳����____________________��
��3�����ط����С�̼ԭ��Ϊ________�ӻ��������ЦҼ���м�����Ŀ֮��Ϊ____________________��
��4��FeO������NaCl����ṹ���ƣ��Ƚ�FeO��NaCl�ľ����ܴ�С������Ҫ֪����������______��
��5��Co(NH3)5BrSO4���γ������ܵ������ṹ�ֱ�Ϊ[Co(NH3)5Br]SO4��[Co(SO4)(NH3)5]Br����֪Co3������λ����6��Ϊȷ���ܵ������Ľṹ���ֶ�����������������ʵ�飺�ڵ�һ���������Һ�м���������Һ������ɫ�������ڵڶ����������Һ�м�����������Һ��������ɫ��������ڶ�������������Ϊ____________________��
��6����������̼�ܽ��ڦã�Fe���γɵ�һ�ּ�϶�����壬���ԣ��侧��Ϊ���������ṹ������ͼ��ʾ��������ʵĻ�ѧʽΪ____________________���������ܶ�Ϊdg��cm3���������������̼ԭ�ӵľ���Ϊ____________________pm������٤��������ֵ��NA��ʾ��д����ļ���ʽ���ɣ���

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ʵ���У���ʹ�õ�װ�ã��г�װ���ԣ����Լ��Ͳ�����������������
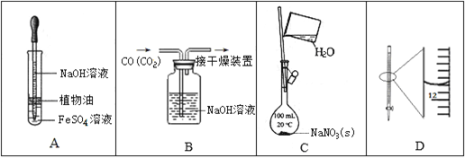
A. �۲�Fe(OH)2������
B. ��ȥCO�е�CO2
C. ����һ�����ʵ���Ũ�ȵ�NaNO3��Һ
D. 25 mL�ζ��ܶ���Ϊ11.80 mL
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������ɱ���ܱ������о�����1mol��A2��2mol��B2������Ӧ��A2(g)+2B2(g)![]() 2AB2(g) ��H��ά������������ѹǿ�ֱ�Ϊp1��p2���ڲ�ͬ�¶��´ﵽƽ�⣬���ƽ��ʱAB2������������¶ȵı仯��ͼ��ʾ��
2AB2(g) ��H��ά������������ѹǿ�ֱ�Ϊp1��p2���ڲ�ͬ�¶��´ﵽƽ�⣬���ƽ��ʱAB2������������¶ȵı仯��ͼ��ʾ��
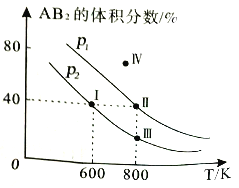
��֪:ͼ�Т������������ϣ�IV�㲻��������
����������ȷ����
A. ���͢�㷴Ӧ������� B. IV��ʱ��Ӧδ����ƽ��v(��)<v(��)
C. I��ʱ��A��ƽ��ת����Ϊ40% D. ����II����Ӧ������ȴ��600K���ɱ�ɵ�I
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com