
【题目】下列离子方程式中,正确的是 ( )
A. 稀硫酸滴在铁片上:2Fe+6H+===2Fe3++3H2↑
B. 碳酸氢钠溶液与稀盐酸混合:HCO3-+H+=H2O+CO2↑
C. 硫酸铜溶液与氢氧化钠溶液混合:CuSO4+2OH-===Cu(OH)2↓+![]()
D. 硝酸银溶液与氯化钠溶液混合:AgNO3+Cl-===AgCl↓+![]()
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】已知下列分子或离子在酸性条件下都能氧化KI,自身发生如下变化:H2O2→H2O IO![]() →I2 MnO
→I2 MnO![]() →Mn2+ HNO2→NO。如果分别用等物质的量的这些物质氧化足量的KI,得到I2最多的是( )
→Mn2+ HNO2→NO。如果分别用等物质的量的这些物质氧化足量的KI,得到I2最多的是( )
A. H2O2 B. HNO2 C. MnO![]() D. IO
D. IO![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】从含有CuCl2、FeCl2、FeCl3的工业废液中回收铜并制备氯化铁晶体的流程如下:
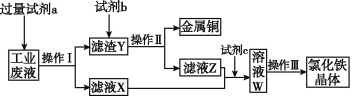
则下列说法正确的是
A. 试剂a是铁,试剂b是稀硫酸
B. 操作Ⅰ、操作Ⅱ、操作Ⅲ所用的仪器完全相同
C. 试剂c是氯气,反应的离子方程式为2Fe2++Cl2![]() 2Fe3++2Cl-
2Fe3++2Cl-
D. 用KSCN溶液可检验溶液W中是否有Fe2+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E、F六种物质有如下变化关系,E是淡黄色粉末,判断:

(1)写出A、B、C、D、E、F的化学式:
A._______;B.______;C.______;
D._______;E.______;F._______。
(2)写出有关反应的化学方程式(是离子反应的直接写出离子方程式)
E![]() B:______
B:______
C![]() F:______
F:______
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在标准状况下,将224L氯化氢气体完全溶于635mL的水(密度为1g/cm3)中,所得盐酸的密度为1.18g/cm3,该溶液中溶质的物质的量是多少__?该盐酸中溶质的质量分数是多少__?
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E五种烃分子中均含有8个氢原子,其中A、B常温下呈气态,C、D、E呈液态。请回答
(1)A是符合上述条件中相对分子质量最小的,则A的分子式为________;B属于链状单烯烃,且与HBr加成的产物只有一种,试写出B的结构简式________。
(2)C属于芳香烃,可用来制烈性炸药,试写出C制取烈性炸药的方程式_______________________________。
(3)已知E的结构简式为![]() 存在于煤焦油中,所有原子均处于同一平面内,则1mol E 最多能和___ mol的H2加成,写出E的所有一氯代物的结构简式_____________________________。
存在于煤焦油中,所有原子均处于同一平面内,则1mol E 最多能和___ mol的H2加成,写出E的所有一氯代物的结构简式_____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】粉煤灰是燃煤电厂的废渣,主要成分为SiO2、Al2O3、Fe2O3和C等。实验室模拟工业从粉煤灰提取活性Al2O3,其流程如下图:
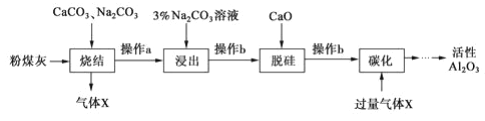
已知烧结过程的产物主要是NaAlO2、Ca2SiO4、NaFeO2和Na2SiO3等。
(1)写出烧结过程中铝元素转化的化学方程式___。
(2)操作 a 为冷却、研磨,其中研磨的目的是___。
(3)①浸出过程中, NaFeO 2 可完全水解,生成沉淀为___。
②3%Na2 CO3溶液显___(填 “酸性 ”、 “碱性 ”或“中性 ”),请用离子方程式解释:___。
(4)操作b 所用的玻璃仪器有漏斗、___、___。
(5)“碳化”时,通入过量气体 x 主要成分的化学式为___。
(6)工业上电解Al2O3制备 Al 是为使Al2O3在较低温下融化,通常加入___。电解过程中做阳极的石墨易消耗,原因是___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究人员最近发现了一种“水”电池,这种电池能利用淡水与海水之间含盐量差别进行发电,在海水中电池总反应可表示为:![]() ,下列“水”电池在海水中放电时的有关说法正确的是( )
,下列“水”电池在海水中放电时的有关说法正确的是( )
A. 负极反应式:![]()
B. ![]() 不断向“水”电池的正极移动
不断向“水”电池的正极移动
C. 每生成![]() 转移5 mol电子
转移5 mol电子
D. 该电池工作时,电子由![]() 电极向Ag电极移动
电极向Ag电极移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】目前人们正研究开发一种高能电池——钠硫电池,它以熔融的钠、硫为两极,以Na+导电的β″Al2O3陶瓷作固体电解质,反应为2Na+xS![]() Na2Sx。以下说法正确的是( )
Na2Sx。以下说法正确的是( )
A. 放电时,钠作正极,硫作负极
B. 放电时,Na+向负极移动
C. 充电时,钠极与外电源正极相连,硫极与外电源的负极相连
D. 放电时,负极发生的反应是:2Na-2e-===2Na+
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com