
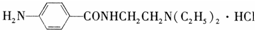 )俗称普鲁卡因胺,是一种常用的抗心律失常药物.纯品普鲁卡因胺为白色晶体,易溶于水,溶于乙醇,难溶于苯和乙醚.工业上生产普鲁卡因胺常用下列途径合成,其中B的化学式为SCl2.
)俗称普鲁卡因胺,是一种常用的抗心律失常药物.纯品普鲁卡因胺为白色晶体,易溶于水,溶于乙醇,难溶于苯和乙醚.工业上生产普鲁卡因胺常用下列途径合成,其中B的化学式为SCl2.
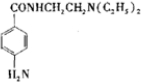 ,与盐酸发生可生成
,与盐酸发生可生成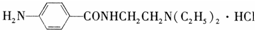 ,结合有机物的结构和性质以及题目要求解答该题.
,结合有机物的结构和性质以及题目要求解答该题. ,与盐酸发生可生成
,与盐酸发生可生成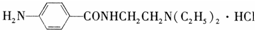 ,
, ,故答案为:还原反应;
,故答案为:还原反应; ;
; ,
,
 ,
,


 暑假作业暑假快乐练西安出版社系列答案
暑假作业暑假快乐练西安出版社系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A | B | C | D | E | F | |
| 主要化合价 | -1 | -3、+5 | -2、+6 | -1、+7 | +2 | +1、+2 |
| 原子半径nm | 0.071 | 0.11 | 0.102 | 0.099 | 0.197 | 0.117 |

查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 氧化剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、所加烧碱溶液的pH=13.0 |
| B、所得溶液中c(Mg2+)=5.6×10-10mol/L |
| C、所得溶液中c(H+)=1.0×10-13mol/L |
| D、所得溶液中由水电离产生的c(OH-)=1.0×10-13mol/L |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com