
| 5.76g |
| 64g/mol |
| 3 |
| 8 |
| 3 |
| 8 |
| 0.03mol |
| 0.1L |
| 2 |
| 3 |
| 8 |
| 3 |
| 0.06mol |
| 0.1L |
| 0.09mol |
| 0.1L |


科目:高中化学 来源: 题型:
| A、向两个相同的密闭容器中充入3He和O2,当它们的温度和密度都相同时,两种气体产生的压强不相等 | ||||
| B、3He的质量数为3,所以3He原子的近似相对原子质量为3 | ||||
C、
| ||||
| D、体积相同、密度相同的3He与HD具有相同的中子数 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 1 |
| 2 |
| 1 |
| 2 |
| 1 |
| 2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
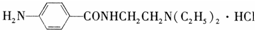 )俗称普鲁卡因胺,是一种常用的抗心律失常药物.纯品普鲁卡因胺为白色晶体,易溶于水,溶于乙醇,难溶于苯和乙醚.工业上生产普鲁卡因胺常用下列途径合成,其中B的化学式为SCl2.
)俗称普鲁卡因胺,是一种常用的抗心律失常药物.纯品普鲁卡因胺为白色晶体,易溶于水,溶于乙醇,难溶于苯和乙醚.工业上生产普鲁卡因胺常用下列途径合成,其中B的化学式为SCl2.
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
 请完成下列各题:第ⅢA、ⅤA元素组成的化合物GaN、GaP、GaAs等是人工合成的新型半导体材料,其晶体结构与金刚石相似.
请完成下列各题:第ⅢA、ⅤA元素组成的化合物GaN、GaP、GaAs等是人工合成的新型半导体材料,其晶体结构与金刚石相似.查看答案和解析>>
科目:高中化学 来源: 题型:
 “奥运会”严格禁止运动员服用兴奋剂.关于某种兴奋剂(结构简式如图)的以下说法中,正确的是( )
“奥运会”严格禁止运动员服用兴奋剂.关于某种兴奋剂(结构简式如图)的以下说法中,正确的是( )| A、该物质属于芳香烃 |
| B、该物质所有原子都在同一平面上 |
| C、该物质的分子式为C20H25O3 |
| D、1mol该物质最多能与7mol H2加成 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com