


科目:高中化学 来源: 题型:
A、再通入少量氯气,
| ||
| B、加入少量固体NaOH,一定有c(Na+)═c(Cl-)+c(ClO-) | ||
| C、加入少量水,水的电离平衡向右移动 | ||
| D、通入少量SO2,溶液漂白性增强 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、氢氧化镁中滴加盐酸:H++OH-═H2O | ||||
| B、用FeCl3溶液腐蚀铜电路板:Fe3++Cu═Fe2++Cu2+ | ||||
| C、在硫酸氢钾溶液中加入氢氧化钡溶液至pH=7:H++SO42-+Ba2++OH-═BaSO4↓+H2O | ||||
D、NH4HCO3溶液中加入过量NaOH溶液并加热:NH4++HCO3-+2OH-
|
查看答案和解析>>
科目:高中化学 来源: 题型:
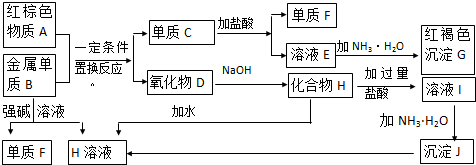
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
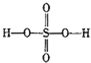 过硫酸:
过硫酸: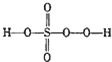
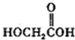 (b)
(b)  (c)H2O2(d)
(c)H2O2(d) 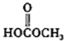 (e)
(e)  (f)
(f)  (g)O3(h)
(g)O3(h) 
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com