
 在2010年12月初农兴中学顺利接受省级示范高中验收期间,学校租用了大量盆栽鲜花装扮校园.为保证鲜花盛开,这些盆栽鲜花都施用了S-诱抗素剂,S-诱抗素的分子结构如图,下列关于该分子说法正确的是( )
在2010年12月初农兴中学顺利接受省级示范高中验收期间,学校租用了大量盆栽鲜花装扮校园.为保证鲜花盛开,这些盆栽鲜花都施用了S-诱抗素剂,S-诱抗素的分子结构如图,下列关于该分子说法正确的是( )| A. | S-诱抗素含有苯环、羟基、羰基、羧基 | |
| B. | S-诱抗素能与NaHCO3反应放出CO2 | |
| C. | S-诱抗素的分子式为C14H20O4 | |
| D. | 1molS-诱抗素在一定条件下可分别与4molH2、2molNaOH发生反应 |
分析 该物质中含有羰基、碳碳双键、醇羟基、羧基,具有酮、烯烃、醇、羧酸的性质,能发生加成反应、还原反应、加聚反应、取代反应、酯化反应等,据此分析解答.
解答 解:A.根据图知,该分子中不含苯环,故A错误;
B.羧基能和碳酸氢钠反应生成二氧化碳,故B正确;
C.根据结构简式知,分子式为C15H20O4,故C错误;
D.碳碳双键和羰基能和氢气发生加成反应,只有羧基能和氢氧化钠反应,所以1molS-诱抗素在一定条件下可分别与4molH2、1molNaOH发生反应,故D错误;
故选B.
点评 本题考查有机物结构和性质,明确官能团及其性质关系是解本题关键,侧重考查酚、烯烃、羧酸的性质,易错选项是A,注意该物质中不含苯环.


科目:高中化学 来源: 题型:解答题
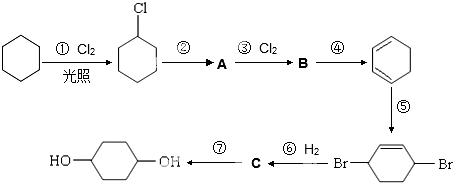
 ;
;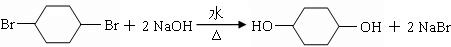 .
.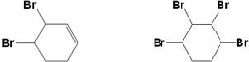 .
.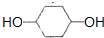 +O2$→_{△}^{催化剂}$
+O2$→_{△}^{催化剂}$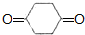 +2H2O.
+2H2O.查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 只有①③④ | B. | 只有②⑤⑥ | C. | 只有①③④⑥ | D. | 只有①③④⑤⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| a | 原子核外电子分别占3个不同能级,且每个能级上排布的电子数相同 |
| b | 基态原子的p轨道电子数比s轨道电子数少1 |
| c | 在周期表所列元素中电负性最大 |
| d | 位于周期表中第4纵行 |
| e | 基态原子M层全充满,N层只有一个电子 |
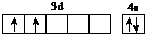 .
.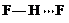 、
、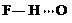 、
、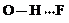 、
、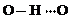 任意一种.
任意一种.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
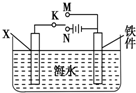 对钢铁制品进行抗腐蚀处理,可适当延长其使用寿命.
对钢铁制品进行抗腐蚀处理,可适当延长其使用寿命.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 ,B的结构简式
,B的结构简式 或
或 .
. ,反应类型:取代反应.
,反应类型:取代反应.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com