
用NA表示阿伏加德罗常数。下列叙述正确的是( )
A.28 g CO与N2的混合气体所占的体积约是22.4 L
B.已知2SO2(g)+O2(g) 2SO3(g) ΔH=-a kJ·mol-1,若将2NA个SO2与NA个O2混合充分反应放出a kJ的热量
2SO3(g) ΔH=-a kJ·mol-1,若将2NA个SO2与NA个O2混合充分反应放出a kJ的热量
C.由CO2和O2组成的混合物中共有NA个分子,其中的氧原子数为2NA
D.25 ℃时,pH=13的1.0 L Ba(OH)2溶液中含有的OH-数目为0.2NA
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:2014年化学高考总复习课时演练 11-4化学实验方案设计与评价练习卷(解析版) 题型:填空题
亚硫酸钠中的+4价硫,既有氧化性,又有还原性。现有试剂:溴水、Na2S溶液、 Na2SO3溶液、稀硫酸、NaOH溶液、氨水。
(1)要证明Na2SO3具有还原性,应选用的试剂有_____,看到的现象是___________________________________。
反应的离子方程式为:_______________________。
(2)要证明Na2SO3具有氧化性,应选用的试剂有_____,看到的现象是___________________________________。
反应的离子方程式为:_______________________。
查看答案和解析>>
科目:高中化学 来源:2014年化学高考总复习课时演练 11-1化学实验仪器和基本操作练习卷(解析版) 题型:选择题
下列实验操作中,仪器需插入液面以下的有( )
①制备Fe(OH)2,用胶头滴管将NaOH溶液滴入FeSO4溶液中;
②制备氢气,简易装置中长颈漏斗的下端管口;
③分馏石油时,测量温度所用的温度计;
④将氯气溶于水时输送氯气的导气管;
⑤用水吸收氨气时的导气管;
⑥用胶头滴管向试管中的BaCl2溶液中滴加稀硫酸
A.①②④ B.①③⑤
C.③⑤⑥ D.②③④
查看答案和解析>>
科目:高中化学 来源:2014年化学高考总复习课时演练 1-2物质的量在实验中的应用练习卷(解析版) 题型:选择题
把V L含有MgSO4和K2SO4的混合溶液分成两等份,一份加入含a mol NaOH的溶液,恰好使镁离子完全沉淀为氢氧化镁;另一份加入含b mol BaCl2的溶液,恰好使硫酸根离子完全沉淀为硫酸钡。则原混合溶液中钾离子的浓度为( )
A.(b-a)/V mol·L-1 B.(2b-a)/V mol·L-1
C.2(b-a)/V mol·L-1 D.2(2b-a)/V mol·L-1
查看答案和解析>>
科目:高中化学 来源:2014年化学高考总复习课时演练 1-1物质的量 气体摩尔体积练习卷(解析版) 题型:填空题
物质的量是高中化学中常用的物理量,请完成以下有关其内容的计算。
(1)0.2 g H2含有个______H原子。
(2)标准状况下,含有相同氧原子数的CO与CO2的体积之比为______。
(3)100 mL 某Al2(SO4)3溶液中,n(Al3+)=0.20 mol,则其中c( )= ______mol/L。
)= ______mol/L。
(4)在9.5 g某二价金属的氯化物中含0.2 mol Cl-,此氯化物的摩尔质量为______;该金属元素的相对原子质量为______。
(5)标准状况下6.72 L CO与一定量的 Fe2O3恰好完全反应(生成Fe和CO2)后,剩余固体的质量为______g。
查看答案和解析>>
科目:高中化学 来源:2014年化学高考总复习课时演练 1-1物质的量 气体摩尔体积练习卷(解析版) 题型:选择题
下列关于物质的量、摩尔质量的叙述正确的是( )
A.0.012 kg 12C中含有约6.02×1023个碳原子
B.1 mol H2O中含有2 mol氢和1 mol氧
C.氢氧化钠的摩尔质量是40 g
D.2 mol水的摩尔质量是1 mol水的摩尔质量的2倍
查看答案和解析>>
科目:高中化学 来源:2014年化学高考总复习单元检测 第四章非金属及其化合物练习卷(解析版) 题型:选择题
下列反应的离子方程式正确的是( )
A.足量的溴化亚铁和少量的氯气反应:2Fe2++Cl2=2Fe3++2Cl-
B.亚硫酸氢铵和氢氧化钠的反应: +OH-
+OH-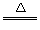 NH3↑+H2O
NH3↑+H2O
C.二氧化硫气体通入过量的Ca(ClO)2溶液中:SO2+H2O+Ca2++2ClO-=CaSO3↓+2HClO
D.Ca(HCO3)2溶液与少量NaOH溶液反应:
查看答案和解析>>
科目:高中化学 来源:2014年化学高考总复习单元检测 第十、十一章有机、实验练习卷(解析版) 题型:实验题
某同学设计了以下流程来检验碳酸钠粉末中可能含有少量氯化钠和氢氧化钠中的一种或两种杂质。

(1)步骤1所需玻璃仪器是______;步骤3的操作名称是______。
(2)对检验碳酸钠粉末中可能含有的杂质提出合理假设:
假设1:只含有氯化钠;
假设2:只含有___________;
假设3:氯化钠和氢氧化钠都含有。
(3)设计实验方案,进行实验。
限选以下试剂:氯化钡溶液、硝酸钡溶液、酚酞试液、稀硝酸、稀盐酸、稀硫酸、硝酸银溶液。回答下列问题:
①加入过量试剂A的名称是______。
②填写下表:
实验步骤 | 预期现象和结论 |
步骤4: |
|
步骤5: |
|
查看答案和解析>>
科目:高中化学 来源:2014年化学高考总复习单元检测 第八章水溶液中的离子平衡练习卷(解析版) 题型:填空题
弱电解质电离情况可以用电离度和电离平衡常数表示,表1是常温下几种弱酸的电离平衡常数(Ka)和弱碱的电离平衡常数(Kb),表2是常温下几种难(微)溶物的溶度积常数(Ksp)。
表1

表2

请回答下面问题:
(1)CH3COONH4的水溶液呈 (选填“酸性”、“中性”或“碱性”),理由是 。溶液中各离子浓度大小关系是 。
(2)物质的量之比为1∶1的NaCN和HCN的混合溶液,其pH>7,该溶液中离子浓度从大到小的排列为 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com