
ΓΨΧβΡΩΓΩΡ≥«ΩΥα–‘»ή“ΚXΘ§Ω…ΡήΚ§”–Al3+ΓΔBa2+ΓΔNH4+ΓΔFe2+ΓΔNa+ΓΔCO32©¹ΓΔSO42©¹ΓΔSiO32©¹ΓΔNO3©¹÷–ΒΡ“Μ÷÷ΜρΦΗ÷÷άκΉ”Θ§»ΓΗΟ»ή“ΚΫχ–– Β―ιΘ§Τδœ÷œσΦΑΉΣΜ·»γœ¬ΆΦΥυ ΨΓΘ

«κΜΊ¥πœ¬Ν–Έ ΧβΘΚ
(1)”…’ϊΧεΒΡ Β―ιΙΐ≥ΧΩ…≈–Εœ»ή“ΚX÷–“ΜΕ®≤Μ¥φ‘ΎΒΡ“θάκΉ””–______ΓΘ
(2)≤ζ…ζΤχΧεAΒΡάκΉ”ΖΫ≥Χ ΫΈΣ____________ΓΘ
(3)‘Ύ Β―ι “÷– ’Φ·ΤχΧεAΘ§Ω…―Γ‘ώ»γΆΦΉΑ÷Ο÷–ΒΡ______ΓΘ
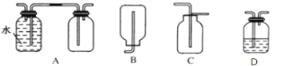
(4)–¥≥ωΔήΖ¥”Π÷–…ζ≥…»ή“ΚHΒΡάκΉ”ΖΫ≥Χ Ϋ____________ΓΘ
(5)Ε‘≤ΜΡή»ΖΕ® «Ζώ¥φ‘ΎΒΡάκΉ”Θ§«κΦρ ωΦλ≤β Β―ιΖΫΑΗ__________ΓΘ
ΓΨ¥πΑΗΓΩCO32-ΓΔSiO32-ΓΔNO3- 3Fe2++4H+ +NO3-=3Fe3++NOΓϋ+2H2O A Al3++ 4OH-=AlO2- + 2H2O ”ΟΫύΨΜ≤§ΥΩ’Κ»Γ ‘―υ‘ΎΜπ―φ…œΉΤ…’Θ§Ιέ≤λΜπ―φ―’…ΪΘ§»τΈΣΜΤ…ΪΘ§‘ρΥΒΟς”–Na+ΘΜ»τΈόΜΤ…ΪΘ§‘ρΈόNa+ΓΘ
ΓΨΫβΈωΓΩ
(1)»ή“ΚX≥ «ΩΥα–‘Θ§”…”ΎH+”κCO32©¹ΓΔSiO32©¹ΜαΖΔ…ζΖ¥”ΠΘ§≤ΜΡή¥σΝΩΙ≤¥φΘ§Υυ“‘≤ΜΚ§CO32-ΓΔSiO32-ΘΜ»ή“Κ”κBa(NO3)2ΜλΚœ…ζ≥…≥ΝΒμCΘ§‘ρΥΒΟς»ή“Κ÷–Κ§SO42-Θ§‘ρ»ή“Κ÷–≤ΜΚ§”κSO42-Ζ¥”Π–Έ≥…≥ΝΒμΒΡBa2+Θ§≥ΝΒμC «BaSO4ΘΜΦ”»κBa(NO3)2»ή“Κ≤ζ…ζΤχΧεAΘ§ΥΒΟςΚ§”–ΜΙ‘≠–‘άκΉ”Fe2+ΘΜ‘ΎΥα–‘ΧθΦΰœ¬NO3-ΨΏ”–«Ω―θΜ·–‘Θ§Υυ“‘»ή“Κ÷–Fe2+”κNO3-≤ΜΡήΙ≤¥φΘ§»ή“Κ÷–≤ΜΚ§NO3-ΘΜΤχΧεA «NOΘ§NO”κO2Ζ¥”Π≤ζ…ζΒΡΤχΧεD «NO2ΘΜNO2ΓΔO2ΓΔΥ°Ζ¥”Π≤ζ…ζΒΡ»ή“ΚE «œθΥαΘΜ»ή“ΚBΦ”»κΙΐΝΩNaOH»ή“Κ≤ζ…ζΤχΧεFΘ§F «NH3Θ§‘ρ»ή“Κ÷–Κ§NH4+ΘΜœθΥα”κΑ±ΤχΖ¥”Π≤ζ…ζœθΥαοßΘ§Υυ“‘I «NH4NO3ΘΜ”…”Ύ»ή“ΚB÷–Κ§”–Fe2+―θΜ·≤ζ…ζΒΡFe3+Θ§Υυ“‘≤ζ…ζΒΡ≥ΝΒμG «Fe(OH)3Θ§Fe(OH)3”κ―ΈΥαΖ¥”Π≤ζ…ζΒΡJ «FeCl3ΘΜ»ή“ΚH÷–Ά®»κΙΐΝΩΕΰ―θΜ·ΧΦΤχΧεΘ§≤ζ…ζ≥ΝΒμΘ§‘ρ»ή“Κ÷–Κ§”–Al3+Θ§≥ΝΒμK «Al(OH)3Θ§»ή“ΚL «NaHCO3ΓΘ
(1)”…’ϊΧεΒΡ Β―ιΙΐ≥ΧΩ…≈–Εœ»ή“ΚX÷–“ΜΕ®≤Μ¥φ‘ΎΒΡ“θάκΉ””–CO32-ΓΔSiO32-ΓΔNO3-ΘΜ
(2)‘ΎΥα–‘ΧθΦΰœ¬Θ§Fe2+ΓΔNO3-ΓΔH+ΖΔ…ζ―θΜ·ΜΙ‘≠Ζ¥”ΠΘ§≤ζ…ζFe3+Θ§NO3-±ΜΜΙ‘≠≤ζ…ζNOΘ§Ά§ ±”–Υ°…ζ≥…Θ§Ζ¥”ΠΒΡάκΉ”ΖΫ≥Χ ΫΈΣ3Fe2++4H+ +NO3- =3Fe3++NOΓϋ+2H2OΘΜ
(3)ΤχΧεA «NOΘ§ΗΟΤχΧε»ί“Ή”κΩ’Τχ÷–ΒΡ―θΤχΖ¥”Π…ζ≥…NO2Θ§Υυ“‘≤ΜΡή”Ο≈≈Ω’ΤχΖΫΖ® ’Φ·Θ§÷ΜΡή”Ο≈≈Υ°ΖΫΖ® ’Φ·Θ§Κœάμ―Γœν «AΘΜ
(4)Δή÷–Al3+”κΙΐΝΩOH-Ζ¥”Π…ζ≥…AlO2-ΚΆΥ°Θ§άκΉ”ΖΫ≥Χ ΫΈΣΘΚAl3++ 4OH- =AlO2-+2H2OΘΜ
(5)Ά®Ιΐ«ΑΟφΖ÷ΈωΩ…÷ΣΘΚ‘Ύ‘≠»ή“Κ÷–“ΜΕ®Κ§”–Al3+ΓΔFe2+ΓΔNH4+ΓΔSO42-ΘΜ“ΜΕ®≤ΜΚ§”–Ba2+ΓΔCO32-ΓΔSiO32-ΓΔNO3-ΘΜ≤ΜΡή»ΖΕ®ΒΡάκΉ” «Na+ΘΜΕ‘”ΎNa+Θ§Φλ≤βΥϋΒΡ Β―ιΖΫΑΗ «”ΟΫύΨΜ≤§ΥΩ’Κ»Γ ‘―υ‘ΎΜπ―φ…œΉΤ…’Θ§Ιέ≤λΜπ―φ―’…ΪΘ§»τΈΣΜΤ…ΪΘ§‘ρΥΒΟς”–Na+ΘΜ»τΈόΜΤ…ΪΘ§‘ρΈόNa+ΓΘ



| ΡξΦΕ | ΗΏ÷–ΩΈ≥Χ | ΡξΦΕ | ≥θ÷–ΩΈ≥Χ |
| ΗΏ“Μ | ΗΏ“ΜΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ | ≥θ“Μ | ≥θ“ΜΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ |
| ΗΏΕΰ | ΗΏΕΰΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ | ≥θΕΰ | ≥θΕΰΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ |
| ΗΏ»ΐ | ΗΏ»ΐΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ | ≥θ»ΐ | ≥θ»ΐΟβΖ―ΩΈ≥ΧΆΤΦωΘΓ |
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩΆ§Έ¬Ά§―Ιœ¬Θ§Ά§ΧεΜΐΒΡΦΉΓΔ““ΝΫ÷÷ΤχΧεΒΡ÷ ΝΩ±» «17:14ΓΘ»τΦΉΤχΧε «H2SΘ§‘ρ““ΤχΧε≤ΜΩ…Ρή «( )
A.N2B.HClC.C2H4D.CO
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩ“―÷ΣFe3O4 «“Μ÷÷Η¥‘”ΒΡΜ·ΚœΈοΘ§ΤδΜ·―ß ΫΩ…ΗΡ–¥ΈΣFeOΓΛFe2O3ΓΘΕ‘”ΎA÷–…ζ≥…ΒΡΚΎ…ΪΈο÷ Θ§”–»ΐΗω―ßœΑ–ΓΉιΧα≥ωΝΥ»ΐ÷÷≤ΜΆ§ΒΡ≤¬œκΘ§“‘œ¬ «–ΓΉιΆ§―ßΫχ––ΒΡ Β―ι≤¬œκ”κΧΫΨΩΘ§«κΡψΗυΨί–ΓΉιΒΡΥΦ¬Ζ”κΧα ΨΆξ≥…œύΙΊΩ’ΑΉΓΘ
Θ®≤¬œκΘ©ΦΉΉιΘΚΚΎ…ΪΈο÷ «FeO
““ΉιΘΚΚΎ…ΪΈο÷ «Fe3O4
±ϊΉιΘΚ_____________ΘΜ
Θ® Β―ιΧΫΨΩΘ©
(1)±ϊΉι»œΈΣ“Μ÷÷ΦρΒΞΕ®–‘ΒΡΖΫΖ®Φ¥Ω…≈–ΕœΦΉΉιΒΡ’ΐΈσΘΚ»ΓA÷–…ζ≥…ΒΡΚΎ…ΪΈο÷ …Ό–μ”Ύ…’±≠Θ§Φ”œΓ―ΈΥα ΙΤδΆξ»Ϊ»ήΫβΘ§‘ΌΦ”______»ή“Κ“‘Φλ―ιFe3ΘΪΘ§Ιέ≤λΒΫ»ή“Κ”–Έό≥ωœ÷_________œ÷œσΦ¥Ω…≈–ΕœΓΘ
(2)““Ήι»œΈΣΩ…Ά®ΙΐΕ®ΝΩ≤βΕ®ά¥»ΖΕ®A÷–…ζ≥…ΒΡΚΎ…ΪΈο÷ ΒΡΉι≥…Θ§“‘―ι÷ΛΗΟΉι≤¬œκ’ΐ»ΖΓΘ»ΓA÷–…ζ≥…ΒΡΚΎ…ΪΈο÷ 2.32g»ήΫβ”Ύ ΝΩœΓ―ΈΥαΚσΘ§Φ”»κ–¬÷Τ¬»Υ°Θ§Φ”»κ¬»Υ°ΚσΖ¥”ΠΒΡάκΉ”ΖΫ≥Χ ΫΈΣΘΚ_____________Θ§‘ΌΦ”»κΉψΝΩNaOH»ή“ΚΚσΘ§Ιΐ¬Υœ¥Β”ΚφΗ…ΉΤ…’≥ΤΝΩΘ§»τ≥ΤΒΟΙΧΧε÷ ΝΩΈΣ________Θ§Φ¥Ω…≈–Εœ““ΉιΆ§―ß≤¬œκ’ΐ»ΖΓΘ
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩ“―÷ΣΖ¥”ΠKClO3 + 6HCl= 3Cl2Γϋ+KCl + 3H2OΘ§œ¬Ν–”–ΙΊΒΡΥΒΖ®÷–Θ§’ΐ»ΖΒΡ «Θ® Θ©
A. HCl ÷–ΒΡCl »Ϊ≤Ω±Μ―θΜ· B. ßΒγΉ”ΒΡ¬»‘≠Ή” «ΒΟΒγΉ”ΒΡ¬»‘≠Ή”ΒΡ5±Ε
C. Ζ¥”Π÷–”–6molΒγΉ”ΖΔ…ζΉΣ“Τ D. Ζ¥”Π÷–KClO3 ±Μ―θΜ·
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩœ¬Ν–ΗςΉιΈο÷ œύΜΞΖ¥”ΠΚσΘ§ΟΜ”–Φν…ζ≥…ΒΡ « Θ® Θ©
A. Na2O2»ή”ΎΥ° B. Κλ»»ΒΡΧζΚΆΥ°’τΤχ
C. Ϋπ τΡΤΆΕ»κΥ°÷– D. Na2OΆΕ»κΥ°÷–
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩΡ≥Μ·―ß–Υ»Λ–ΓΉι÷Τ»Γ¬»ΥαΦΊΚΆ¬»Υ°≤ΔΫχ––”–ΙΊΧΫΨΩ Β―ιΓΘ
Β―ι“Μ ÷Τ»Γ¬»ΥαΦΊΚΆ¬»Υ°
άϊ”Οœ¬ΆΦΥυ ΨΒΡ Β―ιΉΑ÷ΟΫχ–– Β―ιΓΘ
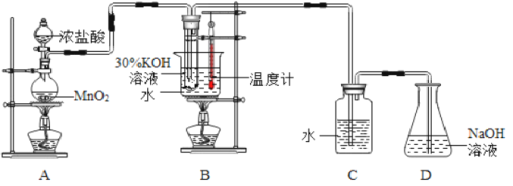
(1)÷Τ»Γ Β―ιΫα χΚσΘ§»Γ≥ωB÷– ‘Ιήά以ΫαΨßΘ§Ιΐ¬ΥΘ§œ¥Β”ΓΘΙΐ¬Υ≤ΌΉςΙΐ≥Χ÷––η“ΣΒΡ≤ΘΝß“«Τς”–__________ΓΘ
(2)»τΕ‘ΒςBΚΆCΉΑ÷ΟΒΡΈΜ÷ΟΘ§_____Θ®ΧνΓΑΡήΓ±ΜρΓΑ≤ΜΡήΓ±Θ©ΧαΗΏB÷–¬»ΥαΦΊΒΡ≤ζ¬ ΓΘDΉΑ÷ΟΒΡΉς”Ο «___________________ΓΘ
(3)‘Ύ Β―ιΙΐ≥Χ÷–Θ§»τ“ΣΦλ―ιCΉΑ÷ΟΒΡΤΩ»ϊ¥Π «ΖώΟήΖβΚΟΘ§«κΦρ ωΜ·―ßΦλ―ιΖΫΑΗ_______ΓΘ
Β―ιΕΰ ¬»ΥαΦΊ”κΒβΜ·ΦΊΖ¥”ΠΒΡ―–ΨΩ
(4)‘Ύ≤ΜΆ§ΧθΦΰœ¬KClO3Ω…ΫΪKI―θΜ·ΈΣI2ΜρKIO3Θ°ΗΟ–ΓΉι…ηΦΤΝΥœΒΝ– Β―ι―–ΨΩΖ¥”ΠΧθΦΰΕ‘Ζ¥”Π≤ζΈοΒΡ”ΑœλΘ§Τδ÷–œΒΝ–a Β―ιΒΡΦ«¬Φ»γœ¬Θ® Β―ι‘Ύ “Έ¬œ¬Ϋχ––Θ©ΘΚ
‘Ιή±ύΚ≈ | 1 | 2 | 3 | 4 |
0.2molL©¹1KI/mL | 1.0 | 1.0 | 1.0 | 1.0 |
KClO3Θ®sΘ©/g | 0.10 | 0.10 | 0.10 | 0.10 |
6.0molL©¹1H2SO4/mL | 0 | 3.0 | 6.0 | 9.0 |
’τΝσΥ°/mL | 9.0 | 6.0 | 3.0 | 0 |
Β―ιœ÷œσ |
ΔΌœΒΝ–a Β―ιΒΡ Β―ιΡΩΒΡ «___________________________ΓΘ
ΔΎ…ηΦΤ1Κ≈ ‘Ιή Β―ιΒΡΉς”Ο «__________________________ΓΘ
Δέ»τ2Κ≈ ‘Ιή Β―ιœ÷œσΈΣ"ΜΤ…Ϊ»ή“Κ",»Γ…ΌΝΩΗΟ»ή“ΚΦ”»κΒμΖέ»ή“Κœ‘άΕ…Ϊ;ΦΌ…η―θΜ·≤ζΈοΈ®“Μ,ΜΙ‘≠≤ζΈοΈΣKCl,‘ρ¥ΥΖ¥”ΠΒΡάκΉ”ΖΫ≥Χ ΫΈΣ__________________________ΓΘ
p> Β―ι»ΐ ≤βΕ®±ΞΚΆ¬»Υ°÷–¬»‘ΣΥΊΒΡΉήΝΩ(5)ΗυΨίœ¬Ν–Ή ΝœΘ§ΈΣΗΟ–ΓΉι…ηΦΤ“ΜΗωΩ…––ΒΡ Β―ιΖΫΑΗΘ®≤Μ±ΊΟη ω≤ΌΉςΙΐ≥ΧΒΡœΗΫΎΘ©ΘΚ____ΓΘ
Ή ΝœΘΚiΘ°¥Έ¬»ΥαΜαΤΤΜΒΥαΦν÷Η ΨΦΝΘΜ
iiΘ°¥Έ¬»ΥαΜρ¬»ΤχΩ…±ΜSO2ΓΔH2O2ΚΆFeCl2Β»Έο÷ ΜΙ‘≠≥…Cl©¹ΓΘ
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩΘ®1Θ©“―÷ΣH2Θ®gΘ©ΓΔCOΘ®gΘ©ΚΆCH3OHΘ®lΘ©ΒΡ»Φ…’»»ΓςHΖ÷±πΈΣ-285.8kJΓΛmol-1ΓΔ-283.0kJΓΛmol-1ΚΆ-726.5kJΓΛmol-1ΓΘΡ«Ο¥”ΟΧΪ―τΡήΖ÷Ϋβ10molΥ°œϊΚΡΒΡΡήΝΩ «____________kJΘΜ
Θ®2Θ©”…Κœ≥…ΤχΘ®Ήι≥…ΈΣH2ΓΔCOΚΆ…ΌΝΩΒΡCO2Θ©÷±Ϋ”÷Τ±ΗΕΰΦΉΟ―Θ§Τδ÷–ΒΡ÷ς“ΣΙΐ≥ΧΑϋά®“‘œ¬ΥΡΗωΖ¥”ΠΘΚ
ΦΉ¥ΦΚœ≥…Ζ¥”ΠΘΚ
Θ®iΘ©CO(g) + 2H2(g) = CH3OH(g) ΓςH1 = -90.1kJmol-1
Θ®iiΘ©CO2(g) + 3H2(g) = CH3OH(g) + H2O(g) ΓςH2 = -49.0kJmol-1
Υ°ΟΚΤχ±δΜΜΖ¥”ΠΘΚ
Θ®iiiΘ©CO(g) + H2O(g) = CO2(g) + H2 (g) ΓςH3 = -41.1kJmol-1
ΕΰΦΉΟ―Κœ≥…Ζ¥”ΠΘΚ
Θ®iVΘ©2 CH3OH(g) = CH3OCH3(g) + H2O(g) ΓςH4 = -24.5kJmol-1
‘ρ”…H2ΚΆCO÷±Ϋ”÷Τ±ΗΕΰΦΉΟ―Θ®Νμ“Μ≤ζΈοΈΣΥ°’τΤχΘ©ΒΡ»»Μ·―ßΖΫ≥Χ ΫΈΣ____________ΓΘ
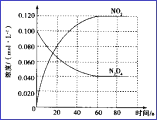
Θ®3Θ©‘Ύ»ίΜΐΈΣ1.00LΒΡ»ίΤς÷–Θ§Ά®»κ“ΜΕ®ΝΩN2O4Θ§ΖΔ…ζN2O4(g) ![]() 2NO2(g), 100Γφ ±Θ§ΧεœΒ÷–ΗςΈο÷ ≈®Ε»Υφ ±Φδ±δΜ·»γΆΦΥυ ΨΓΘ‘Ύ0ΓΪ60s ±ΕΈΘ§v(N2O4)=_______________________Θ§
2NO2(g), 100Γφ ±Θ§ΧεœΒ÷–ΗςΈο÷ ≈®Ε»Υφ ±Φδ±δΜ·»γΆΦΥυ ΨΓΘ‘Ύ0ΓΪ60s ±ΕΈΘ§v(N2O4)=_______________________Θ§
Θ®4Θ©“―÷ΣΖ¥”Π2HIΘ®gΘ©=H2(g) + I2(g)ΒΡΠΛH= +11kJΓΛmol-1Θ§1molH2Θ®gΘ©ΓΔ1mol I2Θ®gΘ©Ζ÷Ή”÷–Μ·―ßΦϋΕœΝ― ±Ζ÷±π–η“ΣΈϋ ’436kJΓΔ151kJΒΡΡήΝΩΘ§‘ρ1molHIΘ®gΘ©Ζ÷Ή”÷–Μ·―ßΦϋΕœΝ― ±–ηΈϋ ’ΒΡΡήΝΩΈΣ___________kJΓΘ‘Ύ716K ±Θ§ΤχΧεΜλΚœΈο÷–ΒβΜ·«βΒΡΈο÷ ΒΡΝΩΖ÷ ΐx(HI)”κΖ¥”Π ±ΦδtΒΡΙΊœΒ»γœ¬±μ
t/min | 0 | 20 | 40 | 60 | 80 | 120 |
x(HI) | 1 | 0.91 | 0.85 | 0.815 | 0.795 | 0.784 |
…œ ωΖ¥”Π÷–Θ§’ΐΖ¥”ΠΥΌ¬ ΈΣv’ΐ= k’ΐΓΛx2(HI)Θ§ΡφΖ¥”ΠΥΌ¬ ΈΣvΡφ=kΡφΓΛx(H2)ΓΛx(I2)Θ§Τδ÷–k’ΐΓΔkΡφΈΣΥΌ¬ ≥Θ ΐΘ§ »τk’ΐ = 0.0027min-1Θ§‘Ύt=40min ±Θ§v’ΐ=_______min-1
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩ Β―ι “≥Θάϊ”Ο“‘œ¬Ζ¥”Π÷Τ»Γ…ΌΝΩΒΣΤχΘΚNaNO2+NH4Cl![]() NaCl+N2Γϋ+2H2OΘΜΙΊ”ΎΗΟΖ¥”ΠΒΡœ¬Ν–ΥΒΖ®≤Μ’ΐ»ΖΒΡ «( )
NaCl+N2Γϋ+2H2OΘΜΙΊ”ΎΗΟΖ¥”ΠΒΡœ¬Ν–ΥΒΖ®≤Μ’ΐ»ΖΒΡ «( )
A. Na2NO2 «―θΜ·ΦΝΘ§NH4Cl «‘≠ΦΝ
B. N2Φ» «―θΜ·≤ζΈοΘ§”÷ «ΜΙ‘≠≤ζΈο
C. NH4Cl÷–ΒΣ‘ΣΥΊ±ΜΜΙ‘≠
D. ΟΩ…ζ≥…1molN2ΉΣ“ΤΒγΉ”ΒΡΈο÷ ΒΡΝΩΈΣ3mol
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΩΤΡΩΘΚΗΏ÷–Μ·―ß ά¥‘¥ΘΚ Χβ–ΆΘΚ
ΓΨΧβΡΩΓΩΒ¬Ιζ÷ΊάκΉ”―–ΨΩ÷––Ρ2010Ρξ2‘¬19»’–ϊ≤ΦΘ§”…ΗΟ÷––Ρ»ΥΙΛΚœ≥…ΒΡΒΎll2Κ≈Μ·―ß‘ΣΥΊ¥”Φ¥»’ΤπΜώ’ΐ ΫΟϊ≥ΤΓΑCopemiciumΓ±Θ§œύ”ΠΒΡ‘ΣΥΊΖϊΚ≈ΈΣΓΑCnΓ±ΓΘΗΟ‘ΣΥΊΒΡΟϊ≥Τ «ΈΣΝΥΦΆΡν÷χΟϊΧλΈΡ―ßΦ“ΗγΑΉΡαΕχΒΟΟϊΓΘΗΟ÷––Ρ»ΥΙΛΚœ≥…CnΒΡΙΐ≥ΧΩ…±μ ΨΈΣΘΚ7030Zn+20882PbΓζ277112Cn+10nΓΘœ¬Ν––π ω÷–’ΐ»ΖΒΡ « Θ® Θ©
A. …œ ωΚœ≥…Ιΐ≥Χ τ”ΎΜ·―ß±δΜ·
B. Cn‘ΣΥΊΈΜ”Ύ‘ΣΥΊ÷ήΤΎ±μΒΡΒΎΤΏ÷ήΤΎΘ§ «Η±Ήε‘ΣΥΊ
C. Cn‘ΣΥΊΒΡœύΕ‘‘≠Ή”÷ ΝΩΈΣ277
D. 277112CnΒΡ‘≠Ή”ΚΥΡΎ÷ Ή” ΐ±»÷–Ή” ΐΕύ53
≤ιΩ¥¥πΑΗΚΆΫβΈω>>
ΙζΦ ―ß–Θ”≈―Γ - ΝΖœΑ≤αΝ–±μ - ‘ΧβΝ–±μ
Κΰ±± ΓΜΞΝΣΆχΈΞΖ®ΚΆ≤ΜΝΦ–≈œΔΨΌ±®ΤΫΧ® | Άχ…œ”–ΚΠ–≈œΔΨΌ±®Ή®«χ | Βγ–≈’©Τ≠ΨΌ±®Ή®«χ | …φάζ Ζ–ιΈό÷ς“ε”–ΚΠ–≈œΔΨΌ±®Ή®«χ | …φΤσ«÷»®ΨΌ±®Ή®«χ
ΈΞΖ®ΚΆ≤ΜΝΦ–≈œΔΨΌ±®ΒγΜΑΘΚ027-86699610 ΨΌ±®” œδΘΚ58377363@163.com