
钙、镁、铝等的化合物在生产生活中有着广泛的应用。甲、乙两研究小组分别对石灰乳吸收硝酸工业的尾气、碱式碳酸镁铝[MgaAlb(OH)c(CO3)d·xH2O]的有关问题进行了以下探究,请你参与并完成对有关问题的解答。
(1)甲组利用石灰乳和硝酸工业的尾气(含NO、NO2)反应,既能净化尾气,又能获得有广泛应用的Ca(NO2)2,其部分实验流程如下:

①大量氮氧化物排放到空气中,会破坏臭氧层,形成酸雨等,由氮氧化物形成的酸雨称为是_________(填“硫酸”或“硝酸”)型酸雨。过滤操作中,需要使用的玻璃仪器有烧杯、玻璃棒和_______________。
②上述流程中采用“气一液逆流接触”吸收(尾气从吸收塔底进入,石灰乳从吸收塔顶喷淋),其目的是_________________;滤渣可循环使用,滤渣的主要成分是________。
(2)乙组查阅有关资料知道碱式碳酸镁铝受热容易分解,因此在生产生活中常用作塑料阻燃剂。
①MgaAlb(OH)c(CO3)d·xH2O中a、b、c、d的代数关系式为______________________。
②根据你的理解,你认为碱式碳酸铝镁具有阻燃作用的可能原因主要是由于其受热分解需吸收大量热量和_______________________________。
③为确定碱式碳酸铝镁的组成,进行如下实验:准确称取6.780 g样品与足量稀盐酸充分反应,生成CO2 1.120 L(已换算成标准状况下)。另取一定量样品在空气中加热,样品的固体残留率随温度的变化如图所示(样品在270℃时已完全失去结晶水,600℃以上残留固体为金属氧化物的混合物)。

注意:固体残留率是指 。则在270℃~600℃之间,物质受热分解放出的气体是__________(填化学式)。6.780 g样品中,除结晶水外还含有的氢原子的物质的量是__________mol。
。则在270℃~600℃之间,物质受热分解放出的气体是__________(填化学式)。6.780 g样品中,除结晶水外还含有的氢原子的物质的量是__________mol。
(1)①硝酸 漏斗 ②增大吸收效率、提高原料利用率 Ca(OH)2(2)①2a+3b=c+2d ②生成的产物具有阻燃作用;③CO2、H2O 0.03
【解析】
试题分析:(1)①酸雨分为硫酸雨、硝酸雨,硫酸雨由SO2引起,硝酸雨由氮的氧化物引起,根据题意酸雨由氮的氧化物形成的,因此称为硝酸型酸雨。过滤时用到的仪器带铁圈的铁架台、漏斗、玻璃棒、烧杯、滤纸,因此需要的玻璃仪器有:漏斗、玻璃棒、烧杯;②尾气从塔底进入,石灰乳从吸收塔顶喷淋目的:增大吸收效率,提高原料利用率;未反应的石灰乳在过滤中作为滤渣,可以循环吸收尾气;(2)①根据化合价的代数和为0,2a+3b=c+2d②碱式碳酸铝镁受热分解吸收大量的热,降低温度,同时分解过程产生大量的CO2进行灭火及氧化镁、氧化铝都是耐高温材料附着在燃烧物上隔绝空气,生成的产物具有阻燃作用;③样品在270℃时已完全失去结晶水,600℃以上残留固体为金属氧化物的混合物,说明在270℃--600℃之间,受热分解放出的气体是CO2、H2O;6.780g样品中n(CO2)=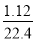 =0.05mol,m(CO2)=0.05×44=2.2g,270℃--600℃之间失去结晶水后进一步分解放出CO2和H2O,m(CO2)+m(H2O)=6.780×(0.7345-0.3702)=2.470g,m(H2O)=2.470-2.2=0.27 g,n(H2O)=0.27/18=0.015mol,n(H)=0.015×2=0.03mol
=0.05mol,m(CO2)=0.05×44=2.2g,270℃--600℃之间失去结晶水后进一步分解放出CO2和H2O,m(CO2)+m(H2O)=6.780×(0.7345-0.3702)=2.470g,m(H2O)=2.470-2.2=0.27 g,n(H2O)=0.27/18=0.015mol,n(H)=0.015×2=0.03mol
考点:考查酸雨的分类,实验基本操作,化学工业的应用及化学计算等相关知识。


 冲刺100分1号卷系列答案
冲刺100分1号卷系列答案科目:高中化学 来源:2014-2015学年山东省莱芜市高三1月月考化学试卷(解析版) 题型:选择题
NA代表阿伏加德罗常数的值。下列有关叙述正确的是
A.含有NA个氮气和乙烯分子的混合气体质量为28g
B.标准状况下,11.2L氦气中含有NA个氦原子
C.将NA个NH3分子溶于lL水中得到lmol/的氨水
D.100mL 0.1mol/LAlCl3溶液含有0.01NA个A13+
查看答案和解析>>
科目:高中化学 来源:2014-2015学年山东省菏泽市高三1月月考化学试卷(解析版) 题型:选择题
下列过程属于化学变化的有
①白色的硫酸铜粉末久置于空气中变成蓝色;②同素异形体之间的互变; ③福尔马林用来浸制标本;④氯化钠溶液通电后导电;⑤蜂蚁螫咬处涂稀氨水或小苏打溶液可以减轻痛苦;⑥同分异构体之间的互变
A.3个 B.4个 C.5个 D.6个
查看答案和解析>>
科目:高中化学 来源:2014-2015陕西省西安市高二上学期期末化学试卷(解析版) 题型:选择题
以硫酸铜作电解液,对含有杂质Fe、Zn、Ag的粗铜进行电解精炼。下列叙述正确的是
①粗铜与直流电源负极相连;
②阴极发生的反应为Cu2++2e-=Cu
③电路中每通过3.01×1023个电子,得到的精铜质量为16g
④杂质Ag以Ag2SO4的形式沉入电解槽形成阳极泥
A.①③ B.②④ C.③④ D.②③
查看答案和解析>>
科目:高中化学 来源:2014-2015陕西省西安市高二上学期期末化学试卷(解析版) 题型:选择题
将纯锌片和纯铜片按图示方式插入同浓度的稀硫酸中一段时间,以下叙述正确的是

A.两烧杯中铜片表面均无气泡产生
B.甲中铜片是正极,乙中铜片是负极
C.两烧杯中溶液的pH均增大
D.产生气泡的速度甲比乙慢
查看答案和解析>>
科目:高中化学 来源:2014-2015江苏徐州市高一上学期期末考试化学试卷(解析版) 题型:选择题
为除去粗盐中的Ca2+、Mg2+、SO42-及泥沙,可先将粗盐溶于水,然后再进行下列五项操作:①过滤:②加过量NaOH溶液;③加适量稀盐酸;④加过量Na2CO3溶液;⑤加过量BaCl2溶液。则正确的操作顺序是
A.①④②⑤③ B.⑤②④③① C.②④⑤①⑨ D.⑤④②①③
查看答案和解析>>
科目:高中化学 来源:2014-2015江苏徐州市高一上学期期末考试化学试卷(解析版) 题型:选择题
下列关于氯气的叙述中不正确的是
A.可用向上排空气法收集少量的氯气
B.与水反应生成的次氯酸是一种弱酸
C.常温下干燥的Cl2能用钢瓶贮运,所以Cl2不与铁反应
D.与氢氧化钠溶液反应时,Cl2既被还原,同时又被氧化
查看答案和解析>>
科目:高中化学 来源:2014-2015江苏省高二第一学期化学试卷(解析版) 题型:实验题
(10分)实验室中有一未知浓度的稀盐酸,某学在实验室中进行测定盐酸浓度的实验,请完成下列填空。
(1)配制100 mL 0.10 mol·L-1 NaOH标准溶液。
①主要操作步骤:计算→称量→溶解→(冷却后)转移→洗涤(并将洗涤液移入容量瓶)→定容→摇匀→将配制好的溶液倒入试剂瓶,贴上标签。
②托盘天平称量 g氢氧化钠固体。
(2)取20.00 mL待测盐酸放入锥形瓶中,并滴加2~3滴酚酞作指示剂,用自己配制的NaOH标准溶液进行滴定。重复上述滴定操作2~3次,记录数据如下。
实验编号 | NaOH溶液的浓度/(mol·L-1) | 滴定完成时,NaOH溶液滴入的体积/mL | 待测盐酸的体积/mL |
1 | 0.10 | 22.58 | 20.00 |
2 | 0.10 | 22.72 | 20.00 |
3 | 0.10 | 22.80 | 20.00 |
①滴定达到终点的标志是 。
②根据上述数据,可计算出该盐酸的浓度约为 (保留两位有效数字)。
③排去碱式滴定管中气泡的方法应采用如图所示操作中的 ,然后轻轻挤压玻璃球使尖嘴部分充满碱液。

④在上述实验中,下列操作(其他操作正确)会造成测定结果偏高的有 。
A.滴定终点读数时俯视读数
B.酸式滴定管使用前,水洗后未用待测盐酸润洗
C.锥形瓶水洗后未干燥
D.碱式滴定管尖嘴部分有气泡,滴定后消失
查看答案和解析>>
科目:高中化学 来源:2014-2015湖南省浏阳市高二上学期理科化学试卷(解析版) 题型:选择题
下列属于放热反应的是
A.浓硫酸的稀释 B.铝热反应
C.氢气还原氧化铜 D.Ba(OH)2·2H2O和NH4Cl(固体)混合
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com