
【题目】向0.5L 0.4mol/L的NaClO溶液中缓慢通入0.1mol CO2根据右表提供的数据,下列判断不正确的是
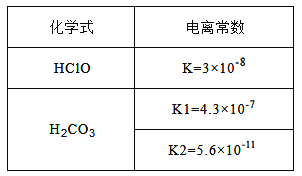
A. 原溶液中:c(ClO-)>c(OH-)>c(H+)
B. 原溶液中c(OH-)=c(H+)+c(HClO)
C. 反应后溶液中c(HClO)>c(HCO3-)>c(ClO-)>c(CO32-)
D. 反应后溶液中c(Na+)=c(HCO3-)+c(CO32-)+c(H2CO3)+c(ClO-)+c(HClO)
【答案】D
【解析】根据表中数据可知酸性:H2CO3>HClO>HCO3-。次氯酸钠的物质的量是0.2mol,与0.1molCO2反应的方程式为:NaClO+CO2+H2O=HClO+NaHCO3,即所得溶液是等浓度的次氯酸钠、次氯酸和碳酸氢钠的混合溶液。A.次氯酸钠水解,溶液显碱性,则原溶液中:c(ClO-)> c(OH-)> c(H+),A正确;B.根据质子守恒可知原溶液中:c(OH-)=c(H+)+c(HClO),B正确;C.次氯酸钠的水解程度大于碳酸氢钠,则反应后溶液中c(HClO)>c(HCO3-)>c(ClO-)>c(CO32-),C正确;D.根据物料守恒可知反应后溶液中:c(Na+)=c(ClO-)+c(HClO),D错误,答案选D。


科目:高中化学 来源: 题型:
【题目】某工厂排放的污水只可能含Na+、K+、NH4+、Mg2+、Fe3+、SO32-、SO42-和Cl-中的几种(忽略由水电离产生的H+、OH-)。将试样平均分成甲、乙、丙各l00mL三份,每次均加入足量的试剂,设计如下实验。下列说法正确的是( )

A. 废水可能含有Na+、K+、Fe3+
B. 可能存在的离子用焰色反应进一步检验确认
C. 废水一定含有Cl-、SO42-和Mg2+,且c(Cl-)=0.2mol·L-1
D. 废水一定不含 SO32-、Cl-、NH4+、Na+、K+、Fe3+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温时,CaCO3在水中的溶解平衡曲线如图所示,已知:25 ℃其溶度积为2.8×10-9 mol2/L2,下列说法不正确的是
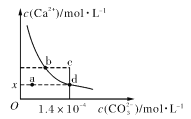
A. x数值为2×10-5
B. c点时有碳酸钙沉淀生成
C. 加入蒸馏水可使溶液由d点变到a点
D. b点与d点对应的溶度积相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了减缓锌和一定浓度盐酸的反应速率,而又不减少产生氢气的量,向盐酸中加入下列物质或措施可行的是( )
A. 升温 B. NaF溶液 C. NaNO3溶液 D. 几滴CuSO4溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关烯烃的说法中,正确的是
A. 烯烃分子中所有的原子一定在同一平面上
B. 烯烃在适宜的条件下只能发生加成反应不能发生取代反应
C. 分子式是C4H8的烃分子中一定含有碳碳双键
D. 通过石油的催化裂化及裂解可以得到气态烯烃
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是元素周期表的一部分,关于元素X、Y、Z的叙述正确的是( )

①X的气态氢化物与Y的最高价氧化物的水化物能发生反应生成盐
②Y、Z的气态氢化物水溶液的酸性Y<Z
③Z的单质在常温下是液体,可与铁粉反应
④Z的原子序数比Y大19 ⑤Z所在的周期中含有32种元素
A. 只有①②③④ B. ①②③④⑤ C. 只有③ D. 只有①④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上制取CuCl2的生产流程如下:
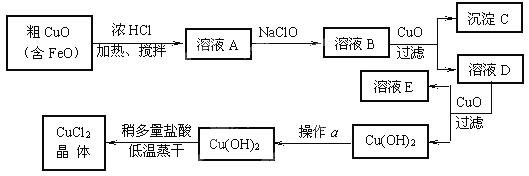
请结合下表数据,回答下列问题:
物 质 | Fe(OH)2 | Cu(OH)2 | Fe(OH)3 |
完全沉淀时的pH范围 | ≥9.6 | ≥6.4 | 3~4 |
⑴ 溶液A中加入NaClO的目的是 ;
此反应离子方程式为 ;
⑵ 在溶液B中加入CuO的作用是 ;
⑶ 操作a的目的是 ;
⑷ 在Cu(OH)2加入盐酸使Cu(OH)2转变为CuCl2。采用多量盐酸和低温蒸干的目的是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关实验操作的叙述错误的是( )
A.过滤操作中,玻璃棒应适时搅拌漏斗器
B.蒸发时,不能把蒸发皿放置于石棉网上加热
C.萃取分液时,将塞上凹槽或小孔对准漏斗上小孔,然后打开活塞才能放出下层液体
D.配制容量瓶,定容时改用胶头滴管滴加蒸馏水
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com