
【题目】如图为原电池装置示意图。
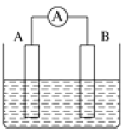
⑴将铝片和铜片用导线相连,一组插入浓硝酸中,一组插入烧碱溶液中,分别形成了原电池,在这两个原电池中,作负极的分别是___________(填字母)。
A.铝片、铜片 B.铜片、铝片 C.铝片、铝片 D.铜片、铜片
写出插入烧碱溶液中形成的原电池的负极反应式:________________。
⑵若A为Pb,B为PbO2,电解质为H2SO4溶液,工作时的总反应为Pb+PbO2+2H2SO4=2PbSO4+2H2O。写出B电极反应式:________________;该电池在工作时,A电极的质量将___________(填“增加”“减小”或“不变”)。若该电池反应消耗了0.1mol H2SO4,则转移电子的数目为____________。
⑶若A、B均为铂片,电解质为KOH溶液,分别从A、B两极通入C3H8和O2,该电池即为丙烷燃料电池,写出B电极反应式:_________________;A极的反应物C3H8的一氯代物有__________种同分异构体。
【答案】B Al-3e-+4OH-=AlO2-+2H2O PbO2+SO42-+4H++2e-=PbSO4+2H2O 增加 0.1NA O2+2H2O+4e-=4OH- 2
【解析】
(1)铝片和铜片用导线相连,一组插入浓硝酸中,一组插入烧碱溶液中,分别形成了原电池,根据负极金属单质上电子来判断;碱性条件下,Al失电子生成偏铝酸根离子;
(2)B为PbO2,是原电池的正极,发生还原反应,注意电解质溶液是硫酸;A是Pb,其离子能够与硫酸根反应生成沉淀;据电池反应式计算;
(3)若AB为金属铂片,电解质溶液为KOH溶液,分别从AB两极通入C3H8和O2,该电池即为丙烷燃料电池,通入C3H8的一极为负极,被氧化,产生的二氧化碳与碱反应生成碳酸盐。
(1)将铝片和铜片用导线相连,一组插入浓硝酸中,铝钝化,所以Cu失电子作负极,一组插入烧碱溶液中,Cu与氢氧化钠不反应,Al失电子作负极,
碱性条件下,Al失电子生成偏铝酸根离子,其电极反应为:Al+4OH--3e-=AlO2-+2H2O;
故答案为:B;Al+4OH--3e-=AlO2-+2H2O;
(2)B为PbO2,是原电池的正极,发生还原反应,电解质溶液是硫酸,铅离子能够与硫酸根离子生成沉淀,电极反应式为:PbO2+SO42-+4H++2e-=PbSO4+2H2O;
A极Pb失电子生成铅离子能够与硫酸根反应生成沉淀,导致质量增大;据电池反应式可知,每有2mol硫酸反应转移电子2mol,则0.1mol硫酸反应转移电子数目为0.1NA,
故答案为:PbO2+SO42-+4H++2e-=PbSO4+2H2O;增重;0.1NA;
(3)若AB均为金属铂片,电解质溶液为KOH溶液,分别从AB两极通入C3H8和O2 ,该电池即为丙烷燃料电池,通入O2的一极为正极,被还原,电极方程式为O2+2H2O+4e-=4OH-,A极的反应物C3H8只有两种不同环境的氢,一氯代物有2种同分异构体。


科目:高中化学 来源: 题型:
【题目】M(NO3)2热分解的化学方程式为:2M(NO3)2 ![]() 2MO+4NO2↑+O2↑。加热29.6 g M(NO3)2使其完全分解,在标准状况下收集11200 mL的气体,那么M的摩尔质量是( )
2MO+4NO2↑+O2↑。加热29.6 g M(NO3)2使其完全分解,在标准状况下收集11200 mL的气体,那么M的摩尔质量是( )
A.64 g·mol-1B.24 g·mol-1
C.65 g·mol-1D.40 g·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】今有化合物
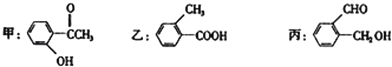
(1)请写出甲中含氧官能团的名称:________
(2)请判别上述哪些化合物互为同分异构体:_______
(3)甲、乙、丙三种物质中,遇FeCl3溶液显紫色的是_____(填“甲”“乙”或“丙”,下同),能与银氨溶液发生银镜反应的是_____,能与碳酸钠溶液反应放出CO2气体的是_____
(4)请按酸性由强至弱排列甲、乙、丙的顺序:_______
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】早在1998年,中国科学家便成功地在较低温度下制造出金刚石:CCl4+4Na![]() C(金刚石)+4NaCl。这项成果被“美国化学与工程新闻”评价为“稻草变黄金”。回答下列问题:
C(金刚石)+4NaCl。这项成果被“美国化学与工程新闻”评价为“稻草变黄金”。回答下列问题:
(1)Ni原子价层电子的排布式为_______。元素C、Cl、Na中,第一电离能最大的是______________。
(2)石墨在高温高压下也可转变为金刚石。在石墨和金刚石中,C原子的杂化类型分别为_____________,熔点较高的是_____________,其原因为_______________。
(3)NH3易与Ni形成配合物 [Ni(NH3)6]SO4,该配合物中存在的化学键类型有_____________,其阴离子的空间构型为_____________。
(4)金属间化合物MgCNi3是一种新型超导体,呈钙钛矿构型,X射线衍射实验测得其晶胞参数为a=0.3812nm,其晶胞结构如图所示。晶胞中C位于Ni所形成的正八面体的体心,该正八面体的边长为___________nm。(![]() =1.414)
=1.414)
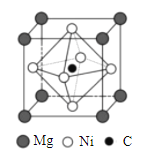
(5)在MgCNi3晶胞结构的另一种表示中,Mg处于体心位置,则C处于________________位置,Ni处于_______________位置。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将100mL稀硝酸和稀硫酸的混合酸溶液平均分成两份。向其中一份中逐渐加入铜粉最多能溶解9.6g(假设此时硝酸只被还原为NO,下同);向另一份中逐渐加入铁粉,产生气体的量随铁粉质量的变化如图所示。则下列判断中错误的是( )
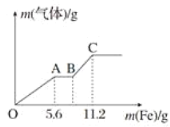
A.原混合酸溶液中H2SO4的浓度为2.0molL-1B.A点对应消耗NO3-物质的量为0.1mol
C.B点对应消耗铁粉的质量为8.4gD.OA段产生的气体是NO,BC段产生的气体是H2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用所学化学知识解答问题:
(1)微粒![]() 中的质子数是_____,中子数是_____,核外电子数是_____。
中的质子数是_____,中子数是_____,核外电子数是_____。
(2)写出氯离子的原子结构示意图__,写出氯化钠的电子式___,用电子式表示HCl的形成过程___。
(3)NH4NO3是___化合物(填“离子”或“共价”),NaOH所含化学键类型为______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)![]() 的名称是_______。
的名称是_______。
(2)分子式符合C7H16且含有四个甲基的结构有__________种。
(3)核磁共振仪处理![]() ,氢谱图中有___种氢,峰面积之比为____。
,氢谱图中有___种氢,峰面积之比为____。
(4)水的熔沸点比同主族其它氢化物的都高,原因是______。
(5)将有机物A置于氧气流中充分燃烧,实验测得:生成5.4gH2O和8.8gCO2,消耗氧气6.72L(标准状况下),则A的实验式是___,用质谱仪测定A的相对分子质量,得到如图所示质谱图,则其相对分子质量为____,A的分子式是____。
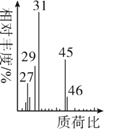
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高氯酸铵(![]() )是复合火箭推进剂的重要成分。通过如图所示的装置及实验步骤可以测定某高氯酸铵样品的纯度。
)是复合火箭推进剂的重要成分。通过如图所示的装置及实验步骤可以测定某高氯酸铵样品的纯度。
步骤1:检查装置气密性。
步骤2:准确称取样品![]() 于蒸馏烧瓶中,加入约
于蒸馏烧瓶中,加入约![]() 水溶解。
水溶解。
步骤3:准确量取![]() 溶液于锥形瓶中。
溶液于锥形瓶中。
步骤4:经仪器A向蒸馏瓶中加入![]() 溶液。
溶液。
步骤5:加热蒸馏至蒸馏烧瓶中剩余约100mL溶液。
步骤6:用新煮沸过的水冲洗冷凝装置2~3次,洗涤液并入锥形瓶中。
步骤7:向锥形瓶中加入酸碱指示剂,用![]() 标准溶液滴定至终点,消耗NaOH标准溶液
标准溶液滴定至终点,消耗NaOH标准溶液![]() 。
。
步骤8:将实验步骤1~7重复2次。

(1)仪器A的名称是______________。
(2)计算样品中高氯酸铵的质量分数_________(写出计算过程,已知杂质不参与反应)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,用 0. 100 mol L-1 的盐酸滴定 0.1 00 molL-1 的氨水,其滴定曲线如图所示:
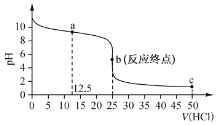
下列说法正确的是
A. 该滴定操作可用甲基橙作指示剂
B. a 点溶液中:c(NH4+)>c(NH3 H2O)>c(Cl- )
C. c 点溶液中:c(Cl-)>c(NH4+)>c(H+)
D. a→c过程中锥形瓶内水的电离度不断增大
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com