
【题目】下列有关环境问题的说法正确的是( )
A.燃煤时加入适量石灰石,可减少废气中SO2的量
B.臭氧的体积分数超过10﹣4%的空气有利于人体健康
C.CO,NO,NO2都是大气污染气体,在空气中都能稳定存在
D.含磷合成洗涤剂易于被细菌分解,故不会导致水体污染
科目:高中化学 来源: 题型:
【题目】100℃时,将0.1 mol N2O4置于1L密闭的烧瓶中,然后将烧瓶放入100℃ 的恒温槽中,烧瓶内的气体逐渐变为红棕色:
N2O4(g)![]() 2NO2(g)。下列结论不能说明上述反应在该条件下已经达到平衡状态的是
2NO2(g)。下列结论不能说明上述反应在该条件下已经达到平衡状态的是
①N2O4的消耗速率与NO2的生成速率之比为1:2
②NO2生成速率与NO2消耗速率相等
③烧瓶内气体的压强不再变化
④烧瓶内气体的质量不再变化
⑤NO2的物质的量浓度不再改变
⑥烧瓶内气体的颜色不再加深
⑦烧瓶内气体的平均相对分子质量不再变化
⑧烧瓶内气体的密度不再变化。
A. ②③⑥⑦ B. ①④⑧ C. 只有①④ D. 只有⑦⑧
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】水是极弱的电解质,改变温度或加入某些电解质会影响水的电离。请回答下列问题:
(1)纯水在100 ℃时,pH=6,该温度下0.1 mol·L-1的NaOH溶液的pH=________。
(2)25 ℃时,向水中加入少量碳酸钠固体,得到pH为11的溶液,其水解的主要离子方程式为_______________________________________,由水电离出的
c(OH-)=________mol·L-1。
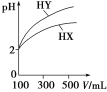
(3)体积均为100 mL、pH均为2的一元酸HX、HY,加水稀释过程中pH与溶液体积的关系如图所示,则HX是________(填“强酸”或“弱酸”),理由是_________________________。
(4)电离平衡常数是衡量弱电解质电离程度强弱的物理量。已知:
化学式 | 电离平衡常数(25 ℃) |
HCN | K=4.9×10-10 |
CH3COOH | K=1.8×10-5 |
H2CO3 | K1=4.3×10-7、K2=5.6×10-11 |
①25 ℃时,等浓度的NaCN溶液、Na2CO3溶液和CH3COONa溶液,溶液的pH由大到小的顺序为______________________(填化学式)。
②25 ℃时,在0.5 mol·L-1的醋酸溶液中由醋酸电离出的c(H+)约是由水电离出的c(H+)的________倍。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙酸异戊酯是组成蜜蜂信息素的成分之一,具有香蕉的香味。实验室制备乙酸异戊酯的反应、装置和有关数据如下:

相对分子质量 | 密度/(g·cm3) | 沸点/℃ | 水中溶解性 | |
异戊醇 | 88 | 0.8123 | 131 | 微溶 |
乙酸 | 60 | 1.0492 | 118 | 溶 |
乙酸异戊酯 | 130 | 0.8670 | 112 | 难溶 |
实验步骤:
在A 中加入4.40g异戊醇、6.00g乙酸、数滴浓硫酸和2~3片碎瓷片。开始缓慢加热A,回流50min。反应液冷至室温后倒入分液漏斗中,分别用少量水、饱和碳酸氢钠溶液和水洗涤;分出的产物加入少量无水MgSO4固体,静置片刻,过滤除去MgSO4固体,进行蒸馏纯化,收集140~143℃馏分,得乙酸异戊酯4.55g。
请回答下列问题:
(1)仪器B的名称是_____;B中冷却水是从_____(填“下口”或“上口”)流进的。
(2)加入碎瓷片的作用是_______;如果加热一段时间后发现忘记加瓷片,应该采取的操作是_____________________。
(3)在洗涤、分液操作中,第二次洗涤,用饱和碳酸氢钠溶液洗涤的主要目的是_______,不能用NaOH溶液洗涤的原因是___________。第二次洗涤后,充分振荡,然后静置,待分层后,产物应该从分液漏斗的_______(填“上口倒出”或“下口放出”)。
(4)在蒸馏操作中,仪器选择及安装都正确的是下图中的_____(填字母标号),若从130℃ 便开始收集馏分,会使实验的产率______(填“偏高”、“偏低”或“无影响”)。

(5)水的沸点为100℃,比乙酸异戊酯低42℃ ,但仍要先加入MgSO4后过滤再蒸馏,而不是直接蒸馏。结合题中信息分析,下列说法正确的是______(填字母)。
A.水可能会与乙酸异戊酯形成一种“恒沸溶液”(在溶液的某一组成时,在某温度下,混合液同时汽化或同时冷凝),不能进一步提纯,所以要先用MgSO4干燥
B.在加入MgSO4后如不先过滤就蒸馏,加热时硫酸镁的结晶水合物又会脱水
C.如不先用MgSO4吸收水分,蒸馏时水先被蒸出,浪费能源和延长蒸馏时间
D.本实验中要乙酸过量,而不是异戊醇过量,可能的原因是异戊醇比乙酸价格贵;另外异戊醇过量时,异戊醇与乙酸异戊酯沸点相近(小于30℃),蒸馏时完全分离困难
(6)将乙酸异戊酯中的异戊醇除去,是在哪个步骤中除去的______(填字母)。
A.在第一次水洗和后面的分液中除去的
B.在第二次用饱和碳酸氢钠溶液洗涤和后面的分液中除去的
C.在“过滤”中除去的
D.由于本实验中加入过量乙酸,异戊醇已经反应完全,所以不需除杂(异戊醇)了
E.在最后的“蒸馏”步骤中除去的
(7)产物乙酸异戊酯的产率是__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】科学家在2000年8月10日出版的英国《自然》杂志上报告,他们用DNA制造出了一种臂长只有7纳米的纳米级镊子,以便能够钳起分子或原子并对它们随意组合.下列分散系中的分散质的粒子直径与纳米级镊子臂长具有相同数量级的是( )
A.溶液
B.悬浊液
C.乳浊液
D.胶体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列常见物质的俗名与化学式对应正确的是
A. 熟石灰—— Ca(OH)2B. 铁红—— Fe3O4
C. 光导纤维—— SiD. 酒精—— CH3COOH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】W、X、Y、Z是四种常见的短周期主族元素,其原子半径随原子序数的变化如图所示。已知W的一种核素的质量数为18,中子数为10;X是短周期元素中原子半径最大的元素(不考虑稀有气体的原子半径);Y的单质呈黄色,常见于火山口附近。下列说法正确的是

A. 氧化物的水化物酸性:Y<Z
B. 简单离子半径:W<X<Z
C. W的简单气态氢化物的沸点高于同族其它元素的简单气态氢化物
D. 将标况下等体积的Z单质与Y的低价氧化物同时通入品红溶液中,品红溶液迅速褪色
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com