
【题目】肉桂酸甲酯(属于酯类,代号M)是常用于调制具有草莓、葡萄、樱桃、香子兰等香味的食用香精。测得其相对分子质量为162,分子中C、H、O原子个数比为5︰5︰1,且分子中只含有1个苯环,苯环上只有一个取代基。现测出M的核磁共振氢谱谱图有6个峰,其面积之比为1︰2︰2︰1︰1︰3。下列说法不正确的是
A.M的分子式为C10H10O2
B.1mol的M最多能被4molH2还原
C.肉桂酸能使溴水和酸性高锰酸钾溶液褪色
D.与M含有相同官能团,且苯环上氢的化学环境只有两种的同分异构体有3种
【答案】D
【解析】
相对分子质量为162,分子中C、H、O原子个数比为5:5:1,则分子式应为C10H10O2,分子中只含有1个苯环,苯环上只有一个取代基,核磁共振氢谱谱图有6个峰,其面积之比为1:2:2:1:1:3,则结构简式为![]() ,含有碳碳双键和苯环,可发生加成反应,含有酯基,可发生水解反应,以此解答该题。
,含有碳碳双键和苯环,可发生加成反应,含有酯基,可发生水解反应,以此解答该题。
相对分子质量为162,分子中C、H、O原子个数比为5:5:1,则分子式应为C10H10O2,分子中只含有1个苯环,苯环上只有一个取代基,核磁共振氢谱谱图有6个峰,其面积之比为1:2:2:1:1:3,则结构简式为![]() ,
,
A.由以上分析可知M的分子式为C10H10O2,故A正确;
B.含有1个苯环和1个碳碳双键,则1mol的M最多能被4molH2还原,故B正确;
C.肉桂酸含碳碳双键能使溴水和酸性高锰酸钾溶液褪色,故C正确;
D.与M含有相同官能团,则含有碳碳双键和酯基,且苯环上氢的化学环境只有两种,说明苯环有两个取代基,且位于对位,则对应的同分异构体有以下几种情况,①CH2=CH-和(HCOOCH2-、CH3COO-、-COOCH3)3种、②CH3-和(CH2=CHCOO-、CH2=CHOOC-)2种以及③(CH3CH=CH-、CH2=CHCH2-)和-OOCH 2种,共7种,故D错误。
故选D。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】室温下,CuSO4·5H2O(s)、CuSO4(s)与其水溶液之间转化的焓变关系如图:

己知CuSO4·5H2O(s)溶于水,溶液温度降低;CuSO4(s)溶于水,溶液温度升高。
下列有关说法不正确的是( )
A.△H2=△H1+△H3
B.1mol CuSO4(s)的总能量大于1mol Cu2+(aq)与1mol SO42-(aq)的总能量
C.△H2<△H1
D.从硫酸铜溶液中析出CuSO4·5H2O(s)的反应焓变△H>0
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氢气、一氧化碳、辛烷、甲烷燃烧的热化学方程式分别为
H2(g)+![]() O2(g)=H2O(l) ΔH=-285.8 kJ·mol-1
O2(g)=H2O(l) ΔH=-285.8 kJ·mol-1
CO(g)+![]() O2(g)=CO2(g) ΔH=-283.0 kJ·mol-1
O2(g)=CO2(g) ΔH=-283.0 kJ·mol-1
C8H18(l)+![]() O2(g)=8CO2(g)+9H2O(l) ΔH=-5 518 kJ·mol-1
O2(g)=8CO2(g)+9H2O(l) ΔH=-5 518 kJ·mol-1
CH4(g)+2O2(g)=CO2(g)+2H2O(l) ΔH=-890.3 kJ·mol-1
相同质量的氢气、一氧化碳、辛烷、甲烷完全燃烧时,放出热量最少的是( )
A.H2B.COC.C8H18D.CH4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列对于化学反应方向说法正确的是 ( )
A.反应2A(g)+B(g) = 3C (s)+D(g)在一定条件下能自发进行,说明该反应的ΔH>0
B.常温下反应2Na2SO3(s)+O2(g)= 2Na2SO4(s)能自发进行,则ΔH<0
C.反应2Mg(s)+CO2(g)![]() C(s)+2MgO(s)能自发进行,则该反应的△H>0
C(s)+2MgO(s)能自发进行,则该反应的△H>0
D.一定温度下,反应2NaCl(s)=2Na(s)+Cl2(g)的 △H<0 ,△S>0
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室为探究铁与浓硫酸![]() 足量
足量![]() 的反应,并验证
的反应,并验证![]() 的性质,设计如图所示装置进行实验,下列说法不正确的是()
的性质,设计如图所示装置进行实验,下列说法不正确的是()

A.装置B中酸性![]() 溶液逐渐褪色,体现了二氧化硫的还原性
溶液逐渐褪色,体现了二氧化硫的还原性
B.实验结束后可向装置A的溶液中滴加KSCN溶液以检验生成的![]()
C.装置D中品红溶液褪色可以验证![]() 的漂白性
的漂白性
D.实验时将导管a插入浓硫酸中,可防止装置B中的溶液倒吸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(16分)工业上用CO生产燃料甲醇。一定条件下发生反应:CO(g)+2H2(g)![]() CH3OH(g)。
CH3OH(g)。
图1表示反应中能量的变化;图2表示一定温度下,在体积为2L的密闭容器中加入4mol H2和一定量的CO后,CO和CH3OH(g)的浓度随时间变化。
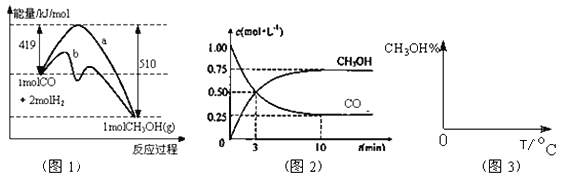
请回答下列问题:
(1)在“图1”中,曲线 (填:a或b)表示使用了催化剂;该反应属于 (填:吸热、放热)反应。
(2)下列说法正确的是
A.起始充入的CO为2mol
B.增加CO浓度,CO的转化率增大
C.容器中压强恒定时,反应已达平衡状态
D.保持温度和密闭容器容积不变,再充入1molCO和2molH2,再次达到平衡时n(CH3OH)/n(CO)会减小
(3)从反应开始到建立平衡, v(H2)=_____;该温度下CO(g)+2H2(g)![]() CH3OH(g)的化学平衡常数为______。若保持其它条件不变,将反应体系升温,则该反应化学平衡常数____ (填“增大”、“减小”或“不变”)。
CH3OH(g)的化学平衡常数为______。若保持其它条件不变,将反应体系升温,则该反应化学平衡常数____ (填“增大”、“减小”或“不变”)。
(4)请在“图3”中画出平衡时甲醇百分含量(纵坐标)随温度(横坐标)变化的曲线,要求画压强不同的2条曲线(在曲线上标出P1、P2,且P1<P2)。
(5)已知CH3OH(g)+3/2O2(g)=CO2(g)+2H2O(g) ΔH=-192.9kJ/mol
又知H2O(l)= H2O(g) ΔH=+44 kJ/mol,请写出32g的CH3OH(g)完全燃烧生成液态水的热化学方程式 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验小组探究KI 与Cu(NO3)2 的反应,进行实验一:

注: 本实验忽略Cu2+在此条件下的水解。
(1)取棕黄色清液,加入少量______溶液(试剂a),清液变为______色,说明生成了I2。
(2)探究生成I2的原因。
①甲同学进行如下实验: 向2mL Imol/LKI 溶液中加入1mL______溶液( 硝酸酸化,pH=1.5 ),再加入少量试剂a,观察到与(1)相同的现象。甲同学由此得出结论: 实验一中生成I2 的原因是酸性条件下,NO3- 氧化了I-。
②乙同学认为仅由甲同学的实验还不能得出相应结论。他的理由是该实验没有排除____氧化I-的可能性。
③若要确证实验一中是NO3-氧化了I-,应在实验一的基础上进行检验______的实验。
(3)探究棕黑色沉淀的组成。
①查阅资料得知: CuI 为难溶于水的白色固体。于是对棕黑色沉淀的组成提出两种假设:
a.CuI吸附I2; b.______吸附I2。
为证明上述假设是否成立,取棕黑色沉淀进行实验二:

已知: CuI难溶于CCl4;I2+2S2O32-=2I-+S4O62-(无色);Cu++2S2O32-=Cu(S2O3)23-(无色)。
由实验二得出结论: 棕黑色沉淀是CuI吸附I2 形成的。
②现象ⅲ为______________。
③用化学平衡移动原理解释产生现象ii 的原因:________________。
④由实验二可推知,Cu(NO3)2 与KI 反应过程中,一定发生的反应的离子方程式为______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列热化学方程式书写正确的是:
A.2SO2+O2![]() 2SO3 ΔH=-196.6 kJ·mol-1
2SO3 ΔH=-196.6 kJ·mol-1
B.H2(g)+ ![]() O2(g)=H2O(l) ΔH=-285.5 kJ·mol-1
O2(g)=H2O(l) ΔH=-285.5 kJ·mol-1
C.2H2(g)+O2(g)=2H2O(l) ΔH=-571.6 kJ
D.C(s)+O2(g)=CO2(g) ΔH=+393.5 kJ·mol-1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com