
【题目】下列化学用语表达错误的是( )
A.环己烷的实验式:CH2
B.四氯化碳分子的球棍模 型: ![]()
C.HCl的电子式: ![]()
D.氟原子的结构示意图: ![]()
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】现有下列四种因素:①温度和压强、②所含微粒数、③微粒本身大小、④微粒间的距离,其中对气体物质体积有显著影响的是( )
A.②③④B.①②④C.①③④D.①②③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向500mLNaOH溶液中投入10.8gAl,二者恰好完全反应后,则参加反应的NaOH的物质的量为________;原NaOH溶液的物质的量浓度为________;生成标准状况下H2的体积为__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】从铝土矿(主要成分是Al2O3 , 含SiO2、Fe2O3、MgO等杂质)中提取氧化铝的两种工艺流程如图: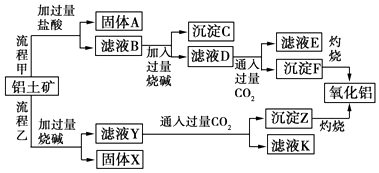
请回答下列问题:
(1)写出流程甲所涉及的离子方程式为、、 .
(2)流程乙加入烧碱后Al2O3发生反应的离子方程式为 .
(3)沉淀C的主要成分是 , 除去沉淀C的操作是 .
(4)滤液D中溶质的主要成分是(填化学式);写出向滤液D中通入过量CO2发生反应的离子方程式 .
(5)在流程中,选用CO2作酸化剂,能不能用盐酸代替CO2 ?其原因是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法规范的是( )
A. 98g稀硫酸所含分子数为1mol B. 氧的摩尔质量为32g/mol
C. 某硫酸溶液中H2SO4的质量分数为60% D. 标准状况下,1mol气体的体积约为22.4L/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二甲醚是一种重要的化工原料,利用水煤气(CO、H2)合成二甲醚是工业上的常用方法,该方法由以下几步组成: 2H2(g)+CO(g)CH3OH(g)△H=﹣90.0kJmol﹣1①
2CH3OH(g)CH3OCH3(g)+H2O(g)△H=﹣24.5kJmol﹣1②
CO(g)+H2O(g)CO2(g)+H2(g)△H=﹣41.1kJmol﹣1③
(1)下列说法正确的是
A.反应①的△S<0、△H<0,所以能在较低温度下自发进行.
B.反应③的H2O与CO的生成速率之比为1:1时,表示该反应已经达到平衡状态
C.反应②属于加成反应
(2)反应①合成的甲醇在工业上可以用作燃料电池,请写出甲醇燃料电池(KOH溶液)负极电极反应式 .
(3)当合成气中CO与H2的物质的量之比恒定时,温度、压强对CO转化率影响如图1所示,图1中A点的v(逆)B点的v(正)(填“>”、“<”或“=”),说明理由 . 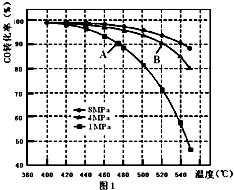
(4)一定温度下,密闭容器中发生反应③,该反应的平衡常数表达式k=;水蒸气的转化率与 ![]() 的关系如图2,计算该温度下反应③的平衡常数K= .
的关系如图2,计算该温度下反应③的平衡常数K= . 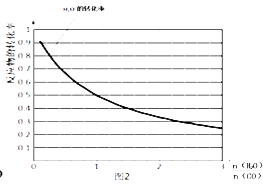
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海洋是资源的宝库,蕴藏着丰富的化学元素,如氯、溴、碘等.
(1)在光照条件下,氯气和氢气反应过程如下: ①Cl2→Cl+Cl
②Cl+H2→HCl+H
③H+Cl2→HCl+Cl
…
反应②中形成的化合物的电子式为;反应③中被破坏的化学键属于键(填“极性”或“非极性”).
(2)已知在短周期主族元素中,元素a与氯元素相邻且属同一周期,元素b也与氯元素相邻且属于同一主族,那么比较元素a、b以及氯元素三者的原子半径由大到小的顺序是(用元素符号表示).与氯元素同周期且金属性最强的元素位于周期表的第周期族.
(3)卤素单质及化合物在许多性质上都存在着递变规律.下列有关说法错误的是(填字母).
A.卤素单质的熔沸点按F2、Cl、Br2、I2的顺序由低到高
B.原子半径按
C.Cl、Br、I的顺序由大到小
D.卤化氢的稳定性按的H
E.HCl、HBr、HI的顺序由强到弱
F.卤素单质与氢气化合按的F2、Cl2、Br2、I2顺序由难变易
(4)碘单质及其化合物具有重要应用.下列说法正确的是(填字母). a. ![]() I与
I与 ![]() I互为同位素
I互为同位素
b.加碘食盐能使淀粉溶液变蓝
c.从海带中提取I2的过程只发生化学变化
d.提纯含泥沙的粗碘可用升华法.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com