
【题目】己烷雌酚的一种合成路线如下:

下列叙述不正确的是
A. 在NaOH水溶液中加热,化合物X可发生消去反应
B. 在一定条件下,1mol化合物Y可消耗4molBr2
C. 用FeCl3溶液可鉴别化合物X和Y
D. 在一定条件,化合物Y可与HCHO发生缩聚反应
 捷径训练检测卷系列答案
捷径训练检测卷系列答案 小夫子全能检测系列答案
小夫子全能检测系列答案科目:高中化学 来源: 题型:
【题目】实验室里常用浓盐酸与二氧化锰反应来制取少量的氯气,反应的化学方程式为 MnO2 + 4HCl (浓)![]() MnCl2+ Cl2↑ +2H2O ,欲制得标准状况下4.48L氯气,
MnCl2+ Cl2↑ +2H2O ,欲制得标准状况下4.48L氯气,
(1)参加反应的HCl的质量是 __________ 克
(2)反应中实际被氧化的HCl的物质的量是__________ mol
(3)反应中转移的电子个数为 ______________ .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NA表示阿伏加德罗常数的值,下列叙述正确的是 ( )
A.常温常压下,22.4 L CCl4、CO2含有的分子数为1NA
B.常温常压下,1.06 g Na2CO3含有的Na+离子数为0.02NA
C.通常状况下,NA个CO2分子占有的体积约为22.4 L
D.物质的量浓度为0.5 mol/L的MgCl2溶液中,含有Cl-个数为1NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述错误的是( )
A. 电镀时,待镀的金属制品作阳极
B. 用惰性电极电解CuSO4溶液,溶液pH增大
C. 氢氧燃料电池(酸性电解质)中,正极反应为O2+4H++4e﹣=2H2O
D. 镀锌铁皮比镀锡铁皮耐腐蚀
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1).某溶液有Cl-、CO![]() 、SO
、SO![]() ,要求依次检验出这三种离子,请完成下列实验设计:
,要求依次检验出这三种离子,请完成下列实验设计:
检验离子 | 所加试剂 | 实验现象 | 离子方程式 |
①CO | 稀硝酸 | _________ | _________ |
②SO | _________ | 产生白色沉淀 | _________ |
③ Cl- | _________ | 产生白色沉淀 | _________ |
(2)KCl样品中含有少量K2CO3、K2SO4和不溶于水的杂质,为了提纯KCl,先将样品溶于适量水中,充分搅拌后过滤,再将滤液按下图所示步骤进行操作:
回答下列问题:

①试剂Ⅰ的化学式为________________,判断试剂Ⅰ已加过量的方法是_____________。
② ②中加入试剂Ⅱ的目的是__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】无水氯化锌是有机合成中重要催化剂,无水氯化锌为白色粉末,易潮解,沸点为732℃。久置市售氯化锌常含Zn(OH)Cl,影响催化效果。实验室用HC1气体“置换”除水、升华氯化锌相结合的方法提纯市售氯化锌。
(1)选用下图所示的装置(可以重复选用)进行实验,装置接口依次连接的合理顺序为:a→___________。
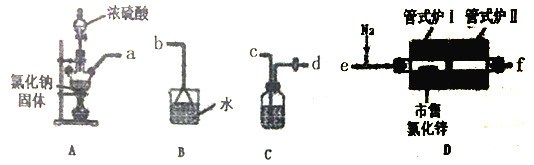
(2)装置A盛氯化钠固体的仪器名称是___________,装置C中试剂是___________。
(3)实验开始时,通入HC1和N2,将管式炉I,Ⅱ升温至150℃,装置D中发生的化学反应方程式为___________;此时通入N2的目的是______________________;
(4)反应一段时间后保持管式炉I、Ⅱ温度为350℃,保证将水除尽,再______________________;(填操作)最后在氮气保护下将氯化锌刮出玻璃管外,保存待用。
(5)若称取100.00g市售氯化锌样品,经提纯最终得到高纯氯化锌100.3g,则样品中氯化锌纯度为___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】石油是一种重要的能源,通过石油分馏可得到重油,以重油为原料,可合成X:CH3COOCH=CH2。其中A是最简单的烯烃,B能发生银镜反应,D的相对分子质量比A小2。请回答下列有关问题:

(1)A中的官能团名称是___________________
(2)B→C的化学方程式_____________________________
(3)已知C与D发生加成反应生成X,其化学方程式为________________________
(4)下列说法正确的是_____
A.此处的“某工艺”指的是分馏 B.B在一定条件下能与氢气发生加成反应
C.X不溶于水,能使酸性高锰酸钾溶液褪色 D.可用溴的四氯化碳溶液鉴别A和D
(5)F是X的同分异构体,1molF能与4molAg(NH3)2OH反应,写出F可能的结构简式_____________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. 将纯水加热至较高温度,Kw变大、pH变小、呈酸性
B. 常温下,将pH=4的醋酸溶液稀释后,溶液中所有离子的浓度均降低
C. 向0.1 mol·L-1醋酸溶液中加入少量冰醋酸,溶液的pH减小,醋酸电离程度变大
D. 等体积、pH都为3的酸HA和HB分别与足量的Zn反应,HA放出的H2多,说明HA的酸性小于HB
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某溶液中只可能含有下列离子中的几种:K+、NO![]() 、SO
、SO![]() 、NH
、NH![]() 、CO
、CO![]() (不考虑溶液中少量的H+和OH-),取200mL该溶液,分为两等份进行下列实验:
(不考虑溶液中少量的H+和OH-),取200mL该溶液,分为两等份进行下列实验:
实验1:第一份加入足量的烧碱并加热,产生的气体在标准状况下为224mL;(已知NH4+在碱性条件下可以生产氨气)
实验2:第二份先加入足量的盐酸,无现象,再加入足量的BaCl2溶液,得固体2.33g。
下列说法正确的是( )
A. 该溶液中无法确定是否含有K+
B. 该溶液中肯定含有NO![]() 、SO
、SO![]() 、NH
、NH![]() 、CO
、CO![]()
C. 不能确定该溶液中是否含有NO![]()
D. 该溶液中一定含K+,且c(K+)= 0.1mol/L
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com