
【题目】填写下列空白:
(1)某元素的气态氢化物的化学式XH4 , 则其最高价氧化物对应的水化物的化学式为 .
(2)氧元素有三种核素16O、17O、18O,它们在自然界中所占的原子个数百分比分别为a%、b%、c%,则氧元素的相对原子质量为 .
(3)物质的量相同的H2O和D2O与足量钠反应,放出的气体的质量之比为 .
(4)X2﹣含中子N个,X的质量数为A,则1g X的氢化物中含质子的物质的量是mol.
(5)铷和另一种碱金属形成的合金4.6g与足量的水反应后,产生0.2g氢气,则此合金中另一碱金属可能是: .
【答案】
(1)H2XO3
(2)16a%+17b%+18c%
(3)1:2
(4)![]()
(5)Li
【解析】解:(1)元素X的气态氢化物的化学式为XH4 , 所以X的最低负价为﹣4价,所以元素R的最高正价为+4价,X的最高价氧化物的水化物的化学式为H2XO3 , 所以答案是:H2XO3;(2)16O、17O、18O在自然界中所占的原子个数百分比分别为:a%、b%、c%,则氧元素的近似相对原子质量为:16a%+17b%+18c%,所以答案是:16a%+17b%+18c%;(3)物质的量相同的H2O和D2O与足量钠反应生成的H2、D2物质的量相等,放出的气体的质量之比语气摩尔质量成正比,则生成气体的质量之比=2g/mol:4g/mol=1:2,所以答案是:1:2;(4)X2﹣含中子N个,X原子X2﹣含有中子数相同,则X原子的质子数=A﹣N,X的氢化物为H2X,该氢化物中含有质子数=A﹣N+2,1gH2X的物质的量为: ![]() =
= ![]() mol,1g X的氢化物中含质子的物质的量是:
mol,1g X的氢化物中含质子的物质的量是: ![]() mol×A﹣N+2=
mol×A﹣N+2= ![]() mol, 所以答案是:
mol, 所以答案是: ![]() ; (5)氢气的物质的量为:
; (5)氢气的物质的量为: ![]() =0.1mol,由
=0.1mol,由
2M+2H2O═2MOH+ | H2↑ |
2 | 1 |
0.2mol | 0.1mol |
则金属的平均摩尔质量为: ![]() =21g/mol,
=21g/mol,
铷的摩尔质量为85.5g/mol,则另一种碱金属的摩尔质量一定小于21g/mol,碱金属元素中摩尔质量小于21g/mol的只有Li,则另一碱金属可能是Li,
所以答案是:Li.
【考点精析】解答此题的关键在于理解核素的相关知识,掌握核素符号:如2713Al、3216S、168O左上角为质量数,左下角为质子数.


科目:高中化学 来源: 题型:
【题目】下列的图示与对应的叙述相符的是
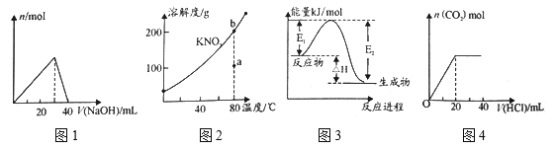
A. 图1表示向l00mL0.l mol·L-l的A1Cl3溶液中滴加1 mol·L-1的NaOH溶液时n [Al(OH)3]的变化情况
B. 图2表示KNO3的溶解度曲线,图中a点表示的溶液通过升温可以得到b点
C. 图3表示某一放热反应,若使用催化剂,E1、E2、△H都会发生改变
D. 图4表示向Na2CO3溶液中滴加稀盐酸时,产生n(CO2)的情况
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列化学肥料属于复合肥料的是( )
A. 尿素:CO(NH2)2 B. 重过磷酸钙:Ca(H2PO4)2
C. 氯化钾:KCl D. 磷酸二氢铵:NH4H2PO4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质中属于强电解质且能导电的是
①氢氧化钠溶液 ②硫酸钙固体 ③铜 ④蔗糖 ⑤三氧化硫 ⑥熔融氯化钠
A.①②⑤ B.①②⑥ C.③⑥ D.⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】可逆反应A(g)+B![]() C(g)+D,达到平衡时,下列说法不正确的是
C(g)+D,达到平衡时,下列说法不正确的是
A. 若B是气体,增大A的浓度会使B转化率增大
B. 若增大A的浓度,平衡体系颜色加深,D不一定是有颜色的气体
C. 升高温度,C百分含量减少,说明正反应是放热反应
D. 增大压强,平衡不移动,说明B是气体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对可逆反应4NH3(g)+5O2(g)![]() 4NO(g)+6H2O(g),下列叙述中正确的是
4NO(g)+6H2O(g),下列叙述中正确的是
A. 达到化学平衡时4v正(O2)=5v逆(NO)
B. 若单位时间内生成x mol NO的同时,消耗x mol NH3,则反应达到平衡状态
C. 达到化学平衡时,若增大容器的体积,则正反应速率减小,逆反应速率增大
D. 化学反应速率的关系是2v逆(NH3)=3v正(H2O)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A,B,C,D,E、F、G七种短周期元素,原子序数依次增大.由A、B形成的单质在一定条件下可生成气体X且X的水溶液呈碱性;D原子K层电子数是其M层电子数的2倍;E的简单阳离子与X具有相同电子数,且E的简单阳离子是同周期中简单离子半径最小的元素;F元素的原子最外层比次外层少两个电子,C和G的最外层电子数之和为13.则
(1)C在周期表中的位置为;
(2)写出:D在C单质中燃烧所生成淡黄色的固体的电子式
(3)A,B,D,E四种元素的原子半径由大到小的顺序为 . (用元素符号表示 )
(4)G的单质在反应中常作氧化剂,该单质的水溶液与F的低价氧化物反应的化学方程式为 .
(5)写出由A,C,D,F这四种元素共同组成的2种化合物在水溶液中发生反应的离子方程式: .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列解释物质用途或现象的反应方程式不准确的是
A. 硫酸型酸雨的形成会涉及反应2H2SO3+O2![]() 2H2SO4
2H2SO4
B. 工业上制取粗硅的化学方程式:SiO2+C![]() Si+CO2↑
Si+CO2↑
C. Na2S2O3溶液中加入稀硫酸:S2O32-+2H+=SO2+S↓+H2O
D. 成分为盐酸的洁厕灵与84消毒液混合使用易中毒:Cl-+ClO-+2H+=Cl2↑+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在2HCHO+NaOH(浓)→HCOONa+CH3OH中,甲醛( )
A. 仅被氧化 B. 仅被还原
C. 既未被氧化,又未被还原 D. 既被氧化,又被还原
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com