
【题目】CuSO4是一种重要化工原料,其制备和有关性质如图所示。
(1)现要用如图所示的浓硫酸来配制步骤①中所需要的1mol/L的稀硫酸480ml,需要用这种浓硫酸的体积为______ml。

(2)配制该稀硫酸所用到的玻璃仪器除玻璃棒、量筒、烧杯外还有_______、__________。
(3)下列操作会使所配溶液浓度偏低的是 _________。
A. 硫酸转移至容量瓶后,没有洗涤烧杯
B. 未冷却至室温就转移至容量瓶
C. 容量瓶中存在少量蒸馏水
D. 定容时俯视刻度 E.量取浓硫酸时量筒内有少量蒸馏水
(4)制取硫酸铜的途径①②③中,途径_________能更好地体现绿色化学的思想。
(5)配制1000ml 0.1mol/L的硫酸铜溶液,需用托盘天平称取________g胆矾。
【答案】27.2 500ml容量瓶 胶头滴管 AE ② 25.0
【解析】
(1)配制1mol/L的稀硫酸480ml,需要用500ml容量瓶,因此配制稀硫酸的体积为500ml,根据图示,浓硫酸的浓度c(浓硫酸)=![]() ,设需要用这种浓硫酸的体积为Vml,根据稀释过程溶质的量不变,列关系式1mol/L×500ml=18.4mol/L×Vml,解得:V=27.2ml;
,设需要用这种浓硫酸的体积为Vml,根据稀释过程溶质的量不变,列关系式1mol/L×500ml=18.4mol/L×Vml,解得:V=27.2ml;
答案为:27.2
(2)配制该稀硫酸所用到的玻璃仪器玻璃棒、量筒、烧杯外、500ml容量瓶、胶头滴管;
答案为:500ml容量瓶、胶头滴管
(3)根据![]() 来进行分析,
来进行分析,
A. 未洗涤,所配溶液的溶质的质量减少,因此浓度减小,故A符合;
B. 未冷却至室温就转移至容量瓶,容量瓶内溶液冷却后,体积会减小,浓度偏高,故B不符合;
C. 容量瓶有无水,对实验无影响,故C不符合;
D. 定容时仰视读数,所配溶液的体积偏小,浓度增大,故D不符合;
E. 量筒含有少量的水,导致量取的溶质的体积减少,浓度减小,故E符合;
答案选AE
(4)途径①会产生有毒的一氧化氮气体,污染空气;途径②![]() ,硫酸利用率高,且不产生有污染的物质,故最好;途径③产生二氧化硫,二氧化硫有毒对环境有危害,且硫酸利用率低。
,硫酸利用率高,且不产生有污染的物质,故最好;途径③产生二氧化硫,二氧化硫有毒对环境有危害,且硫酸利用率低。
答案为:②;
(5)根据硫酸铜守恒,溶液中硫酸铜的物质的量等于胆矾中硫酸铜的物质的量,因此有![]() 。
。
答案为:25.0;


 小学生10分钟口算测试100分系列答案
小学生10分钟口算测试100分系列答案科目:高中化学 来源: 题型:
【题目】按要求回答下列问题:
(1)氯气的制取方法有很多,写出实验室用MnO2来制取氯气的离子方程式__________。
(2)工业炼铁通常在___________设备中进行,需要用到铁矿石、焦炭、__________和空气。
(3)氯化铁溶液通常应用于印刷电路板制作,写出其反应的离子方程式___________。
(4)请写出红热的炭与浓硫酸反应的化学方程式__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】白藜芦醇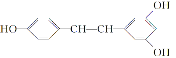 广泛存在于食物(例如桑椹、花生,尤其是葡萄)中,它可能具有抗癌性。下列关于白藜芦醇的说法错误的是( )
广泛存在于食物(例如桑椹、花生,尤其是葡萄)中,它可能具有抗癌性。下列关于白藜芦醇的说法错误的是( )
A. 白藜芦醇属于三元醇,能与Na反应产生H2
B. 能与NaOH反应,1 mol 该化合物最多能消耗NaOH 3 mol
C. 能使FeCl3溶液显色
D. 能与浓溴水反应,1 mol 该化合物最多能消耗溴6 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】取10g粗铁加入足量稀硫酸中,共收集到5.6L氢气(标准状况),则粗铁中混有的杂质不可能是( )
A. Cu和Mg B. Mg和Al C. Al 和 Si D. SiO2和Zn
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将一定质量的铜片加入到20 mL某浓度的浓硝酸中,充分反应后,铜片全部溶解,并收集到标准状况下的混合气体共896mL(假设[体中只有NO和NO2)。向反应后所得溶液中逐滴滴加lmol/L的NaOH溶液,产生沉淀质量与加入NaOH溶液体积(单位: mL)的关系如图所示。回答下列问题:
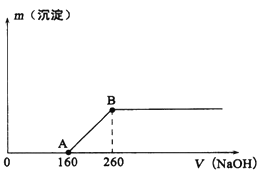
(1)B点所表示溶液中只含一种溶质,该物质是______(填化学式)。
(2)收集的气体中,NO2的物质的量为_______mol。
(3)原浓硝酸的浓度为_______mol/L。
(4)欲使铜与硝酸产生的混合气体在氢氧化钠溶液中全部转化为硝酸钠,至少需要30%的双氧水______g(保留两位有效数字)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上制备下列物质的生产流程合理的是( )
A. 由铝土矿冶炼铝:铝土矿![]() Al2O3
Al2O3![]() AlCl3
AlCl3![]() Al
Al
B. 从海水中提取镁:海水![]() Mg(OH)2
Mg(OH)2![]() MgO
MgO![]() Mg
Mg
C. 由NaCl制漂白粉:饱和食盐水![]() Cl2
Cl2![]() 漂白粉
漂白粉
D. 由黄铁矿制硫酸:黄铁矿![]() SO2
SO2![]() SO3
SO3![]() H2SO4
H2SO4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以高硫铝土矿(主要成分为Al2O3、Fe2O3,还含有少量FeS2)为原料,生产氧化铝并获得Fe3O4的部分工艺流程如图,下列叙述错误的是( )
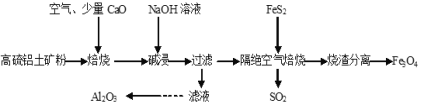
A.烧渣分离可以选择用磁铁将烧渣中的Fe3O4分离出来
B.隔绝空气焙烧时理论上反应消耗的n(FeS2)∶n(Fe2O3)=1∶5
C.向滤液中通入过量CO2、过滤、洗涤、灼烧沉淀可制得Al2O3
D.加入CaO可以减少SO2的排放同时生成建筑材料CaSO4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,KHS溶液里存在下列平衡:a.HS-+H2O ![]() H3O++S2- b.HS-+H2O
H3O++S2- b.HS-+H2O![]() OH-+H2S。
OH-+H2S。
(1)平衡a是_______平衡(填“电离”或“水解”,下同),平衡b是_______平衡。
(2)向KHS溶液中加入少量NaOH固体,c(S2-)将__________(填“增大”、“减小”或“不变”,下同),向KHS溶被中通入HCl时,c(HS-)将__________。
(3)向KHS溶液中加入CuSO4溶液,有黑色沉淀(CuS)产生,则平衡a__________移动(填“正向”、“逆向”或“不”,下同),平衡b__________移动。
(4)在KHS溶液中,c(OH-)-c(H+)=____________________。
(5)向KHS溶液中加入AlCl3溶液,产生的现象为______________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某溶液中含有Ba2+,Cu2+,Ag+,现用NaOH溶液、盐酸和Na2SO4溶液将这三种离子逐一沉淀分离。其流程图如右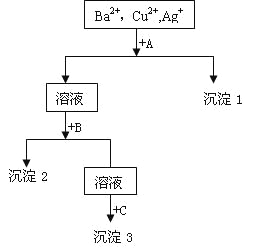
(1)沉淀的化学式:沉淀1___________,沉淀2__________,沉淀3____________;
(2)写出混合液+A的离子方程式________________________________________;
溶液+B的离子方程式_____________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com