
【题目】白藜芦醇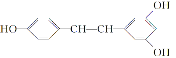 广泛存在于食物(例如桑椹、花生,尤其是葡萄)中,它可能具有抗癌性。下列关于白藜芦醇的说法错误的是( )
广泛存在于食物(例如桑椹、花生,尤其是葡萄)中,它可能具有抗癌性。下列关于白藜芦醇的说法错误的是( )
A. 白藜芦醇属于三元醇,能与Na反应产生H2
B. 能与NaOH反应,1 mol 该化合物最多能消耗NaOH 3 mol
C. 能使FeCl3溶液显色
D. 能与浓溴水反应,1 mol 该化合物最多能消耗溴6 mol
科目:高中化学 来源: 题型:
【题目】某澄清溶液中含有下表离子中的一种或多种。分别取它的水溶液两份进行实验,结果如下:
阳离子 | Fe2+、Fe3+、Al3+ |
阴离子 | SO32-、CO32-、SiO32-、I-、NO3- |
①向一份溶液中加入过量盐酸,产生气泡,溶液颜色变深,但仍澄清;
②继续向①溶液中加入少许四氯化碳,震荡,静置,下层呈现紫红色,上层溶液呈现黄色;
③向另一份溶液中加入过量氢氧化钠溶液,产生沉淀的质量与加入碱液的体积关系如图所示。
根据以上信息,回答下列问题:
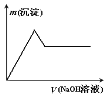
(1)原溶液中肯定含有的离子是______________________________________________;
(2)①中生成的气体是______________(填化学符号),它具有的性质是_____________(填字母序号);
A.无色无味 B.能被NaOH溶液吸收 C.属于大气污染物 D.难溶于水
(3)①中发生反应的离子方程式有_______________________________________________。
(4)③中沉淀溶解的化学反应方程式是________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室常用加热高锰酸钾的方法制取少量氧气。
(1)现在欲制取标准状况下1.12L氧气,需要消耗高锰酸钾________g;
(2)反应产生的MnO2经分离出来,与足量浓盐酸反应,其中被氧化的HCl的物质的量是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】足量锌与一定量浓H2SO4充分在加热下反应生成会SO2和H2的混合气体。现有甲乙两研究小组分别实验探究:
(1)甲研究小组按下图实验验证锌与浓硫酸反应生成物中含有SO2和H2。取一定量的Zn置于b中,向a中加入100mL 18mol·L-1的浓硫酸,经过一段时间,恰好完全反应。
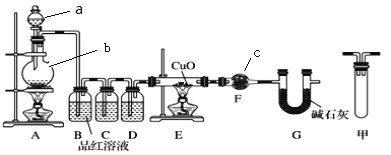
①填写仪器名称:c___________。
②实验开始前应先检验装置的气密性,请回答如何检验装置A的气密性___________。
③用化学方程式表示产生SO2的原因______________。
④U型管G的作用为__________。
⑤有同学认为A、B间应增加图中的甲装置,该装置的作用为__________。
⑥实验结束后测得装置F增重18.0g,计算实验开始时加入的Zn的质量为________g。你认为实际消耗Zn的质量应比计算值____________。(填“大”、“小”或“相同”)
(2)乙研究小组为了探究锌与稀硫酸反应过程中的速率及能量的变化,进行以下实验,分析影响反应速率的因素。
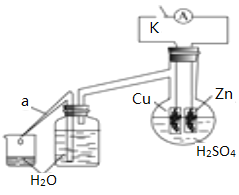
实验时,从断开K开始,每间隔1分钟,交替断开或闭合K,并连续计数每1分钟内从a管流出的水滴数,得到的水滴数如下表所示:
1分钟水滴数(断开K) | 34 | 59 | 86 | 117 | … | 102 |
1分钟水滴数(闭合K) | 58 | 81 | 112 | 139 | … | 78 |
分析反应过程中的水滴数,请回答:
由水滴数58>34、81>59,说明在反应初期,闭合K时比断开K时的反应速率快,主要原因是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲、乙两烧瓶中各盛有100mL 3mol·L-1的盐酸和氢氧化钾溶液;向两烧瓶中分别加入等质量的铝粉,反应结束测得生成的气体体积甲∶乙=2∶3(相同状况),则加入铝粉的质量为( )
A. 2.7g B. 3.6g C. 5.04g D. 4.05g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某天然拒食素具有防御非洲大群蚯蚓的作用,其结构简式为 (未表示出原子或原子团的空间排列)。该拒食素与下列某试剂充分反应,所得有机物分子的官能团数目增加,则该试剂是( )
(未表示出原子或原子团的空间排列)。该拒食素与下列某试剂充分反应,所得有机物分子的官能团数目增加,则该试剂是( )
A. H2B. Br2的CCl4溶液
C. HBrD. Ag(NH3)2OH溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列选项中所示的物质转化过程中未涉及到氧化还原反应的是
A.Fe3O4![]() FeI2
FeI2![]() Fe(OH)2
Fe(OH)2
B.SiO2![]() Si
Si![]() SiCl4
SiCl4
C.NaCl![]() NaHCO3
NaHCO3![]() Na2CO3
Na2CO3
D.SO2![]() H2SO4
H2SO4![]() Na2SO4
Na2SO4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CuSO4是一种重要化工原料,其制备和有关性质如图所示。
(1)现要用如图所示的浓硫酸来配制步骤①中所需要的1mol/L的稀硫酸480ml,需要用这种浓硫酸的体积为______ml。

(2)配制该稀硫酸所用到的玻璃仪器除玻璃棒、量筒、烧杯外还有_______、__________。
(3)下列操作会使所配溶液浓度偏低的是 _________。
A. 硫酸转移至容量瓶后,没有洗涤烧杯
B. 未冷却至室温就转移至容量瓶
C. 容量瓶中存在少量蒸馏水
D. 定容时俯视刻度 E.量取浓硫酸时量筒内有少量蒸馏水
(4)制取硫酸铜的途径①②③中,途径_________能更好地体现绿色化学的思想。
(5)配制1000ml 0.1mol/L的硫酸铜溶液,需用托盘天平称取________g胆矾。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】1.92gFe和Fe2O3的混合物溶于200mL盐酸中,生成0.336L(标准状况下)氢气,向反应后的溶液中加入KSCN检验,溶液不显红色。为让溶液中的金属离子恰好完全沉淀,消耗了400mL0.750 mol/L的氢氧化钠溶液。则:
(1)产生的氢气中所含的分子数为___。
(2)混合物中Fe和Fe2O3的物质的量之比为___。
(3)盐酸的物质的量浓度为___mol·L-1。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com