
【题目】某温度下,![]()
![]() 分别在溶液中达到沉淀溶解平衡后,改变溶液
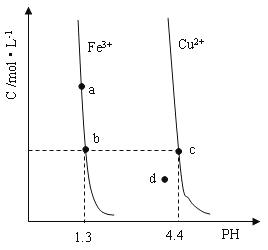
分别在溶液中达到沉淀溶解平衡后,改变溶液![]() ,金属阳离子浓度的变化如图所示。据图分析,下列判断错误的是
,金属阳离子浓度的变化如图所示。据图分析,下列判断错误的是
A.![]()
B.加适量![]() 固体可使溶液由
固体可使溶液由![]() 点变到
点变到![]() 点
点
C.![]()
![]() 两点代表的溶液中
两点代表的溶液中![]() 与
与![]() 乘积相等
乘积相等
D.![]() 、
、![]() 分别在
分别在![]() 、
、![]() 两点代表的溶液中达到饱和
两点代表的溶液中达到饱和
【答案】B
【解析】
A.由b、c两点对应数据可比较出KSP[Fe(OH)3]与KSP[Cu(OH)2]的大小,KSP[Fe(OH)3]=c(Fe3+)(OH-)3=c(Fe3+)(10-12.7)3,KSP[Cu(OH)2]=c(Cu2+)(OH-)2=c(Cu2+)(10-9.6)2,因c(Fe3+)=c(Cu2+),故KSP[Fe(OH)3]<KSP[Cu(OH)2],选项A正确;
B.向溶液中加入NH4Cl固体,不会导致溶液中的c(OH-)增大,故不能使溶液由a点变到b点,选项B错误;
C.只要温度不发生改变,溶液中c(H+)与c(OH-)的乘积(即Kw)就不变,该题中温度条件不变,故c、d两点代表的溶液中c(H+)与c(OH-)的乘积相等,选项C正确;
D.b、c两点分别处在两条的沉淀溶解平衡曲线上,故两点均代表溶液达到饱和,选项D正确;
答案选B。


 名师指导期末冲刺卷系列答案
名师指导期末冲刺卷系列答案科目:高中化学 来源: 题型:
【题目】二氢弥猴桃内酯(J)是一种调配烟草用香精,制备该物质的合成路线如下:

已知:A、B、C中含有一种相同的官能团,B和C中均含有两个甲基。
(1)A的化学名称是_________;Ⅰ中所含官能团的名称是_________。
(2)A生成B或C的反应类型是_________,G生成H的反应类型是_________。
(3)A在催化剂作用下发生加聚反应,生成的常见高分子化合物的结构简式为_________。
D生成E所用的试剂为乌洛托品,其相对分子质量为140,可由甲醛与氨气以物质的量之比3∶2反应脱去水得到,乌洛托品分子中有4个六元环,所有氢原子化学环境相同,乌洛托品的分子式为_________,结构简式为_____________________________。
(4)化合物E与足量H2 在催化剂及加热条件下反应的化学方程式为________________________。
(5)芳香族化合物X是J 的同分异构体,1mol X能与2mol NaOH 反应,X的核磁共振氢谱有5组峰,且峰面积之比为1∶1∶2∶6∶6,写出一种符合条件的X的结构简式:__________________。
(6)写出以1-丙醇为原料(其他试剂任选)制备2-丁烯酸的合成路线____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】立德粉ZnS·BaSO4(也称锌钡白),是一种常用白色颜料。回答下列问题:
以重晶石(BaSO4)为原料,可按如下工艺生产立德粉:

①在回转窑中重晶石被过量焦炭还原为可溶性硫化钡,该过程的化学方程式为____________________________。回转窑尾气中含有有毒气体,生产上可通过水蒸气变换反应将其转化为CO2和一种清洁能源气体,该反应的化学方程式为_______________________。
②沉淀器中反应的离子方程式为___________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一水合甘氨酸锌是一种矿物类饲料添加剂,结构简式如图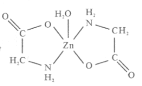 。
。
(1)基态Zn2+的价电子排布式为_______________;一水合甘氨酸锌中所涉及的非金属元素电负性由大到小的顺序是___________________。
(2)甘氨酸(H2N-CH2-COOH)中N的杂化轨道类型为______________;甘氨酸易溶于水,试从结构角度解释___________________________________________。
(3)一水合甘氨酸锌中Zn2+的配位数为______________________。
(4) [Zn(IMI)4](ClO4)2是Zn2+的另一种配合物,IMI的结构为![]() ,则1 mol IMI中含有________个σ键。
,则1 mol IMI中含有________个σ键。
(5)常温下IMI的某种衍生物与甘氨酸形成的离子化合物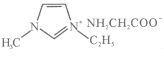 为液态而非固态,原因是________________________________________。
为液态而非固态,原因是________________________________________。
(6)Zn与S形成某种化合物的晶胞如图Ⅰ所示。
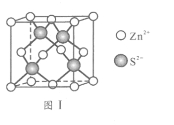
①Zn2+填入S2-组成的________________空隙中;
②由①能否判断出S2- 、Zn2+相切?_________(填“能”或“否”);已知晶体密度为d g/cm3,S2-半径为a pm,若要使S2-、Zn2+相切,则Zn2+半径为____________________pm(写计算表达式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据下列实验操作和现象所得出的结论正确的是
选项 | 实验操作和现象 | 结论 |
A | 向苯酚浊液中滴加Na2CO3溶液,浊液变清 | 苯酚的酸性强于H2CO3的酸性 |
B | 向碘水中加入等体积CCl4,振荡后静置,上层接近无色,下层显紫红色 | I2在CCl4中的溶解度大于在水中的溶解度 |
C | 向CuSO4溶液中加入铁粉,有红色固体析出 | Fe2+的氧化性强于Cu2+的氧化性 |
D | 向NaCl、NaI的混合稀溶液中滴入少量稀AgNO3溶液,有黄色沉淀生成 | Ksp(AgCl) >Ksp(AgI) |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】油脂是重要的营养物质.某天然油脂A可发生下列反应:
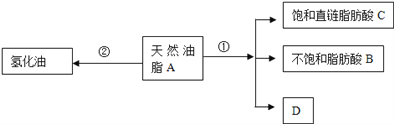
已知:A的分子式为C57H106O6.1mol该天然油脂A经反应①可得到1molD、1mol不饱和脂肪酸B和2mol直链饱和脂肪酸C.经测定B的相对分子质量为280,原子个数比为C:H:O=9:16:1;
(1)写出B的分子式:________________________;
(2)写出反应①的反应类型:____________;C的名称(或俗称)是_________;
(3)近日,电视媒体关于“氢化油危害堪比杀虫剂”的报道引发轩然大波,反应②为天然油脂的氢化过程.下列有关说法不正确的是_______________;
a.氢化油又称人造奶油,通常又叫硬化油.
b.植物油经过氢化处理后会产生副产品反式脂肪酸甘油酯,摄入过多的氢化油,容易堵塞血管而导致心脑血管疾病.
c.氢化油的制备原理是在加热植物油时,加入金属催化剂,通入氢气,使液态油脂变为半固态或固态油脂.
d.油脂的氢化与油脂的皂化都属于加成反应
(4)D和足量金属钠反应的化学方程式_____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】今有室温下四种溶液,下列有关叙述不正确的是( )

A. ③和④中分别加入适量的醋酸钠晶体后,两溶液的pH均增大
B. ②和③两溶液等体积混合,所得溶液中c(H+)>c(OH-)
C. 分别加水稀释10倍,四种溶液的pH:①>②>④>③
D. V1L ④与V2L ①溶液混合后,若混合后溶液pH=7,则V1<V2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】W、P、Q、M是原子序数依次增大的短周期元素,a、b、c、d分别是这4种元素的单质,甲、乙、丙、丁分别是由这些元素组成的化合物。已知:Q是地壳中含量最高的金属元素;向甲的溶液中通入丙气体,产生白色沉淀;丙气体溶于水,溶液呈碱性。它们之间的转化关系如图所示。下列说法正确的是( )
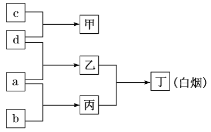
A.元素非金属性:M>W>P
B.丁是含有共价键的离子化合物
C.P的氧化物的水化物一定是强酸
D.甲、乙、丙、丁四种化合物均能抑制水的电离
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表中的实线表示元素周期表的部分边界。
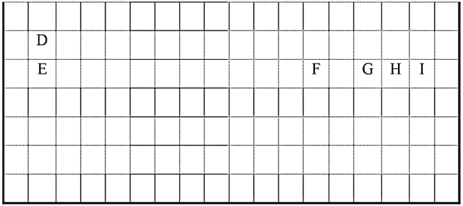
(1)请在上表中用实线补出元素周期表的上边界。_____________
(2)某主族元素原子的核外电子排布为: ,该元素在元素周期表中的位置为_______________。
,该元素在元素周期表中的位置为_______________。
(3)元素I的非金属性________(填“强于”或“弱于”)元素H,用原子结构的观点解释原因:同周期元素随着原子序数的递增,______________________,非金属性增强。设计实验证明元素E的金属性强于元素F:__________________________。
(4)处于周期表中对角线位置(左上方和右下方) 的元素,其性质具有相似性,称为“对角线规则”。元素D与F的单质及其化合物性质相似,如D、DO、D(OH)2与NaOH溶液都能反应生成Na2DO2等物质。回答下列问题。
①写出F的单质与氢氧化钠溶液反应的离子方程式___________________________。
②鉴别元素D与E的氢氧化物可用试剂是_________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com