
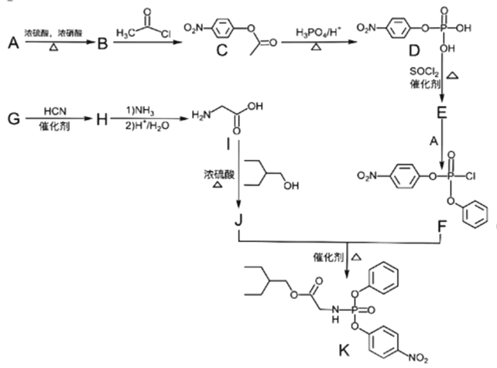
【题目】药物瑞德西韦(Remdesivir))对2019年新型冠状病毒(2019-nCoV)有明显抑制作用;K为药物合成的中间体,其合成路线如下:
已知:1. ![]()
2. ![]()
回答下列问题:
(1)检验A中官能团的方法是________________,B的化学名称为_________。
(2)C→D的反应类型是_____________,J+F→K的反应类型是___________。
(3)I中官能团的名称为___________________,F的分子式是_____________。
(4)E的结构简式为_________________________________。
(5)由G生成H的化学反应方程式为______________________________________。
(6)X是C同分异构体,写出满足下列条件的X的结构简式__________________。
①苯环上含有硝基且苯环上只有一种氢原子;
②遇FeCl3溶液发生显色反应;
③1mol的X与足量金属Na反应可生成2gH2 。
(7)设计由苯甲醇为原料制备化合物 。
。
___________________________________________________________________________。
【答案】加入FeCl3溶液成紫色 对硝基苯酚(4-硝基苯酚) 取代反应 取代反应 羧基、氨基 C12H9O5NPCl  HCHO+HCN
HCHO+HCN![]() HO
HO![]() CN
CN 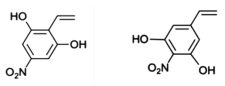

【解析】
(1)-(6)A发生取代反应生成B,B发生信息1的反应生成C,根据C结构简式知,B为![]() ,则A为
,则A为![]() ,D发生信息①的反应生成E,E中含两个Cl原子,则E为
,D发生信息①的反应生成E,E中含两个Cl原子,则E为 ,E和A发生取代反应生成F,G发生信息②的反应生成H,H发生取代反应、水解反应得到I,根据I结构简式知H为HOCH2CN,G为HCHO,I发生酯化反应生成J,F、J发生取代反应生成K,J为
,E和A发生取代反应生成F,G发生信息②的反应生成H,H发生取代反应、水解反应得到I,根据I结构简式知H为HOCH2CN,G为HCHO,I发生酯化反应生成J,F、J发生取代反应生成K,J为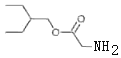 ;
;
(7)以苯甲醇为原料制备化合物 ,
, 可由
可由![]() 发生酯化反应得到,
发生酯化反应得到,![]() 可由
可由![]() 水解得到,苯甲醛和HCN发生加成反应得到
水解得到,苯甲醛和HCN发生加成反应得到![]() ,苯甲醇发生氧化反应生成苯甲醛。
,苯甲醇发生氧化反应生成苯甲醛。
(1)A为![]() ,向A中加入FeCl3溶液成紫色,即可证明A中含有酚羟基;B的结构简式为
,向A中加入FeCl3溶液成紫色,即可证明A中含有酚羟基;B的结构简式为![]() ,化学名称为对硝基苯酚(4-硝基苯酚);
,化学名称为对硝基苯酚(4-硝基苯酚);
(2)C→D为![]() 与H3PO4在酸性条件下,加热发生取代反应,生成
与H3PO4在酸性条件下,加热发生取代反应,生成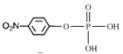 ;F、J发生取代反应生成K,则J+F→K的反应类型是取代反应;
;F、J发生取代反应生成K,则J+F→K的反应类型是取代反应;
(3)I的结构简式为![]() ,含有官能团的名称为羧基、基,F的结构简式为
,含有官能团的名称为羧基、基,F的结构简式为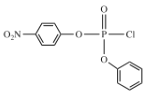 ,其分子式是C12H9O5NPCl;
,其分子式是C12H9O5NPCl;
(4)由分析知:E的结构简式为 ;
;
(5)HCHO和HCN发生加成反应生成HOCH2CN的化学反应方程式为HCHO+HCN![]() HOCH2CN;
HOCH2CN;
(6)X是C的同分异构体,X符合下列条件:①苯环上含有硝基且苯环上只有一种氢原子;②遇FeCl3溶液发生显色反应,说明含有酚羟基;③1mol的X与足量金属Na反应可生成2gH2,说明含有2个-OH,则符合条件的结构简式为 、
、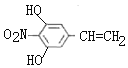 ;
;
(7)以苯甲醇为原料制备化合物 ,
, 可由
可由![]() 发生酯化反应得到,
发生酯化反应得到,![]() 可由
可由![]() 水解得到,苯甲醛和HCN发生加成反应得到
水解得到,苯甲醛和HCN发生加成反应得到![]() ,苯甲醇发生氧化反应生成苯甲醛,其合成路线为
,苯甲醇发生氧化反应生成苯甲醛,其合成路线为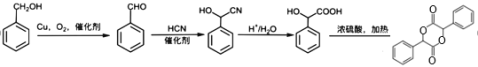 。
。


科目:高中化学 来源: 题型:
【题目】某学习小组以电路板刻蚀液(含有大量Cu2+、Fe2+、Fe3+)为原料制备纳米Cu20,制备流程如下:
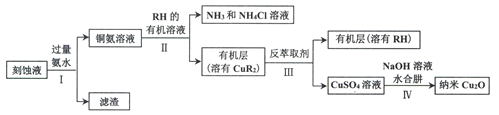
已知:①Cu2O在潮湿的空气中会慢慢氧化生成CuO,也易被还原为Cu; Cu2O不溶于水,极易溶于碱性溶液;Cu2O+2H+ =Cu2++Cu+H2O。
②生成Cu2O的反应:4Cu(OH)2+N2H4H2O=2Cu2O+N2↑+7H2O
请回答:
(1)步骤II,写出生成CuR2反应的离子方程式:____________________________
(2)步骤II,需对水层多次萃取并合并萃取液的目的是___________________________
(3)步骤III,反萃取剂为_____________
(4)步骤IV,①制备纳米Cu2O时,控制溶液的pH为5的原因是_______________
A. 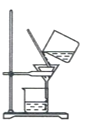 B.
B. 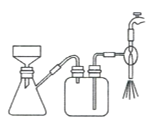 C.
C. 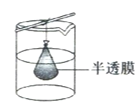
②从溶液中分离出纳米Cu2O采用离心法,下列方法也可分离Cu2O的是_________
③Cu2O干燥的方法是_________________
(5)为测定产品中Cu2O的含量,称取3.960g产品于锥形瓶中,加入30mL硫酸酸化的Fe2(SO4)3溶液(足量),充分反应后用0.2000 mol·L-1标准KMnO4溶液滴定,重复2~3次,平均消耗KMnO4溶液50.00mL。
①产品中Cu2O的质量分数为_______
②若无操作误差,测定结果总是偏高的原因是_____
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向绝热恒容密闭容器中通入SO2和NO2,一定条件下使反应![]() 达到平衡,正反应速率随时间变化的示意图如下所示。
达到平衡,正反应速率随时间变化的示意图如下所示。
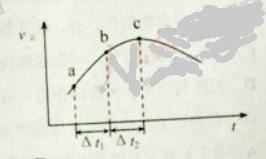
A. 反应在c 点达到平衡状态
B. 反应物浓度:![]() 点小于
点小于![]() 点
点
C. 反应物的总能量低于生成物的总能量
D. ![]() 时,SO2的转化率:
时,SO2的转化率:![]() 段小于
段小于![]() 段
段
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在300mL的密闭固定容器中,一定条件下发生Ni(s)+4CO(g) ![]() Ni(CO)4(g)的反应,该反应平衡常数(K)与温度(T)的关系如下表所示:
Ni(CO)4(g)的反应,该反应平衡常数(K)与温度(T)的关系如下表所示:
T/℃ | 25 | 80 | 230 |
K | 5×104 | 2 | 1.9×10﹣5 |
下列说法不正确的是( )。
A.上述生成Ni(CO)4(g)的反应为放热反应
B.230℃时,该反应的正反应为不自发的反应
C.80℃达到平衡时,测得n(CO)=0.3mol,则Ni(CO)4的平衡浓度为2 mol·L-1
D.25℃时反应Ni(CO)4(g) ![]() Ni(s)+4CO(g)的平衡常数为2×10-5
Ni(s)+4CO(g)的平衡常数为2×10-5
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关说法正确的是
A.常温下,![]() 溶液的
溶液的![]()
B.工业上电解饱和食盐水时,以石墨为阴极,铁棒为阳极
C.铅蓄电池放电时,正极电极反应为:![]()
D.常温下,在AgCl悬浊液中加入少量NaCl饱和溶液,![]() 减小,
减小,![]() 减小
减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,部分物质的电离平衡常数如表所示:
化学式 |
|
| HClO |
|
|
电离平衡常数 |
|
|
|
|
|
(1)25℃时,等浓度的![]() 溶液、
溶液、![]() 溶液、
溶液、![]() 溶液,3种溶液的pH由大到小的顺序为________。
溶液,3种溶液的pH由大到小的顺序为________。
(2)工业上可用氨水除去尾气![]() 。将
。将![]() 通入氨水中,当
通入氨水中,当![]() 降至
降至![]() _____。
_____。
(3)常温下,用![]() 溶液滴定
溶液滴定![]() 溶液所得滴定曲线如图:
溶液所得滴定曲线如图:
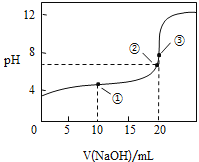
①在整个实验过程中,不需要的仪器或用品是 ______(填序号).
![]() 容量瓶 b 锥形瓶c 滴定管夹d 漏斗e 玻璃棒f 滴定管
容量瓶 b 锥形瓶c 滴定管夹d 漏斗e 玻璃棒f 滴定管
②到达滴定终点的标志是 _____________ .
③下列操作会导致测定结果偏高的是 ______ .
A 碱式滴定管在装液前未用标准NaOH溶液润洗
B 滴定过程中,锥形瓶摇荡得太剧烈,锥形瓶内有液滴溅出
C 碱式滴定管尖嘴部分在滴定前没有气泡,滴定终点时发现气泡
D 达到滴定终点时,仰视读数
④如图点①所示溶液中![]() __________
__________![]() 填“>”“<”或“=”,下同,点②所示溶液中:
填“>”“<”或“=”,下同,点②所示溶液中:![]() ________
________![]() ,点③所示溶液中所有离子浓度由大到小的顺序为:_________。
,点③所示溶液中所有离子浓度由大到小的顺序为:_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】同温同压下,等质量的二氧化硫气体和二氧化碳气体的比较中,正确的是( )
A.密度比为11∶16B.物质的量比为16∶11
C.体积比为11∶16D.分子个数比为16∶11
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】华法林(Warfarin)又名杀鼠灵,为心血管疾病的临床药物。其合成路线(部分反应条件略去) 如下所示:
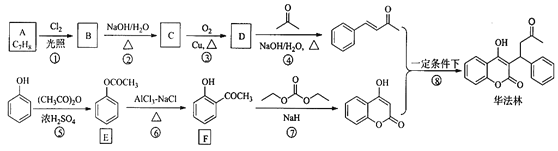
回答下列问题:
(1)A 的名称为________,E 中官能团名称为________。
(2)B 的结构简式为________。
(3)由 C 生成 D 的化学方程式为___________
(4)⑤的反应类型为_________,⑧的反应类型为________。
(5)F 的同分异构体中,同时符合下列条件的同分异构体共有___________种。
a.能与 FeCl3 溶液发生显色反应 b.含有-CHO
其中核磁共振氢谱为五组峰的结构简式为___________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如果发现了原子序数为114的元素,下列对它的叙述中正确的是( )
①位于第七周期②非金属元素③最外电子层有4个电子④没有放射性⑤属于第IVA族元素⑥属于锕系元素.
A.①③⑤B.②⑥C.①③⑥D.③④⑤
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com