
【题目】在下列物质转化中,A是一种酸式盐,D的相对分子质量比C的相对分子质量大16,E是酸,当X无论是强酸还是强碱时,都有如下的转化关系:
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
当X是强酸时,A、B、C、D、E均含同一种元素;当X是强碱时,A、B、C、D、E均含另外同一种元素。请回答:
(1)A是________, Z是________。
(2)当X是强酸时,写出B生成C的化学方程式:___________________。
(3)当X是强碱时,E是________,写出E和铜反应生成C的化学方程式:__________________。
【答案】NH4HSH2O2H2S+3O2![]() 2SO2+2H2OHNO33Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O
2SO2+2H2OHNO33Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O
【解析】D的相对分子质量比C的相对分子质量大16,说明Y是氧气,D是氧化物,E又是酸,说明Z是H2O,从B到D两次氧化,生成酸,这样的元素不多可能是N和S,A既能和酸反应又能和碱反应,说明是铵盐,再结合元素,是正盐,可推测为(NH4)2S,当X是强酸时,B、C、D、E分别为H2S 、SO2、SO3、H2SO4。当X是强碱时, B、C、D、E分别为NH3、NO、NO2、HNO3。由以上分析可知(1)A是(NH4)2S, Z是H2O;(2)当X是强酸时, B是H2S, C是SO2,B生成C的化学方程式2H2S+3O2![]() 2SO2+2H2O;(3)当X是强碱时,B、C、D、E分别为NH3、NO、NO2、HNO3, 稀硝酸和铜反应生成NO,化学方程式是3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O。
2SO2+2H2O;(3)当X是强碱时,B、C、D、E分别为NH3、NO、NO2、HNO3, 稀硝酸和铜反应生成NO,化学方程式是3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O。


 应用题天天练四川大学出版社系列答案
应用题天天练四川大学出版社系列答案科目:高中化学 来源: 题型:
【题目】有四种物质的量浓度相等、且都由一价阳离子A+和B+及一价阴离子X-和Y-组成的盐
溶液。据测定常温下AX和BY溶液的pH=7,AY溶液的pH>7,BX溶液的pH<7,由此判断不水解的盐是( )
A.BX B.AX C.AY D.BY
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各表述与示意图一致的是( )
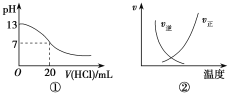
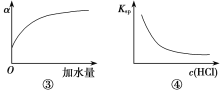
A.图①表示25 ℃时,用0.1 mol·L-1盐酸滴定20 mL 0.1 mol·L-1NaOH溶液,溶液的pH随加入盐酸体积的变化
B.图②中曲线表示反应N2(g)+O2(g)2NO(g) ΔH>0,正、逆反应速率随温度的变化
C.图③中曲线表示10 mL 0.01 mol·L-1醋酸的电离度α随加水量的变化
D.图④中曲线表示AgCl的溶度积Ksp随盐酸浓度c(HCl)的变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】水是极弱的电解质,改变温度或加入某些电解质会影响水的电离。请回答下列问题:
(1)纯水在100 ℃时,pH=6,该温度下0.1 mol·L-1的NaOH溶液的pH=________。
(2)25 ℃时,向水中加入少量碳酸钠固体,得到pH为11的溶液,其水解的离子方程式为_________________,由水电离出的c(OH-)=________ mol·L-1。
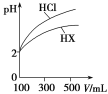
(3)体积均为100 mL、pH均为2的盐酸与一元酸HX,加水稀释过程中pH与溶液体积的关系如图所示,则HX是________(填“强酸”或“弱酸”),理由是______________________________。
(4)电离平衡常数是衡量弱电解质电离程度强弱的物理量。已知:
化学式 | 电离平衡常数(25 ℃) |
HCN | K=4.9×10-10 |
CH3COOH | K=1.8×10-5 |
H2CO3 | K1=4.3×10-7、K2=5.6×10-11 |
①25 ℃时,等浓度的NaCN溶液、Na2CO3溶液和CH3COONa溶液,溶液的pH由大到小的顺序为________(填化学式)。
②25 ℃时,在0.5 mol·L-1的CH3COOH溶液中由CH3COOH电离出的c(H+)约是由水电离出的c(H+)的________倍。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】黄铜矿(CuFeS2)是制取铜及其化合物的主要原料之一,还可以制备硫及铁的化合物。
(1)冶炼铜的反应为8CuFeS2+21O2![]() 8Cu+4FeO+2Fe2O3+16SO2若CuFeS2中Fe的化合价为+2,反应中被还原的元素是____________(填元素符号)。
8Cu+4FeO+2Fe2O3+16SO2若CuFeS2中Fe的化合价为+2,反应中被还原的元素是____________(填元素符号)。
(2)冶炼铜的主要流程如下:

气体A中的大气污染物可选用下列试剂中的_______吸收。
a.浓H2SO4 b.稀HNO3 c.NaOH溶液
用稀HNO3浸泡熔渣B,取少量所得溶液,滴加KSCN溶液后呈红色,一位同学由此得出该熔渣中铁元素价态为+3的结论。请指出该结论是否合理并说明理由________。
(3)冶炼出的铜可以发生下列反应
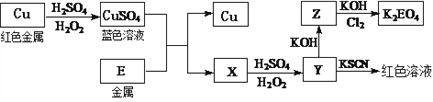
写出Cu溶于稀H2SO4和H2O2混合液的离子方程式:___________________。
写出Cl2将Z氧化为K2EO4的化学方程式:_____________________。
对于0.1molL-1 CuSO4溶液,正确的是_______
A、常温下,pH>7
B、 c(Cu2+)>c(SO42―)>c(H+)>c(OH―)
C、c(H+)+2 c(Cu2+)= 2c(SO42―)+c(OH―)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知温度T时水的离子积常数为KW,该温度下,将浓度为a mol·L-1的一元酸HA与bmol·L-1的一元碱BOH等体积混合,可判定该溶液呈中性的依据是( )
A. a=b
B. 混合溶液的pH=7
C. 混合溶液中,c(H+)=![]()
D. 混合溶液中,c(H+)+ c(B+)= c(OH-)+ c(A-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA代表阿伏加德罗常数的值,下列叙述正确的是
A. 60g丙醇中存在的共价键总数为10NA
B. 1L 0.1 mol·L-1的NaHCO3溶液中HCO3-和CO32-的离子数之和为0.1NA
C. 钠在空气中燃烧可生成多种氧化物,23g钠充分燃烧时转移电子数为1 NA
D. 235g核素![]() 发生裂变反应:
发生裂变反应:![]() +
+![]() +
+![]() +10
+10![]() ,净产生的中子(
,净产生的中子(![]() )数为10 NA
)数为10 NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】具有下列电子排布式的原子中,半径最大的是
A. 1s22s22p63s23p4 B. 1s22s22p3
C. 1s22s22p2 D. ls22s22p63s23p1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com