
����Ŀ�������缫������KOH��Һ�У�Ȼ��ֱ�������ͨ��CH4��O2����������������Ϊ����ȼ�ϵ�ء���֪����ȼ�ϵ�������缫�ϵķ�Ӧ�ֱ�ΪCH4��8e-��10OH-=CO32-��7H2O��2O2��8e-��4H2O=8OH-�������й�˵���д�����ǣ� ��
A.CH4�ڸ����Ϸ�Ӧ��O2�������Ϸ�Ӧ
B.�ŵ�����е������Һ�ļ��Լ���
C.�˵�����ڻ����Ѻ��͵��
D.�˵���л�ѧ��100%ת��Ϊ����
���𰸡�D
��������
A��CH4ȼ�ϵ���У�ȼ��ʧ���ӷ���������Ӧ������CH4�ڸ����Ϸ�Ӧ�������õ��ӷ�����ԭ��Ӧ������O2�������Ϸ�Ӧ����A��ȷ��
B�����ݵ���ܷ�ӦCH4��2O2��2OH��=![]() ��3H2O֪��OH���μӷ�Ӧ��������Һ��OH��Ũ�Ƚ��ͣ���Һ�ļ��Լ�������B��ȷ��
��3H2O֪��OH���μӷ�Ӧ��������Һ��OH��Ũ�Ƚ��ͣ���Һ�ļ��Լ�������B��ȷ��
C���õ�طŵ�ʱ�������Ի�������Ⱦ�����ʣ��������ڻ����Ѻ��͵�أ���C��ȷ��
D���˵���л�ѧ��ת��Ϊ���ܺ��������ܣ���D����
��ѡD��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���״�����Ҫ�Ļ���ԭ�ϣ��ֿɳ�Ϊȼ�ϡ����úϳ�������Ҫ�ɷ�ΪCO��CO2��H2���ڴ����������ºϳɼ״�������������Ӧ���£�
��CO(g)+2H2(g)![]() CH3OH(g) ��H1
CH3OH(g) ��H1
��CO2(g)+3H2(g)![]() CH3OH��g��+H2O(g) ��H2
CH3OH��g��+H2O(g) ��H2
��CO2(g)+H2(g)![]() CO(g)+H2O(g) ��H3
CO(g)+H2O(g) ��H3
�ش��������⣺
��1����֪��Ӧ���е���صĻ�ѧ�������������£�
��ѧ�� | H-H | C-O | C | H-O | C-H |
E/��kJ.mol-1�� | 436 | 343 | 1076 | 465 | 413 |
�ɴ˼�����H1=________kJ.mol-1����֪��H2=-58kJ.mol-1������H3=_________kJ.mol-1
��2����Ӧ�ٵĻ�ѧƽ�ⳣ��K�ı���ʽΪ_____________��ͼ1������ȷ��ӳƽ�ⳣ��K���¶ȱ仯��ϵ������Ϊ______�������߱����ĸ�������ж�������__________________��
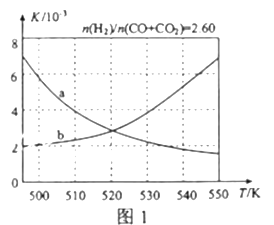 .
.
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ͼ��ֱ��ʾ�йط�Ӧ�ķ�Ӧ�����������仯�Ĺ�ϵ���ݴ��ж�����˵����ȷ���� �� ��
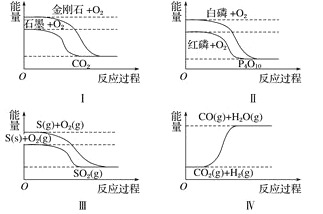
A.���ʯ��ʯī�ȶ�
B.����ת��Ϊ���������ȷ�Ӧ
C.S(g)+O2(g) === SO2(g)����H1 ��S(s)+O2(g) === SO2(g)����H2������H1>��H2
D.CO(g)+H2O(g) === CO2(g)+H2(g)����H>0
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ܱ������з�����Ӧ2SO2(g)��O2(g)![]() 2SO3(g)�����ijһʱ��SO2��O2��SO3���ʵ���Ũ�ȷֱ�Ϊ0.2 mol��L��1��0.1 mol��L��1��0.2 mol��L��1������Ӧ�ﵽƽ��ʱ���������ݿ��ܴ��ڵ���(����)
2SO3(g)�����ijһʱ��SO2��O2��SO3���ʵ���Ũ�ȷֱ�Ϊ0.2 mol��L��1��0.1 mol��L��1��0.2 mol��L��1������Ӧ�ﵽƽ��ʱ���������ݿ��ܴ��ڵ���(����)
A. SO2��O2Ũ�ȷֱ�Ϊ0.4 mol��L��1��0.2 mol��L��1
B. SO3Ũ��Ϊ0.25 mol��L��1
C. SO3Ũ��Ϊ0.4 mol��L��1
D. SO3��SO2Ũ�Ⱦ�Ϊ0.15 mol��L��1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ���¶��£���2L���ܱ������У�M��N������������ʵ�����ʱ��仯��������ͼ��ʾ��
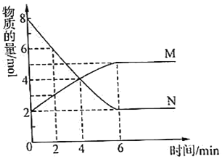
��1����Ӧ�Ļ�ѧ����ʽΪ___��
��2����Ӧ�ﵽ����ȵ�ʱ����__min����ʱ���ڵ�ƽ����Ӧ��������N����__��
��3����Ӧ�ﵽƽ��״̬ʱ���ų�6QkJ����������������ʼʱ����lmolN����Ӧ�ų�������Ϊ__��
A������QkJ B����QkJ C������QkJ D������2QkJ
��4���жϸ÷�Ӧ�ﵽƽ��״̬��������___��
�ٸ������£����淴Ӧ���ʶ�Ϊ��
�ڸ������£���������ƽ��Ħ���������ٷ����仯
�۸������£���������ѹǿ���ٷ����仯
�ܸ������£���λʱ��������2mol N��ͬʱ������1mol M
��5���ܼӿ췴Ӧ���ʵĴ�ʩ��___��
�������¶� ������������䣬�����������Ar
������ѹǿ���䣬�����������Ar ��ʹ�ô���
��6��һ���¶��£���һ������N2��H2����2L�̶�������ܱ������н��з�Ӧ��N2(g)+3H2(g)![]() 2NH3(g)������ʼʱ�������г���10mol��N2��15mol��H2��10minʱ�ﵽƽ�⣬���������NH3��Ũ��Ϊ2molL��1��10minʱN2��ת����Ϊ___��ƽ��ʱ��ѹǿ����ʼʱ��ѹǿ֮��Ϊ___��
2NH3(g)������ʼʱ�������г���10mol��N2��15mol��H2��10minʱ�ﵽƽ�⣬���������NH3��Ũ��Ϊ2molL��1��10minʱN2��ת����Ϊ___��ƽ��ʱ��ѹǿ����ʼʱ��ѹǿ֮��Ϊ___��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijͬѧ���һ��ȼ�ϵ��(����ͼ��ʾ)��Ŀ����̽���ȼҵԭ���ʹ�ͭ�ľ���ԭ����������װ����XΪ�����ӽ���Ĥ��
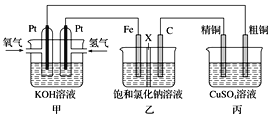
��1��ͨ�������ĵ缫Ϊ________ (��������)���õ缫��ӦʽΪ________��
��2��ʯī�缫Ϊ________ (������������)�������ܷ�Ӧ��ѧ����ʽΪ________����������缫��ʯī�缫����������Һ�����ֵ�������_________��
��3�������ͭ�к���п���������ʣ���װ���з�Ӧһ��ʱ�䣬����ͭ��ҺŨ�Ƚ�__________(�������С�����䡱)��
��4������������0.01mol O2�����о�ͭ����_________�ˡ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijͬѧ�����ͼ��ʾʵ�飬̽����Ӧ�е������仯��

�����ж���ȷ����
A. ��ʵ���֪��(a)��(b)��(c)���漰�ķ�Ӧ���Ƿ��ȷ�Ӧ
B. ��ʵ��(a) �еĵ���������Ƭ�������ۺ��ͷų���������������
C. ʵ��(c)�н����β����������Ϊ���ʽ������ʵ����û��Ӱ��
D. ����NaOH����ⶨ�к��ȣ���ⶨ���ƫ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������mA(s)��nB(g)qC(g) ��H��0�Ŀ��淴Ӧ����һ���¶��´�ƽ��ʱ��B�����������(B)��ѹǿp�Ĺ�ϵ��ͼ��ʾ���������йظ÷�Ӧ��������ȷ���ǣ� ��

A. m+n��qB. n��q
C. x��Ļ������v (��)��v (��)D. x���y��Ļ���������Ӧ����С
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��A��B��C��D��E�ֱ����������Ļ��������D��һ�ֺ��ɫ�����������Ӧ��ϵ��ͼ��ʾ��

������ͼ��ʾ�仯����Ҫ��ش��������⣺
��1��д��A��E�Ļ�ѧʽ��A__��E__��
��2��д�����м�����Ӧ�Ļ�ѧ����ʽ��
C��B��___��
B��D��___��
E��A��___��
��3��C�м���NaOH��Һ��������������__��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com