
【题目】某同学设计如图所示实验,探究反应中的能量变化。

下列判断正确的是
A. 由实验可知,(a)、(b)、(c)所涉及的反应都是放热反应
B. 将实验(a) 中的等质量的铝片换成铝粉后,释放出的热量有所增加
C. 实验(c)中将环形玻璃搅拌棒改为铁质搅拌棒对实验结果没有影响
D. 若用NaOH固体测定中和热,则测定结果偏高
 口算心算速算应用题系列答案
口算心算速算应用题系列答案 同步拓展阅读系列答案
同步拓展阅读系列答案科目:高中化学 来源: 题型:
【题目】照相底片定影时,常用定影液硫代硫酸钠(![]() )溶解未曝光的溴化银(
)溶解未曝光的溴化银(![]() ),生成含
),生成含![]() 的废定影液再向其中加入
的废定影液再向其中加入![]() 使
使![]() 中的银转化为
中的银转化为![]() ,使定影液再生。将
,使定影液再生。将![]() 在高温下转化为Ag,达到回收银的目的。回答下列问题:
在高温下转化为Ag,达到回收银的目的。回答下列问题:
(1)元素周期表中,铜、银、金位于同一副族相邻周期,则基态银原子的最外层电子排布式为__________________。
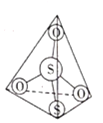
(2)![]() 离子结构如图所示,其中心硫原子的杂化方式为___________。基态S原子中,核外电子占据的最高能级的符号是__________,占据最高能级电子的电子云轮廓图为________形。
离子结构如图所示,其中心硫原子的杂化方式为___________。基态S原子中,核外电子占据的最高能级的符号是__________,占据最高能级电子的电子云轮廓图为________形。
(3)写出![]() 溶于
溶于![]() 溶液反应的离子方程式______。
溶液反应的离子方程式______。![]() 中存在的作用力有离子键、共价键、__________。
中存在的作用力有离子键、共价键、__________。
(4)在空气中灼烧![]() 生成
生成![]() 和
和![]() ,
,![]() 分子的空间构型为__________。分子中的大
分子的空间构型为__________。分子中的大![]() 键可用符号
键可用符号![]() 表示,其中m代表参与形成大
表示,其中m代表参与形成大![]() 键的原子数n代表参与形成大
键的原子数n代表参与形成大![]() 键的电子数(如苯分子中的大
键的电子数(如苯分子中的大![]() 键可表示为
键可表示为![]() ),则
),则![]() 中的大
中的大![]() 键应表示为_________。
键应表示为_________。
(5)![]() 的键角小于
的键角小于![]() 的键角,原因是_________________。
的键角,原因是_________________。
(6)用X射线衍射法可测定阿伏加德罗常数。由金的X射线衍射图像可知金的晶胞属于面心立方晶胞。若金原子的半径为![]() ,金的密度为
,金的密度为![]() ,摩尔质量为
,摩尔质量为![]() ,列出计算阿伏加德罗常数的算式_________(用含
,列出计算阿伏加德罗常数的算式_________(用含![]() 的表达式表示)。
的表达式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温时,向20mL 0.1 mol/L的CH3COOH溶液中逐滴滴加0.1 mol/L的NaOH溶液,滴入NaOH溶液的体积与溶液pH的变化如图所示。下列说法正确的是
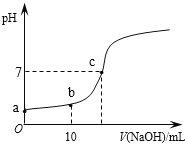
A. a点的pH=1
B. b点时,c (CH3COO—)=0.05mol/L
C. c点时,V(NaOH)=20mL
D. 反应过程中![]() 的值不断增大
的值不断增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将铂电极放置在KOH溶液中,然后分别向两极通入CH4和O2,即产生电流,称为甲烷燃料电池。已知甲烷燃料电池两个电极上的反应分别为CH4-8e-+10OH-=CO32-+7H2O,2O2+8e-+4H2O=8OH-。下列有关说法中错误的是( )
A.CH4在负极上反应,O2在正极上反应
B.放电过程中电解质溶液的碱性减弱
C.此电池属于环境友好型电池
D.此电池中化学能100%转化为电能
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室制取乙酸乙酯的装置如下图,按要求回答问题。
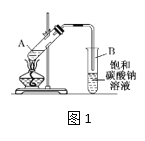
(1)写出制取乙酸乙酯的化学方程式_________________________。
(2)浓硫酸的作用是______,长导管末端不伸入饱和碳酸钠溶液的目的是______。
(3)上述实验中饱和碳酸钠溶液的作用是_______(填字母代号)。
A.反应掉乙酸和乙醇
B.反应掉乙酸并吸收部分乙醇
C.乙酸乙酯在饱和碳酸钠溶液中的溶解度比在水中的更小,有利于分层析出
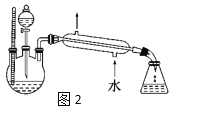
(4)某化学课外小组设计了图2所示的制取乙酸乙酯的装置(铁架台、铁夹、加热装置均已略去),与图1装置相比,此装置的主要优点有______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】恒温下,将a mol N2与b mol H2的混合气体通入一定容积的密闭容器中,发生如下反应:N2(g)+3H2(g)![]() 2NH3(g)
2NH3(g)
(1)若反应进行到某时刻t时,n(N2)=13mol,n(NH3)=6mol,
计算a=_______。
(2)反应达到平衡时,混合气体的体积为716.8L(标准状况下),其中NH3的百分含量(体积分数)为25%。计算:平衡时NH3的物质的量为_____________。
(3)原混合气体与平衡混合气体的总物质的量之比
n(始): n(平)=____________。
(4)原混合气体中a : b=_______________。
(5)达到平衡时,N2和H2的转化率![]() (N2):
(N2):![]() (H2)=______________。
(H2)=______________。
(6)平衡混合气体中n(N2): n(H2): n(NH3)=______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在容积为1 L的密闭容器中,加入5 mol A物质,在一定条件下同时发生下列两个反应:①2A(g)![]() 2B(g)+C(g);②A(g)
2B(g)+C(g);②A(g)![]() C(g)+D(g),当达到平衡时,测得c(A)= 2.5 mol/L,c(C)=2.0 mol/L.,则下列说法中正确的是
C(g)+D(g),当达到平衡时,测得c(A)= 2.5 mol/L,c(C)=2.0 mol/L.,则下列说法中正确的是
A.达到平衡时A的总转化率为40%
B.达到平衡时c(B)为1.0 mol/L
C.达到平衡时c(B)=2c(D)
D.达到平衡时c(D)=2c(B)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】改变0.1mol/L二元弱酸H2A溶液的pH,溶液中的H2A、HA-、A2-的物质的量分数![]() 随pH的变化如图所示已知[
随pH的变化如图所示已知[![]() ]。
]。
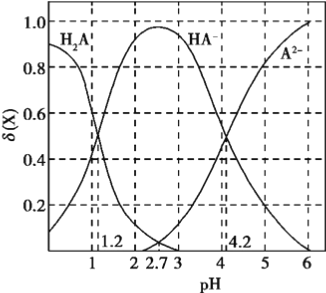
下列叙述错误的是
A. lg[K2(H2A)]=-4.2
B. pH=4.2时,c(HA-) = c(A2-) = c(H+)
C. pH=2.7时,c(HA-)>c(H2A)= c(A2-)
D. pH=1.2时,c(H2A)=c(HA-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】深埋在潮湿土壤中的铁管道,在硫酸盐还原菌作用下,能被硫酸根腐蚀,其电化学腐蚀原理如图示,下列与此原理有关说法错误的是
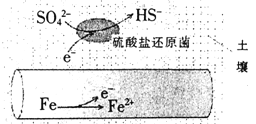
A. 正极反应为:SO42-+5H2O+8e-=HS-+9OH-
B. 输送暖气的管道不易发生此类腐蚀
C. 这种情况下,Fe腐蚀的最终产物为Fe2O3·xH2O
D. 管道上刷富锌油漆可以延缓管道的腐蚀
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com