
【题目】秦皮是一种常用的中药,具有抗炎镇痛、抗肿瘤等作用。“秦皮素”是其含有的一种有效成分,结构简式如图所示,有关其性质叙述不正确的是( )

A.该有机物分子式为C10H8O5
B.分子中有四种官能团
C.该有机物能发生加成、氧化、取代等反应
D.1mol该化合物最多能与3molNaOH反应
科目:高中化学 来源: 题型:
【题目】下列叙述中正确的是( )
A. 能电离出H+的化合物除水外都是酸,分子中含有几个氢原子它就是几元酸
B. 无机含氧酸分子中含有几个羟基,它就属于几元酸
C. 同一元素的含氧酸,该元素的化合价越高,其酸性越强,氧化性也越强
D. H3PO4和H2CO3分子中非羟基氧的个数均为1,但它们的酸性不相近,H3PO4是中强酸而H2CO3是弱酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】能源问题日益成为制约国际社会经济发展的瓶颈,越来越多的国家开始实行“阳光计划”,开发太阳能资源,寻求经济发展的新动力。
(1)太阳能热水器中常使用一种以镍或镍合金(含铁)空心球为吸收剂的太阳能吸热涂层,铁、镍基态原子未成对电子数各为_____________、________________。
(2)C60可用作储氢材料,已知金刚石中的C-C键的键长为0.154 nm,C60中C-C键键长为0.140~0.145 nm,有同学据此认为C60的熔点高于金刚石,你认为是否正确?_________,阐述理由:________________________________________________________________________。C60晶体(其结构模型如图)中每个C60分子周围与它距离最近且等距离的C60分子有_____个。
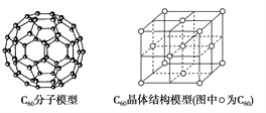
(3)富勒烯衍生物由于具有良好的光电性能,在太阳能电池的应用上具有非常光明的前途。富勒烯(C60)的结构如下图所示,分子中碳原子轨道的杂化类型为_________;1 mol C60分子中σ键的数目为________。科学家把C60和K掺杂在一起制造了一种富勒烯化合物,其晶胞如图所示,该物质在低温时是一种超导体。该物质的K原子和C60分子的个数比为________。
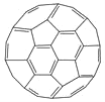
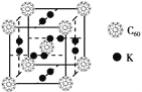
(4)继C60后,科学家又合成了Si60、N60,C、Si、N原子电负性由大到小的顺序是______________。Si60分子中每个硅原子只跟相邻的3个硅原子形成共价键,且每个硅原子最外层都满足8电子稳定结构,则Si60分子中π键的数目为______个。
(5)请解释如下现象:熔点:Si60>N60>C60,而破坏分子所需要的能量: N60>C60>Si60,其原因是:________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于密闭容器中进行的反应:P(g)+ Q(g)![]() R(g)+ S(g)下列说法可以充分说明这一反应已经达到化学平衡状态的是( )
R(g)+ S(g)下列说法可以充分说明这一反应已经达到化学平衡状态的是( )
A. P、Q、R、S的浓度相等
B. P、Q、R、S在密闭容器中共存
C. P、Q、R、S的浓度不再变化
D. 用P的浓度表示的化学反应速率与用Q的浓度表示的化学反应速率相等。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于甲、乙、丙、丁四个图像的说法中,正确的是( )


A.图甲表示向乙酸溶液中通入NH3过程中溶液导电性的变化
B.由图乙可知,若除去CuSO4溶液中的Fe3+可采用向溶液中加入适量CuO至pH在4左右
C.图丙表示25 ℃时,用0.1 mol·L-1盐酸滴定20 mL 0.1 mol·L-1氨水,溶液的pH随加入盐酸体积的变化
D.图丁表示向Al2(SO4)3溶液中滴入NaOH溶液,生成Al(OH)3沉淀的量随NaOH溶液体积的变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图为直流电源电解稀Na2SO4水溶液的装置。通电后在石墨电极a和b附近分别滴加几滴石蕊溶液。下列实验现象中正确的是( )

A.逸出气体的体积,a电极的小于b电极的
B.一电极逸出无味气体,另一电极逸出刺激性气味气体
C.a电极附近呈红色,b电极附近呈蓝色
D.a电极附近呈蓝色,b电极附近呈红色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】新华网报道,我国固体氧化物燃料电池技术研发取得新突破。科学家利用该技术实现了H2S废气资源回收能量,并得到单质硫的原理如图所示。下列说法正确的是

A. 电极b为电池负极
B. 电路中每流过4mol电子,正极消耗44.8LH2S
C. 电极b上的电极反应为:O2+4e-+4H+=2H2O
D. 电极a上的电极反应为:2H2S+2O2--4e-=S2+2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】1g H2燃烧生成液态水放出142.9 kJ的热量,下列热化学方程式书写正确的是( )
A.2H2(g)+ O2(g) = 2H2O (1), ΔH = -142.9 kJ·mol-1
B.2H2(g)+ O2(g) = 2H2O (1), ΔH = -571.6 kJ·mol-1
C.2H2+O2= 2H2O, ΔH = -571.6 kJ·mol-1
D.H2(g)+![]() O2(g) = H2O (1), ΔH = +285.8 kJ·mol-1
O2(g) = H2O (1), ΔH = +285.8 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】从海水中提取试剂级NaCl及回收金属Mg的工业流程如图:
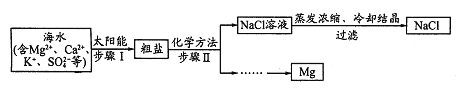
![]() 步骤I原理如图,在实验室中完成该步骤所用装置为 ______
步骤I原理如图,在实验室中完成该步骤所用装置为 ______ ![]() 填序号
填序号![]() 。
。
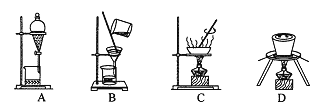
![]() 某学习小组设计了实验模拟步骤Ⅱ:
某学习小组设计了实验模拟步骤Ⅱ:
粗盐溶解![]() 过滤
过滤![]() NaCl溶液
NaCl溶液
![]() 该实验中加入
该实验中加入![]() 的作用是 ______ ;若向粗盐溶液中加入的是
的作用是 ______ ;若向粗盐溶液中加入的是![]() 浓溶液,则有难溶的
浓溶液,则有难溶的![]() 生成,同时有气体逸出.该反应的离子方程式为 ______。
生成,同时有气体逸出.该反应的离子方程式为 ______。
![]() 学习小组发现上述实验即使
学习小组发现上述实验即使![]() 用量不足,第
用量不足,第![]() 步沉淀中依然含有少量
步沉淀中依然含有少量![]() ,试从平衡角度分析 ______。
,试从平衡角度分析 ______。
![]() 在第
在第![]() 步后增加过滤,并从滤渣中得到
步后增加过滤,并从滤渣中得到![]() ,工业上通过电解获得Mg的化学方程式为 ______ ; 若
,工业上通过电解获得Mg的化学方程式为 ______ ; 若![]() 时直接将
时直接将![]() 熔融,然后用惰性电极电解,发现有固体剩余,则该固体可能是 ______
熔融,然后用惰性电极电解,发现有固体剩余,则该固体可能是 ______ ![]() 写化学式
写化学式![]() ;现有a g滤渣,用上二述方法处理回收Mg时产生标况下
;现有a g滤渣,用上二述方法处理回收Mg时产生标况下![]() ,剩余固体为c g。则滤渣中镁元素的质量分数为
,剩余固体为c g。则滤渣中镁元素的质量分数为 ![]() 不必化简
不必化简![]() 。
。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com