
【题目】(1)22克CO2的物质的量为_________mol,其中含有O原子的个数为_____________,含质子的物质的量为____mol,该气体在标准状况下的体积为_________L。
(2)写出下列反应的离子方程式。Fe2O3与稀盐酸反应_________________________________
(3)写出下列离子方程式对应的任意一个化学方程式。2H++CO32-![]() CO2↑+H2O __________________________________;
CO2↑+H2O __________________________________;
【答案】 0.5 6.02×1023 11 11.2 Fe2O3+6H+=2Fe3++3H2O Na2CO3+2HCl =2 NaCl +CO2↑+H2O
【解析】(1)CO2的摩尔质量为44g/mol,22克CO2为0.5mol,含有O原子的个数为0.5×2× 6.02×1023=6.02×1023;0.5molCO2含有质子的量为0.5×(6+8×2)=11mol; 0.5molCO2气体在标准状况下的体积为0.5×22.4=11.2L;正确答案:(1)0.5 ;(2)6.02×1023 ;(3)11;(4). 11.2。
(2)Fe2O3为金属氧化物,不溶于水,不能拆为离子,稀盐酸为强电解质溶液,能够拆成离子形式,生成物氯化铁为可溶于水的盐溶液,拆成离子形式,离子方程式为Fe2O3+6H+=2Fe3++3H2O;正确答案:Fe2O3+6H+=2Fe3++3H2O。
(3)满足该2H++CO32-![]() CO2↑+H2O的反应物的条件为:酸必须是强酸,碳酸盐必须是可溶性的,才能符合题意,酸可以为盐酸、硫酸、硝酸等,碳酸盐可以为碳酸钠、碳酸钾等; 正确答案:Na2CO3+2HCl =2 NaCl +CO2↑+H2O。
CO2↑+H2O的反应物的条件为:酸必须是强酸,碳酸盐必须是可溶性的,才能符合题意,酸可以为盐酸、硫酸、硝酸等,碳酸盐可以为碳酸钠、碳酸钾等; 正确答案:Na2CO3+2HCl =2 NaCl +CO2↑+H2O。


科目:高中化学 来源: 题型:
【题目】体积均为aL的盐酸和碳酸钠溶液,将碳酸钠溶液逐渐加入盐酸中与将盐酸逐渐加入碳酸钠溶液中产生的气体体积比为x:y(同温同压,且x不等于y),则原碳酸钠与盐酸溶液中溶质的物质的物质的量浓度之比为( )
A. x :y B. (x-2y) :x C. 2x :(2x-y) D. (2x-y) :2x
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】E是一种治疗心血管疾病的药物,它的合成路线如下: 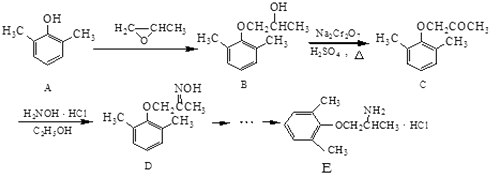
(1)C分子中含氧官能团的名称为 .
(2)由B→C的反应类型为 .
(3)由A制备B的过程中有少量副产物F,它与B互为同分异构体,F的结构简式为 .
(4)写出同时满足下列条件的D的一种同分异构体的结构简式: . ①属于α﹣氨基酸;
②是苯的衍生物,且苯环上的一氯代物只有两种;
③分子中含有两个手性碳原子.
(5)已知乙烯在催化剂作用与氧气反应可以生成环氧乙烷(). 写出以邻甲基苯酚 ( 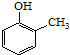 )和乙醇为原料制备
)和乙醇为原料制备  的合成路线流程图(无机试剂任用).
的合成路线流程图(无机试剂任用).
合成路线流程图示例如下:H2C=CH2 ![]() CH3CH2Br
CH3CH2Br ![]() CH3CH2OH.
CH3CH2OH.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图表示的反应关系中,部分产物被略去。已知2 mol白色固体粉末X受热分解,恢复到室温生成白色固体A、无色液体B和无色气体C各1 mol。X、E、G的焰色反应均为黄色。

回答下列问题:
(1)写出下列物质的化学式:G_____________ D_____________
(2)写出G与C反应生成D的化学反应方程式:____________________________
(3)写出X+E→A的离子方程式:______________________________________
(4)写出C与Na2O2反应的化学方程式:_____________________________,若有0.2 mol Na2O2参加反应则转移的电子数目为_____________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将①H+、②NH4+、③NO3﹣、④K+、⑤CO32﹣、⑥OH﹣分别加入H2O中,基本上不影响水的电离平衡的是( )
A.③④
B.②③⑥
C.①⑥
D.②④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有关化学反应的说法中,正确的是( )
A.自发反应都是放热反应
B.自发反应都是熵增加的反应
C.自发反应都是△G<0的反应
D.自发反应都是△G>0的反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有一份气体样品的质量是14.2 g,体积是4.48 L(标准状况下),该气体的摩尔质量是
( )。
A. 28.4 B. 28.4 g/mol C. 71 D. 71 g/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各表述与示意图一致的是( )
A.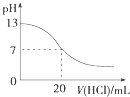
图表示25℃时,用0.1 molL﹣1盐酸滴定20 mL 0.1 molL﹣1 NaOH溶液,溶液的pH随加入酸体积的变化
B.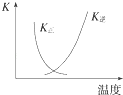 图中曲线表示反应2SO2(g)+O2(g)2SO3(g)△H<0正、逆反应的平衡常数K随温度的变化
图中曲线表示反应2SO2(g)+O2(g)2SO3(g)△H<0正、逆反应的平衡常数K随温度的变化
C.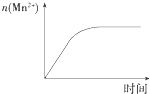
图表示10 mL 0.01 molL﹣1 KMnO4酸性溶液与过量的0.1 molL﹣1 H2C2O4溶液混合时,n(Mn2+)随时间的变化
D.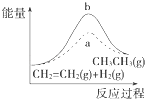
图中a、b曲线分别表示反应CH2═CH2(g)+H2(g)﹣→CH3CH3(g)△H<0使用和未使用催化剂时,反应过程中的能量变化
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com