
ЎҫМвДҝЎҝПВНјұнКҫөД·ҙУҰ№ШПөЦРЈ¬Іҝ·ЦІъОпұ»ВФИҘЎЈТСЦӘ2 mol°ЧЙ«№ММе·ЫД©XКЬИИ·ЦҪвЈ¬»ЦёҙөҪКТОВЙъіЙ°ЧЙ«№ММеAЎўОЮЙ«ТәМеBәНОЮЙ«ЖшМеCёч1 molЎЈXЎўEЎўGөДСжЙ«·ҙУҰҫщОӘ»ЖЙ«ЎЈ

»ШҙрПВБРОКМвЈә
ЈЁ1Ј©РҙіцПВБРОпЦКөД»ҜС§КҪЈәG_____________ D_____________
ЈЁ2Ј©РҙіцGУлC·ҙУҰЙъіЙDөД»ҜС§·ҙУҰ·ҪіМКҪЈә____________________________
ЈЁ3Ј©РҙіцXЈ«EЎъAөДАлЧУ·ҪіМКҪЈә______________________________________
ЈЁ4Ј©РҙіцCУлNa2O2·ҙУҰөД»ҜС§·ҪіМКҪЈә_____________________________Ј¬ИфУР0.2 mol Na2O2ІОјУ·ҙУҰФтЧӘТЖөДөзЧУКэДҝОӘ_____________________
Ўҫҙр°ёЎҝ NaAlO2 Al(OH)3 NaAlO2 Ј« CO2 Ј« 2H2O === Al(OH)3Ўэ Ј« NaHCO3»т2NaAlO2 Ј« CO2 Ј« 3H2O === 2Al(OH)3Ўэ Ј« Na2CO3 HCO![]() Ј« OHЈӯ === CO
Ј« OHЈӯ === CO![]() Ј« H2O 2CO2 Ј« 2Na2O2 === 2Na2CO3 Ј« O2 0.2 NA »т 1.204ЎБ1023
Ј« H2O 2CO2 Ј« 2Na2O2 === 2Na2CO3 Ј« O2 0.2 NA »т 1.204ЎБ1023
ЎҫҪвОцЎҝКФМв·ЦОцЈәұҫМвҝјІйОЮ»ъНЖ¶ПЈ¬»ҜС§·ҪіМКҪәНАлЧУ·ҪіМКҪөДКйРҙЈ¬Сх»Ҝ»№Фӯ·ҙУҰЦРЧӘТЖөзЧУКэөДјЖЛгЎЈBОӘОЮЙ«ТәМеЈ¬BУлNa2O2·ҙУҰЙъіЙөДEДЬУлAl·ҙУҰЈ¬ЗТEЎўGөДСжЙ«ОӘ»ЖЙ«Ј¬НЖіцBОӘH2OЎўEОӘNaOHЎўGОӘNaAlO2Ј»CКЗОЮЙ«ЖшМеЈ¬CДЬУлNa2O2·ҙУҰЙъіЙAЈ¬A+HClЎъCЈ¬ФтAОӘNa2CO3ЎўCОӘCO2Ј»2 mol°ЧЙ«№ММе·ЫД©XКЬИИ·ЦҪвЈ¬»ЦёҙөҪКТОВЙъіЙAЎўBЎўCёч1 molЈ¬XөДСжЙ«·ҙУҰіК»ЖЙ«Ј¬XОӘNaHCO3Ј»CУлG·ҙУҰЙъіЙDЈ¬CO2УлNaAlO2ИЬТә·ҙУҰЙъіЙөДDОӘAlЈЁOHЈ©3ЎЈ
ЈЁ1Ј©ёщҫЭЙПКц·ЦОцЈ¬GөД»ҜС§КҪОӘNaAlO2Ј¬DөД»ҜС§КҪОӘAlЈЁOHЈ©3ЎЈ
ЈЁ2Ј©G+CЎъDКЗCO2УлNaAlO2ИЬТәөД·ҙУҰЈ¬ИфCO2№эБҝЈ¬·ҙУҰөД»ҜС§·ҪіМКҪОӘNaAlO2+CO2+2H2O=AlЈЁOHЈ©3Ўэ+NaHCO3Ј»ИфCO2ЙЩБҝЈ¬·ҙУҰөД»ҜС§·ҪіМКҪОӘ2NaAlO2+CO2+3H2O=2Al(OH)3Ўэ+Na2CO3ЎЈ
ЈЁ3Ј©X+EЎъA·ҙУҰөД»ҜС§·ҪіМКҪОӘNaHCO3+NaOH=Na2CO3+H2OЈ¬·ҙУҰөДАлЧУ·ҪіМКҪОӘHCO3-+OH-=CO32-+H2OЎЈ
ЈЁ4Ј©CУлNa2O2·ҙУҰөД»ҜС§·ҪіМКҪОӘ2Na2O2+2CO2=2Na2CO3+O2Ј¬УГЛ«ПЯЗЕұкіцөзЧУЧӘТЖ·ҪПтәНКэДҝОӘЈә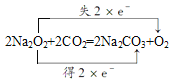 Ј¬2molNa2O2ІОјУ·ҙУҰЧӘТЖ2molөзЧУЈ¬Фт0.2molNa2O2ІОјУ·ҙУҰЧӘТЖ0.2molөзЧУЈ¬ЧӘТЖөзЧУКэОӘ0.2NA»т1.204
Ј¬2molNa2O2ІОјУ·ҙУҰЧӘТЖ2molөзЧУЈ¬Фт0.2molNa2O2ІОјУ·ҙУҰЧӘТЖ0.2molөзЧУЈ¬ЧӘТЖөзЧУКэОӘ0.2NA»т1.204![]() 1023ЎЈ
1023ЎЈ



| Дкј¶ | ёЯЦРҝОіМ | Дкј¶ | іхЦРҝОіМ |
| ёЯТ» | ёЯТ»Гв·СҝОіМНЖјцЈЎ | іхТ» | іхТ»Гв·СҝОіМНЖјцЈЎ |
| ёЯ¶ю | ёЯ¶юГв·СҝОіМНЖјцЈЎ | іх¶ю | іх¶юГв·СҝОіМНЖјцЈЎ |
| ёЯИэ | ёЯИэГв·СҝОіМНЖјцЈЎ | іхИэ | іхИэГв·СҝОіМНЖјцЈЎ |
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә МвРНЈә
ЎҫМвДҝЎҝПВБРОпЦКИЬУЪЛ®»б·ЕіцСхЖшөДКЗЈЁ Ј©
A.NaB.Na2O2C.NaOHD.Na2O
Ійҝҙҙр°ёәНҪвОц>>
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә МвРНЈә
ЎҫМвДҝЎҝОўЙъОпөзіШКЗЦёФЪОўЙъОпөДЧчУГПВҪ«»ҜС§ДЬЧӘ»ҜОӘөзДЬөДЧ°ЦГЈ¬Жд№ӨЧчФӯАнИзНјЛщКҫЈ®ПВБРУР№ШОўЙъОпөзіШөДЛө·ЁҙнОуөДКЗЈЁ Ј© 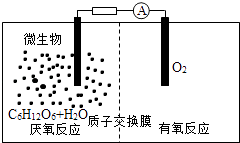
A.Хэј«·ҙУҰЦРУРCO2ЙъіЙ
B.ОўЙъОпҙЩҪшБЛ·ҙУҰЦРөзЧУөДЧӘТЖ
C.ЦКЧУНЁ№эҪ»»»ДӨҙУёәј«ЗшТЖПтХэј«Зш
D.өзіШЧЬ·ҙУҰОӘC6H12O6+6O2ЁT6CO2+6H2O
Ійҝҙҙр°ёәНҪвОц>>
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә МвРНЈә
ЎҫМвДҝЎҝТСЦӘЈә·ҙУҰaAЈЁgЈ©+bBЈЁgЈ©cCЈЁgЈ©ДіОВ¶ИПВЈ¬ФЪ2LөДГЬұХИЭЖчЦРН¶ИлТ»¶ЁБҝөДAЎўBЈ¬БҪЦЦЖшМеөДОпЦКөДБҝЕЁ¶ИЛжКұјдұд»ҜөДЗъПЯИзНјЛщКҫЈ® 
ЈЁ1Ј©ҙУ·ҙУҰҝӘКјөҪ12sКұЈ¬УГAұнКҫөД ·ҙУҰЛЩВКОӘЈ»
ЈЁ2Ј©ҫӯІв¶ЁЗ°4sДЪvЈЁCЈ©=0.05molL©Ғ1s©Ғ1 Ј¬ ФтёГ·ҙУҰөД»ҜС§·ҪіМКҪОӘЈ»
ЈЁ3Ј©ЗлФЪНјЦРҪ«ЙъіЙОпCөДОпЦКөДБҝЕЁ¶ИЛжКұјдөДұд»ҜЗъПЯ»жЦЖіцАҙЈ»
ЈЁ4Ј©ИфЙПКц·ҙУҰ·ЦұрФЪјЧЎўТТЎўұы ИэёцПаН¬өДГЬұХИЭЖчЦРҪшРРЈ¬ҫӯН¬Т»¶ОКұјдәуЈ¬ІвөГИэёцИЭЖчЦРөД·ҙУҰЛЩВК·ЦұрОӘЈә јЧЈәvЈЁAЈ©=0.3molL©Ғ1s©Ғ1Ј»
ТТЈәvЈЁBЈ©=0.12molL©Ғ1s©Ғ1Ј»
ұыЈәvЈЁCЈ©=9.6molL©Ғ1min©Ғ1Ј»
ФтјЧЎўТТЎўұыИэёцИЭЖчЦР·ҙУҰЛЩВКУЙҝмөҪВэөДЛіРтОӘ Ј®
Ійҝҙҙр°ёәНҪвОц>>
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә МвРНЈә
ЎҫМвДҝЎҝПВБРЛө·ЁЦРХэИ·өДКЗ(ЎЎЎЎ)
A. Тт·ўЙъјУіЙ·ҙУҰЈ¬ұҪҝЙТФК№деЛ®НКЙ«
B. ГәҝЙТФНЁ№эёЙБуЎўТә»ҜУлЖш»ҜөИОпАнұд»ҜЧӘ»ҜОӘЗеҪаДЬФҙ
C. МмИ»ЦІОпУНіЈОВПВТ»°гіКТәМ¬Ј¬ДСИЬУЪЛ®Ј¬УРәг¶ЁөДИЫөгЎў·Рөг
D. ·ЦЧУКҪОӘC8H10ЗТКфУЪ·јПгМюөДН¬·ЦТм№№МеУР4ЦЦ
Ійҝҙҙр°ёәНҪвОц>>
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә МвРНЈә
ЎҫМвДҝЎҝЈЁ1Ј©22ҝЛCO2өДОпЦКөДБҝОӘ_________molЈ¬ЖдЦРә¬УРOФӯЧУөДёцКэОӘ_____________,ә¬ЦКЧУөДОпЦКөДБҝОӘ____molЈ¬ёГЖшМеФЪұкЧјЧҙҝцПВөДМе»эОӘ_________LЎЈ
ЈЁ2Ј©РҙіцПВБР·ҙУҰөДАлЧУ·ҪіМКҪЎЈFe2O3УлПЎСОЛб·ҙУҰ_________________________________
ЈЁ3Ј©РҙіцПВБРАлЧУ·ҪіМКҪ¶ФУҰөДИОТвТ»ёц»ҜС§·ҪіМКҪЎЈ2H+Ј«CO32-![]() CO2ЎьЈ«H2O __________________________________Ј»
CO2ЎьЈ«H2O __________________________________Ј»
Ійҝҙҙр°ёәНҪвОц>>
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә МвРНЈә
ЎҫМвДҝЎҝДі»ҜС§РЛИӨРЎЧйЦЖИЎВИЛбјШЎЈЦЖИЎКөСйҪбКшәуЈ¬ИЎіцЙъіЙБЛВИЛбјШөДКФ№ЬАдИҙҪбҫ§Ўў№эВЛЎўПҙөУЎЈЗлјтКцПҙөУВИЛбјШҫ§МеөДІЩЧч__________________________________ЎЈ
Ійҝҙҙр°ёәНҪвОц>>
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә МвРНЈә
ЎҫМвДҝЎҝФЪ25ЎжКұЈ¬ДіПЎИЬТәЦРУЙЛ®өзАлІъЙъөДc(OHЈӯ)ЈҪ10Јӯ12mol/LЎЈПВБРУР№ШёГИЬТәөДРрКцХэИ·өДКЗ
A. ёГИЬТәТ»¶ЁіКЛбРФ
B. ёГИЬТәЦРөДc(HЈ«)ҝЙДЬөИУЪ10Јӯ3
C. ёГИЬТәөДpHҝЙДЬОӘ2Ј¬ҝЙДЬОӘ12
D. ёГИЬТәУРҝЙДЬіКЦРРФ
Ійҝҙҙр°ёәНҪвОц>>
ҝЖДҝЈәёЯЦР»ҜС§ АҙФҙЈә МвРНЈә
ЎҫМвДҝЎҝПВБРИЬТәәН100mL 0.5mol/L CaCl2ИЬТәЛщә¬өДClЈӯОпЦКөДБҝЕЁ¶ИПаН¬өДКЗ
A. 500mL 0.1mol/L MgCl2ИЬТә B. 100mL 0.5mol/L AlCl3ИЬТә
C. 50mL 1mol/L NaClИЬТә D. 25mL 0.5mol/L HClИЬТә
Ійҝҙҙр°ёәНҪвОц>>
№ъјКѧУУЕСЎ - Б·П°ІбБРұн - КФМвБРұн
әюұұКЎ»ҘБӘНшОҘ·ЁәНІ»БјРЕПўҫЩұЁЖҪМЁ | НшЙПУРәҰРЕПўҫЩұЁЧЁЗш | өзРЕХ©ЖӯҫЩұЁЧЁЗш | ЙжАъК·РйОЮЦчТеУРәҰРЕПўҫЩұЁЧЁЗш | ЙжЖуЗЦИЁҫЩұЁЧЁЗш
ОҘ·ЁәНІ»БјРЕПўҫЩұЁөз»°Јә027-86699610 ҫЩұЁУКПдЈә58377363@163.com