
【题目】按如图所示装置进行实验,并回答下列问题。
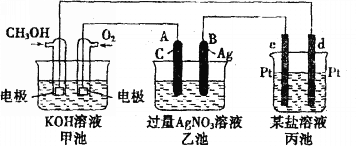
(1)甲池是_________池,通入CH3OH(甲醇)的电极作为_______极,电极反应式为________________________________________________。
(2)乙池是________池,A电极名称为______极,电极反应式为_______________________,乙池中的总反应化学方程式为________________________________,溶液的pH________(填“增大”、“减小”或“不变”)。
(3)当甲池中消耗O2 0.56L(标准状况下)时,理论上乙池中B极的质量增加_______g;此时丙装置中_____________(填“c”或“d”)电极析出1.20g金属,则丙装置中的某盐溶液可能是________(填序号)。
a.MgSO4溶液 b.CuSO4溶液 c.NaCl溶液 d.AgNO3溶液
【答案】 原电池 负 CH3OH - 6e- + 8OH-= CO32- + 6H2O 电解 阳 2H2O-4e- =O2↑++4H+ 或4OH--4e-=O2↑+2H2O 4AgNO3+2H2O ![]() 4Ag+O2↑+4HNO3 减小 10.8 【答题空10】d bd
4Ag+O2↑+4HNO3 减小 10.8 【答题空10】d bd
【解析】(1)甲池是燃料电池是原电电池装置,通入燃料CH3OH的电极是负极;甲醇失电子和氢氧根离子反应生成碳酸根离子和水,电极反应式为CH3OH-6e-+8OH-═6H2O+CO32-,故答案为:原电池;负;CH3OH-6e-+8OH-═6H2O+CO32-;
(2)乙为电解池,A与原电池正极相连,为电解池的阳极,发生氧化反应,电极方程式为4OH--4e-═O2↑+2H2O,乙池中电解硝酸银溶液,阳极生成氧气,阴极生成银,电解总反应式为4AgNO3+2H2O ![]() 4Ag+O2↑+4HNO3,生成H+,则溶液pH减小,故答案为:电解;阳;4OH--4e-═O2↑+2H2O;4AgNO3+2H2O
4Ag+O2↑+4HNO3,生成H+,则溶液pH减小,故答案为:电解;阳;4OH--4e-═O2↑+2H2O;4AgNO3+2H2O ![]() 4Ag+O2↑+4HNO3;减小;
4Ag+O2↑+4HNO3;减小;
(3)当甲池中消耗O2 0.56L(标准状况下)时,消耗氧气的物质的量为![]() =0.025mol,转移电子0.025mol ×4=0.1mol,B(Ag)极析出的是金属银,质量增加0.1mol×108g/mol =10.8g,此时丙池中d电极上发生还原反应,析出1.20g某金属,转移电子为0.1mol,反应过程中可能金属阳离子放电后,溶液中的氢离子继续放电。当析出一价金属时,其摩尔质量≥
=0.025mol,转移电子0.025mol ×4=0.1mol,B(Ag)极析出的是金属银,质量增加0.1mol×108g/mol =10.8g,此时丙池中d电极上发生还原反应,析出1.20g某金属,转移电子为0.1mol,反应过程中可能金属阳离子放电后,溶液中的氢离子继续放电。当析出一价金属时,其摩尔质量≥![]() =12g/mol,当析出的是二价金属,则其摩尔质量≥
=12g/mol,当析出的是二价金属,则其摩尔质量≥![]() ×2=24g/mol,a.MgSO4溶液中镁离子不能放电生成金属镁,错误;b.CuSO4溶液中铜离子可以放电生成铜,之后溶液中的氢离子放电,正确;c.NaCl溶液中的钠离子不能放电,不能析出金属,错误;d.AgNO3溶液的银离子可以放电形成银,之后氢离子放电,正确;故选bd;故答案为:10.8; d;bd 。
×2=24g/mol,a.MgSO4溶液中镁离子不能放电生成金属镁,错误;b.CuSO4溶液中铜离子可以放电生成铜,之后溶液中的氢离子放电,正确;c.NaCl溶液中的钠离子不能放电,不能析出金属,错误;d.AgNO3溶液的银离子可以放电形成银,之后氢离子放电,正确;故选bd;故答案为:10.8; d;bd 。


 导学全程练创优训练系列答案
导学全程练创优训练系列答案科目:高中化学 来源: 题型:
【题目】【题目】烃A的质谱图中,质荷比最大的数值为42。碳氢两元素的质量比为6:1,其核磁共振氢谱有三个峰,峰的面积比为1:2:3。A与其他有机物之间的关系如下:
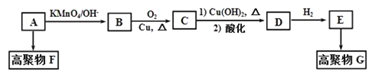
已知:CH2=CH2![]() HOCH2CH2OH,回答下列问题:
HOCH2CH2OH,回答下列问题:
(1)有机物B的分子式___________________________。
(2)高聚物F结构简式为___________________。
(3)写出C与新制的氢氧化铜反应的化学方程式___________________________。
(4)E在一定条件下可以相互反应生成一种六元环有机物H,H的结构简式________.。
(5)写出生成G的化学方程式_____________________________________________;
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氧化还原反应与四种基本类型反应的关系如图所示,则下列化学反应中属于阴影部分的是( )
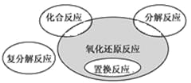
A. CuSO4 + Mg = Cu + MgSO4
B. 4NH3 + 5O2 = 4NO + 6H2O
C. 4Fe(OH)2 + O2 + 2H2O = 4Fe(OH)3
D. 2NaHCO3 =Na2CO3 + H2O + CO2 ↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】龙癸醛是一种珍贵香料,广泛应用于香料、医药、染料及农药等行业。其合成路线如图所示(部分反应产物和反应条件已略去)。

回答下列问题:
(1)下列有关R和烯烃C3H6的说法正确的是__________________。(填代号)
A.它们的实验式相同 B.它们都能使溴水褪色
C.它们都能发生加成反应 D.它们都含有碳碳双键
(2)反应⑤的试剂和条件是___________________________;反应③的类型是_____________________。
(3)T所含官能团的名称是________;反应④的化学方程式为__________________________________。
(4)X的名称是____________________。
(5)遇氯化铁溶液发生显色反应的T的同分异构体有________种,其中,在核磁共振氢谱上有4组峰且峰面积比为1∶2∶3∶6的结构简式为_______________________________________________。
(6)参照上述流程图,以2—甲基—1,3—丁二烯为原料,经三步制备2—甲基—1,4—丁二醛,设计合成路线:________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在2KMnO4+16HCl═2KCl+2MnCl2+5Cl2↑+8H2O反应中氧化剂与还原剂物质的量之比为( )
A.1:8
B.8:1
C.1:5
D.5:1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关物质用途的说法中,不正确的是
A.液氨可以作制冷剂
B.浓硫酸具有吸水性,可用于干燥氨气
C.二氧化硫可以漂白某些有色物质
D.氨和硝酸都能用于制造化肥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学生做如下实验:第一步,在淀粉KI溶液中,滴入少量NaClO溶液,并加入少量稀硫酸,溶液立即变蓝;第二步,在上述蓝色溶液中,滴加足量的Na2SO3溶液,蓝色逐渐消失。下列有关该同学对实验原理的解释和所得结论的叙述不正确的是( )
A. 氧化性:ClO->I2>SO42—
B. 蓝色消失的原因是Na2SO3溶液具有漂白性
C. 淀粉KI溶液变蓝是因为I-被ClO-氧化为I2,I2使淀粉变蓝
D. 若将Na2SO3溶液加入氯水中,氯水褪色
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com