
【题目】下列离子方程式的书写正确的是
A. 漂白粉溶液中通入SO2气体:Ca2++2ClO-+SO2+H2O===CaSO3↓+2HClO
B. 碳酸氢钙溶液中加入过量的氢氧化钠溶液:HCO![]() +OH-===CO
+OH-===CO![]() +H2O
+H2O
C. 向Fe2(SO4)3溶液中加入过量铁粉:2Fe3++Fe===3Fe2+
D. 向Na2SiO3溶液中滴加稀盐酸:Na2SiO3+2H+===H2SiO3↓+2Na+
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】X、Y、Z、W有如图所示的转化关系(反应条件和部分其它反应物省略),则X、Y、Z可能是
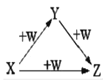
①Na、Na2O、Na2O2 ②A1Cl3、A1(OH)3、NaA1O2
③)Fe、FeCl2、FeCl3 ④NaOH、Na2CO3、NaHCO3
A. ①②④ B. ②④ C. ①②③ D. ①②③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究小组在实验室探究氨基甲酸铵(NH2COONH4)分解反应平衡常数和水解反应速率的测定.
(1)将一定量纯净的氨基甲酸铵置于特制的密闭真空容器中(假设容器体积不变,固体试样体积忽略不计),在恒定温度下使其达到分解平衡:NH2COONH4(s)2NH3(g)+CO2(g).实验测得不同温度下的平衡数据列于下表:
温度(℃) | 15.0 | 20.0 | 25.0 | 30.0 | 35.0 |
平衡总压强(kPa) | 5.7 | 8.3 | 12.0 | 17.1 | 24.0 |
平衡气体总浓度(×10﹣3mol/L) | 2.4 | 3.4 | 4.8 | 6.8 | 9.4 |
①可以判断该分解反应已经达到化学平衡的是(填字母).
A.2v(NH3)=v(CO2) B.密闭容器中总压强不变
C.密闭容器中混合气体的密度不变 D.密闭容器中氨气的体积分数不变
②根据表中数据,计算25.0℃时的分解平衡常数为 .
(2)已知:NH2COONH4+2H2ONH4HCO3+NH3H2O.该研究小组分别用三份不同初始浓度的氨基甲酸铵溶液测定水解反应速率,得到c(NH2COO﹣)随时间变化趋势如图所示.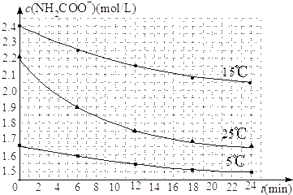
③计算25℃时,0~6min氨基甲酸铵水解反应的平均速率为 .
④根据图中信息,如何说明水解反应的平均速率随温度升高而增大: .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化工原料红矾钠(重铬酸钠:Na2Cr2O72H2O)主要是以铬铁矿(主要成分为FeOCr2O3 , 还含有Al2O3、SiO2等杂质)为主要原料生产,其主要工艺流程如下: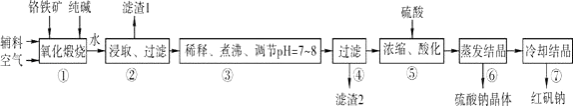
步骤①中主要反应的化学方程式如下:
4FeOCr2O3+8Na2CO3+7O2═8Na2CrO4+2Fe2O3+8CO2
(1)①中反应是在回转窑中进行的,反应时需不断搅拌,其作用是 .
(2)杂质Al2O3在①中转化的化学反应方程式为 .
(3)用化学平衡移动原理说明③中煮沸的作用是(用离子方程式结合文字说明),若调节pH过低产生的影响是 .
(4)⑤中酸化是使CrO42﹣转化为Cr2O72﹣写出该反应的离子方程式: . 
(5)工业上还可用电解法制备重铬酸钠,其装置示意图如上.阴极的电极反应式为;
阳极的电极反应式为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】小闵同学拥有下列实验仪器:

(1)写出仪器名称:c______。
(2)实验室用氯酸钾和二氧化锰制取氧气:
①上述仪器中不需要用到的是(填序号)_____。
②在用排水法收集氧气的过程中,判断集气瓶中氧气已集满的现象是______。
A.集气瓶中水位下降了;
B.在水槽中出现气泡;
C.将带火星的木条放在集气瓶口,木条复燃。
③要从反应后的剩余固体中回收二氧化锰,需要以下操作步骤:______、______、洗涤、烘干。
④小闵是否可以用向上排空气法收集氧气______(填写是或否)。
⑤小闵若在实验室利用12.25g氯酸钾与3gMnO2混合加热,列式计算最多可以得到多少物质的量的氧气____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】呵护生存环境,共建和谐社会是当今社会的主题.
(1)扬州市六圩污水处理厂三期工程不仅是“十二五”期间淮河流域水污染防治规划工程,也是我市今年重点减排项目.处理废水时加入明矾可作为混凝剂以吸附水中的杂质,明矾的化学式为;漂白粉能杀菌消毒,其作用原理可用化学方程式表示为 .
(2)现在人们使用乙醇汽油作为汽车燃料充分体现了低碳经济,物质的量相同的乙醇与汽油(设为C8H18)均完全燃烧产生的CO2的物质的量之比为 .
(3)废旧的钢圈、轮胎应投入如图所示 (填“A”或“B”)标志的垃圾桶中.下列污水处理方法只涉及物理变化的是 . 
A.过滤法
B.氧化还原法
C.中和法
D.化学沉淀法.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】完成下列流程图。
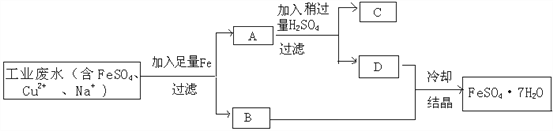
(1)其中,滤渣A中有______________,滤液D中溶质有________________。(填化学式)
(2))加入Fe的目的是_______________________________________。(用化学方程式表示)
(3)加入H2SO4的目的是____________________________________。(用化学方程式表示)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com