
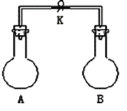
【题目】如图所示,室温下,A、B两个容积相等的烧瓶中分别集满了两种气体(同温、同压),当取下K夹,使两烧瓶内气体充分接触后,容器内压强由小到大的顺序正确的是( )
编号 | ① | ② | ③ | ④ |
A中气体 | H2S | H2 | NH3 | NO |
B中气体 | SO2 | Cl2 | HCl | O2 |
A.②③④①B.③①④②
C.③②①④D.④③②①
【答案】B
【解析】
相同温度下,一定体积的容器中气体压强与气体的物质的量成之比,气体的物质的量越大其压强越大,结合发生的反应来解答。
设A.B中的体积均为V,
①中硫化氢与二氧化硫反生成硫单质和水,2H2S+SO2=3S↓+2H2O,反应后气体体积减小,剩余SO2气体体积0.5V;
②中氢气和氯气在常温下不反应,气压不变,剩余气体为2V;
③中氨气和氯化氢反应生成氯化铵,反应后气体压强为零,剩余气体为0;
④中一氧化氮和氧气化合会生成二氧化氮,即2NO+O2═2NO2,然后发生2NO2N2O4,反应后气体体积减小,剩余O2气体体积为积0.5V,生成NO2体积V,剩余气体总体积约1.5V;
则使两烧瓶内气体充分接触后,容器内压强由小到大的顺序为③①④②,答案选B。


 同步练习强化拓展系列答案
同步练习强化拓展系列答案科目:高中化学 来源: 题型:
【题目】铁与人类密切相关,几乎无处不在,地壳中大约5%是铁,是含量仅次于铝的金属.根据所学知识回答下列问题:
(1)铁原子价电子轨道表示式为______,与铁同周期的元素的基态原子中,最外层电子数与铁相同的元素共有_____种(包含铁)。
(2)下列关于铁的说法,不正确的是_____(填选项字母)
A.基态铁原子的电子排布式1s22s22p63s23p103d24s2违反了泡利原理
B.铁属于黑色金属,在周期表中属于ds区元素
C.铁丝可用于焰色反应实验时蘸取待测物,是由于铁在光谱图中无特征的谱线
D.Fe能与CO形成配合物Fe(CO)5,配体CO中C是配原子
(3)某铁的化合物结构简式如图所示。

①组成上述化合物中5种元素原子电负性由小到大的顺序为_____。
②上述化合物中氮原子的杂化方式有_____。
③在图中用“→”标出亚铁离子的配位键_____。
(4)类卤素离子SCN-可用于Fe3+的检验,其对应的酸有两种,分别为硫氰酸(H-S-C≡N)和异硫氰酸(H-N=C=S),这两种酸中沸点较高的是后者,原因是_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知乙烯能发生以下转化:
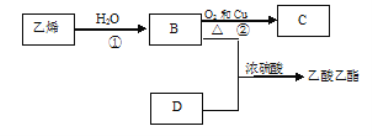
(1)乙烯的结构简式为:______________
(2)写出化合物官能团的化学式及名称:
①B中含官能团_________名称________;
②D中含官能团__________名称_________;
(3)写出反应的化学方程式
①__________反应类型:___________
②__________反应类型:___________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯气(Cl2)是高中化学一种非常重要的气体单质,它是制备许多化工产品的原料。
Ⅰ.甲同学在实验室用体积比为1:3的氯气和空气(不参与反应)的混合气体与潮湿的碳酸钠反应来制备Cl2O,其实验装置如图所示。

已知:Cl2O熔点为-120.6℃,沸点为2.0℃,常温常压下为一种棕黄色气体。
(1)仪器B的名称为________,KMnO4与浓盐酸反应生成Cl2的离子方程式为________。
(2)装置C的作用为________,装置E中的现象是________。
(3)氯气与潮湿的碳酸钠制Cl2O的化学方程式为________。
Ⅱ.乙同学在实验室用Cl2和熔融的S反应制备S2Cl2,其实验装置如图所示。

已知:S2Cl2熔点为-76℃,沸点为138℃,常温下为橙黄色的液体,遇水易水解。
(4)W中盛放的试剂为________。
(5)乙同学应进行合理的操作顺序为________(填序号)。
a.点燃酒精灯 b.停止通氯气 c.开始通氯气 d.熄灭酒精灯
(6)检验S2Cl2和水反应的产生的气体为SO2的实验操作为________。
(7)本实验需改进的地方为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A是一种常见的单质,B、C为中学常见的化合物,A、B、C均含有元素X。它们有如下的转化关系(部分产物及反应条件已略去):下列判断正确的是( )

A.X元素可能为Al
B.X元素一定为金属元素
C.反应①和②互为可逆反应
D.反应①和②一定为氧化还原反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下的容积不变的密闭容器中,下列叙述不是可逆反应A(g)+3B(g)![]() 2C(g)+2D(s)达到平衡的标志的是
2C(g)+2D(s)达到平衡的标志的是
① C的生成速率与C的消耗速率相等 ②单位时间内生成amolA,同时生成3amolB
③ A、B、C的浓度不再改变 ④混合气体的密度不再改变
⑤ 混合气体的总压强不再改变 ⑥混合气体的总物质的量不再改变
⑦ A、B、C、D浓度之比为1:3:2:2
A. ②⑦ B. ②⑤⑦ C. ①③④⑦ D. ②⑤⑥⑦
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】空气明朝《天工开物》中有世界上最早的“火法”炼锌技术的记载,锌是生命体必需的微量元素,被称为“生命之花”。(已知阿伏加德罗常数的值为NA)
(1)基态![]() 原子核外的最高能层符号是________,基态
原子核外的最高能层符号是________,基态![]() 最外层电子排布式为________。
最外层电子排布式为________。
(2)乳酸锌[ ]是一种很好的食品锌强化剂,其中存在的作用力有________(填编号)。
]是一种很好的食品锌强化剂,其中存在的作用力有________(填编号)。![]() 乳酸锌中含有________个σ键。
乳酸锌中含有________个σ键。
A.离子键 B.极性共价键 C.金属键 D.配位键 E.范德华力
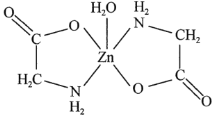
(3)一水合甘氨酸锌是一种矿物类饲料添加剂,结构简式如图所示。其中所涉及的非金属元素的电负性由大到小的顺序是________,![]() 分子的空间构型为________形,
分子的空间构型为________形,![]() 的配位数为________。甘氨酸(
的配位数为________。甘氨酸(![]() )中N原子的杂化轨道类型为________;甘氨酸易溶于水,试从结构角度解释________。
)中N原子的杂化轨道类型为________;甘氨酸易溶于水,试从结构角度解释________。
(4)Zn与S形成某种化合物的晶胞如图所示。

![]()
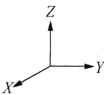
①以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子分数坐标。例如图中原子1的坐标为![]() ,则原子2的坐标为________。
,则原子2的坐标为________。
②已知晶体密度为![]() ,
,![]() 半径为
半径为![]() ,若要使
,若要使![]() 、
、![]() 相切,则
相切,则![]() 半径为________
半径为________![]() (写计算表达式)。
(写计算表达式)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】-钒和五氧化二钒在工业中应用广泛,某工厂从钒渣(主要成分有 V2O3、FeO,还含有少量 CuO、Al2O3 等)中回收金属,工艺流程如图:
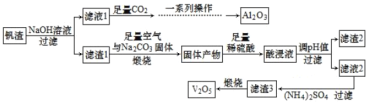
已知:①KspCu(OH)2=1.0×10-21,KspFe(OH)3=4.0×10-38 ,KspFe(OH)2=8.0×10-16
②NH4VO3 难溶于水,(VO2)2SO4 易溶于水。
(1)制取纯净的 Al2O3 需要经过“一系列操作”为过滤、___、___。
(2)滤渣 1 在“煅烧”过程中,主要成分 V2O3 转化为可溶性 NaVO3,写出其反应的化学方程式______ 。
(3)加入稀硫酸后,酸浸液中 VO![]() 与 VO
与 VO![]() 能大量共存的原因是______ (用离子方程式解释)。
能大量共存的原因是______ (用离子方程式解释)。
(4)常温下调节酸浸液的 pH=___,即可以完全除去铁、铜两种元素对应的离子; 实际 pH 值要调整到 8,其目的是______。
(5)请写出煅烧滤渣 3 时,发生反应的化学方程式 ________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在容积一定的密闭容器中,置入一定量的一氧化氮和足量碳发生化学反应:C(s)+2NO(g)![]() CO2(g)+N2(g),平衡时c(NO)与温度T的关系如图所示,则下列说法正确的是( )
CO2(g)+N2(g),平衡时c(NO)与温度T的关系如图所示,则下列说法正确的是( )
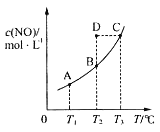
A.该反应的ΔH>0
B.若该反应在T1、T2℃时的平衡常数分别为K1、K2,则K1<K2
C.在T2℃时,若反应体系处于状态D,则此时v正>v逆
D.若状态B、C、D的压强分别为p(B)、p(C)、p(D),则p(C)=p(D)>p(B)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com