
【题目】反应C2H6(g)![]() C2H4(g)+H2(g) △H>0,在一定条件下于密闭容器中达到平衡。下列各项措施中,不能提高乙烷平衡转化率的是( )
C2H4(g)+H2(g) △H>0,在一定条件下于密闭容器中达到平衡。下列各项措施中,不能提高乙烷平衡转化率的是( )
A. 增大容器容积B. 升高反应温度
C. 分离出部分氢气D. 等容下通入惰性气体
科目:高中化学 来源: 题型:
【题目】将纯锌片和纯铜片按图示方式插入同浓度的稀硫酸中一段时间,以下叙述正确的是 ( )

A. 两烧杯中溶液的pH均增大
B. 甲中铜片是正极,乙中铜片是负极
C. 两烧杯中铜片表面均无气泡产生
D. 产生气泡的速度甲比乙慢
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图表示一些晶体中的某些结构,它们分别是NaCl、CsCl、干冰、金刚石、石墨结构中的某一种的某一部分。

(1)其中代表金刚石的是(填编号字母,下同)____,其中每个碳原子与______个碳原子最接近且距离相等。金刚石属于________晶体。
(2)其中代表NaCl的是________,每个Na+周围与它最接近且距离相等的Na+有________个。
(3)代表干冰的是________,它属于________晶体,每个CO2分子与______个CO2分子紧邻。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】所示A、B、C、X均为中学化学常见物质,一定条件下它们有如图所示转化关系(其它产物已略去),下列说法错误的是

A.若A为AlCl3,则 X可能为KOH溶液
B.A也有可能是Na
C.若X可能为CO2,则C可能为NaHCO3溶液
D.若X为O2,C可能是CO等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、M、N、Q、P为元素周期表前四周期的7种元素。其中,X原子核外的M层中只有两对成对电子,Y原子核外的L层电子数是K层的两倍,Z是地壳内含量最高的元素,M的内层电子数是最外层电子数的9倍,N的原子序数比M小1,Q在元素周期表的各元素中电负性最大。P元素的第三电子层处于全充满状态,第四电子层只有一个电子。请回答下列问题:
(1)基态X的外围电子电子排布图为_____,P元素属于_____ 区元素。
(2)XZ2分子的空间构型是_____,YZ2分子中Y的杂化轨道类型为_____,相同条件下两者在水中的溶解度较大的是_____(写分子式),理由是_____。
(3)含有元素N的盐的焰色反应为____色,许多金属盐都可以发生焰色反应,其原因是___。
(4)元素M与元素Q形成晶体中,M离子与Q离子的配位数之比为_____。
(5)P单质形成的晶体中,P原子采取的堆积方式为_____,P原子采取这种堆积方式的空间利用率为_____(用含π表达式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,AgCl(s)![]() Ag+(aq)+Cl-(Aq)体系中,c(Ag+)和c(Cl-)的关系如图所示。下列说法正确的是( )
Ag+(aq)+Cl-(Aq)体系中,c(Ag+)和c(Cl-)的关系如图所示。下列说法正确的是( )
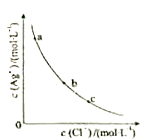
A. a、b、c三点对应的Ksp相等
B. AgCl在c点的溶解度比b点的大
C. AgCl溶于水形成的饱和溶液中,c(Ag+)=c(Cl-)
D. b点的溶液中加入AgNO3固体,c(Ag+)沿曲线向c点方向变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】元素周期表的一部分如图所示,W、X、Y、Z均为短周期主族元素,X与Z的最高正价之和与W的相等。下列说法错误的是
![]()
A.原子半径:X>Y>Z>W
B.X2W2中含有离子键和共价键
C.Y的最高价氧化物对应的水化物难溶于水
D.将由X、Z的单质组成的混合物放入冷水中,Z的单质不发生反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关气体体积的叙述正确的是( )
A.一定温度和压强下,各种气态物质体积的大小,由构成气体的分子大小决定
B.一定温度和压强下,各种气态物质体积的大小,由构成气体的分子数决定
C.不同的气体,若体积不同,则它们所含的分子数也不同
D.气体摩尔体积指1mol任何气体所占的体积约为22.4L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)化学平衡常数K表示可逆反应的进行程度,K值越大,表示______________________________,K值大小与温度的关系是:温度升高,K值____(填序号) 。
a.一定增大 b.一定减小 c.可能增大也可能减小
(2)在一体积为10L的容器中,通入一定量的CO和H2O,在850℃时发生如下反应:CO(g)十H2O(g)![]() CO2(g)十H2 (g) △H<0;CO和H2O浓度变化如下图,则0~4 min的平均反应速率v(CO)=______ mol/(L·min)
CO2(g)十H2 (g) △H<0;CO和H2O浓度变化如下图,则0~4 min的平均反应速率v(CO)=______ mol/(L·min)

(3)t1℃(高于850℃)时,在相同容器中发生上述反应,容器内各物质的浓度变化如上表。
①表中3 min~4 min之间的时间段,正逆反应速率的大小关系是v(正)______v(逆)(填 “>”、 “<”、 “=”或“无法确定”);C1_______0.08 mol/L (填 “>”、 “<”、 “=”)。
②反应在4 min~5 min之间,平衡向逆反应方向移动,可能的原因是_______(单选),表中5 min~6 min之间数值发生变化,可能的原因是_______(单选)。
a.增加水蒸气 b.降低温度 c.使用催化剂 d.增加氢气的浓度
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com