
【题目】A、B、C、D、E、F六种短周期主族元素,原子序数依次增大。下表为元素有关信息:
元素 | 信息 |
B | 其单质在常温下为双原子分子,与A可形成分子X,且X的水溶液呈碱性 |
D | 其简单阳离子与X具有相同电子数,且是同周期中简单阳离子中半径最小的 |
E | 元素原子最外层比次外层少2个电子 |
C、F | 两种元素的原子最外层共有13个电子 |
回答下列问题:
(1)B的原子结构示意图为__,且在周期表中的位置为___。
(2)写出BA3气体验满的方法__。
(3)F的单质在氧化还原反应中常做__剂,该单质与E的低价氧化物1:1通入水中,发生反应的离子方程式为__。
(4)C、D形成的化合物的化学式为__,此物质对应的水化物决定了在物质的分类中应属于__。
【答案】![]() 第二周期第VA族 用湿润的酚酞试纸靠近集气瓶口,试纸变红则收集满(或其他正确答案即可) 氧化 Cl2+SO2+2H2O = 4H+ + 2Cl- + SO42 Al2O3 两性氧化物
第二周期第VA族 用湿润的酚酞试纸靠近集气瓶口,试纸变红则收集满(或其他正确答案即可) 氧化 Cl2+SO2+2H2O = 4H+ + 2Cl- + SO42 Al2O3 两性氧化物
【解析】
A、B、C、D、E、F六种短周期主族元素,原子序数依次增大,B单质在常温下为双原子分子,与A可形成分子X,X的水溶液呈碱性,则X是NH3,A的原子序数小于B,所以A是H元素,B是N元素;D简单阳离子与X具有相同电子数,且是同周期中简单阳离子中半径最小的,电子层数相同的离子,离子半径随着原子序数的增大而减小,且D能形成阳离子,则D是Al元素;E元素的原子最外层比次外层少2个电子,E的原子序数大于D,且为短周期主族元素,则E为S,F为Cl;C、F原子最外层电子数共13个,F最外层含有7个电子,则C最外层含有6个电子,为第VIA族短周期元素,则C为O元素。
⑴通过以上分析知,B是N元素,N原子核外有2个电子层,最外层有5个电子,所以其原子结构示意图为:![]() ,周期表位置为第二周期第VA族;故答案为:
,周期表位置为第二周期第VA族;故答案为:![]() ;第二周期第VA族。
;第二周期第VA族。
⑵NH3气体验满的方法是用湿润的酚酞试纸靠近集气瓶口,试纸变红则收集满;故答案为:用湿润的酚酞试纸靠近集气瓶口,试纸变红则收集满(或其他正确答案即可)。
⑶F是Cl元素,氯气在化学反应中常常容易得电子而作氧化剂,在水溶液里,二氧化硫和氯气能发生氧化还原反应生成硫酸和盐酸,离子反应方程式为:Cl2 + SO2 + 2H2O = 4H+ + 2Cl-+ SO42;故答案为:氧化;Cl2+SO2+2H2O = 4H+ + 2Cl- + SO42。
⑷C是O元素,D是Al元素,所以C和D形成的化合物是Al2O3,氧化铝既能和强酸、强碱反应生成盐和水,所以氧化铝是两性氧化物;故答案为:Al2O3;两性氧化物。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】2019年诺贝尔化学奖授予了锂离子电池开发的三位科学家。一种锂离子电池的结构如图所示,电池反应式为 LixC6 + Li1-xCoO2![]() C6 + LiCoO2(x<1)。下列说法正确的是
C6 + LiCoO2(x<1)。下列说法正确的是
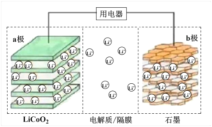
A.放电时,a极为负极
B.充电时,Li1-xCoO2/LiCoO2电极发生Li+脱嵌,放电时发生Li+嵌入
C.放电时,若转移0.02mol电子,石墨电极将减重0.21g
D.放电时,Li+在电解质中由a极向b极迁移
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示,把试管放入盛有25℃饱和石灰水的烧杯中,试管中开始放入几小块镁片,再滴入5mL稀盐酸。
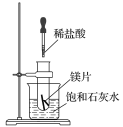
回答下列问题:
(1)实验中观察到的现象是________________。
(2)产生上述现象的原因是________________。
(3)写出有关反应的离子方程式____________。
(4)由实验推知,MgCl2溶液和H2的总能量________(填“大于”、“小于”或“等于”)镁片和盐酸的总能量。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】胡妥油(D)是香料的原料,它可由A合成得到:
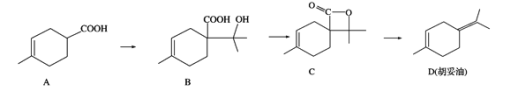
下列说法正确的是( )
A.有机物B的分子式为C11H19O3
B.1molB与足量的Na反应可产生11.2LH2(已换算成标准状况)
C.有机物C的所有同分异构体中不可能有芳香族化合物存在
D.一定条件下,A分别可以发生加成、取代、氧化等反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学对铜与浓硫酸反应产生的黑色沉淀进行探究,实验步骤如下:
Ⅰ.将光亮铜丝插入浓硫酸,加热;
Ⅱ.待产生黑色沉淀和气体时,抽出铜丝,停止加热;
Ⅲ.冷却后,从反应后的混合物中分离出黑色沉淀,洗净、干燥备用。
查阅文献:检验微量Cu2+的方法是:向试液中滴加K4[Fe(CN)6] 溶液,若产生红
褐色沉淀,证明有Cu2+。
(1)该同学假设黑色沉淀是CuO。检验过程如下:
①将CuO放入稀硫酸中,一段时间后,再滴加K4[Fe(CN)6] 溶液,产生红褐色沉淀。
②将黑色沉淀放入稀硫酸中,一段时间后,再滴加K4[Fe(CN)6] 溶液,未见红褐色沉淀。由该检验过程所得结论是_______________。
(2)再次假设,黑色沉淀是铜的硫化物。实验如下:
实验装置 | 现象 |
| 1. A试管中黑色沉淀逐渐溶解 |
①现象2说明黑色沉淀具有______性。
②能确认黑色沉淀中含有S元素的现象是_________,相应的离子方程式是_____________。
③为确认黑色沉淀是“铜的硫化物”,还需进行的实验操作是___________________。
(3)以上实验说明,黑色沉淀中存在铜的硫化物。进一步实验后证明黑色沉淀是CuS与Cu2S的混合物。将黑色沉淀放入浓硫酸中加热一段时间后,沉淀溶解,其中CuS溶解的化学方程式是_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】磁性材料A是由两种元素组成的化合物,某研究小组按如图流程探究其组成:
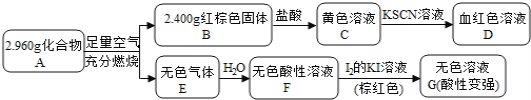
已知E是形成酸雨的主要气体,请回答:
(1)A的组成元素为______(用化学符号表示);
(2)C溶液可溶解铜片,写出该反应的离子方程式______________________________;
(3)写出F→G反应的化学方程式_________________________________,设计实验证明溶液G中含有![]() ____________________________________________________________________。
____________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】活性炭可处理大气污染物NO,反应原理:C(s)+2NO(g)![]() N2(g)+CO2(g)。T℃时,在2L密闭容器中加入0.100molNO和2.030mol活性炭(无杂质),平衡时活性炭物质的量是2.000mol。下列说法不合理的是
N2(g)+CO2(g)。T℃时,在2L密闭容器中加入0.100molNO和2.030mol活性炭(无杂质),平衡时活性炭物质的量是2.000mol。下列说法不合理的是
A.该温度下的平衡常数是:K=![]()
B.达到平衡时,NO的转化率是60%
C.3min末达到平衡,则v(NO)=0.01mol/(L·min)
D.若平衡时再加入0.100molNO,则达到新平衡时NO的转化率比原平衡时低
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关实验的图示及分析均正确的是
选项 | 实验目的 | 实验图示 | 实验分析 |
A | 实验室用酸性高锰酸钾溶液滴定草酸溶液 |
| 摇瓶时,使溶液向一个方向做圆周运动,勿使瓶口接触滴定管,溶液也不得溅出。 |
B | 石油分馏时接收馏出物 |
| 为收集到不同沸点范围的馏出物,需要不断更换锥形瓶。 |
C | 测定锌与稀硫酸反应生成氢气的速率 |
| 实验中,需测定的物理量是反应时间和生成氢气的体积。 |
D | 用四氯化碳萃取碘水中的碘 |
| 充分振荡后静置,待溶液分层后,先把上层液体从上口倒出,再让下层液体从下口流出。 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】右图是一种试验某气体化学性质的实验装置,图中B为开关。 如先打开B,在A处通入干燥氯气,C中红色布条颜色无变化;当关闭B时,C处红色布条颜色褪去。则D瓶中盛有的溶液是( )
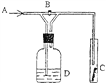
A. 浓H2SO4 B. 浓NaOH溶液
C. 饱和Na2SO4溶液 D. 石灰乳
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com